Lewis používal jednoduché diagramy (nyní se nazývají Lewisovy diagramy), aby zjistil, kolik elektronů se nachází ve vnější neboli valenční slupce daného atomu. Jádro atomu, tj. jádro spolu s vnitřními elektrony, je znázorněno chemickým symbolem a pouze valenční elektrony jsou nakresleny jako tečky obklopující chemický symbol. Tři atomy znázorněné na obrázku 1 z knihy Elektrony a valence lze tedy znázornit následujícími Lewisovými diagramy:
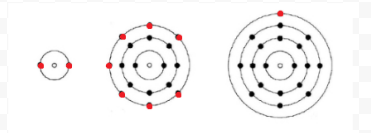

Je-li atom atomem vzácného plynu, jsou možné dva alternativní postupy. Buď můžeme uvažovat, že atom má nulové valenční elektrony, nebo můžeme považovat nejvzdálenější zaplněnou slupku za valenční slupku. První tři vzácné plyny lze tedy zapsat jako:
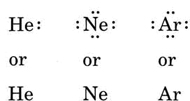
Příklad \(\PageIndex{1}\): Lewisovy struktury
Nakreslete Lewisovy diagramy pro atom každého z následujících prvků: Li, N, F, Na
Řešení
Z periodické tabulky na přední straně obálky zjistíme, že Li má atomové číslo 3. Obsahuje tedy tři elektrony, o jeden více než vzácný plyn He. To znamená, že vnější neboli valenční slupka obsahuje pouze jeden elektron a Lewisův diagram je
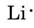
Podle stejné úvahy má N sedm elektronů, o pět více než He, zatímco F má devět elektronů, o sedm více než He, což dává
![]()
Na má o devět elektronů více než He, ale osm z nich je v jádře, což odpovídá osmi elektronům ve vnější slupce Ne. Protože Na má pouze o 1 elektron více než Ne, jeho Lewisův diagram je
![]()
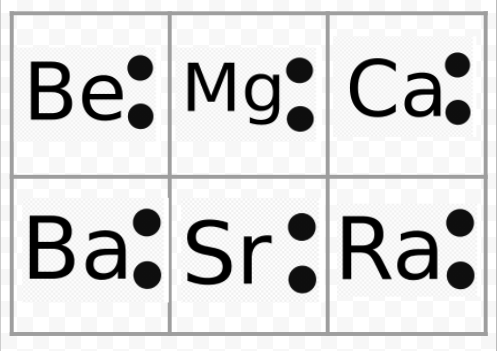
Podle předchozího příkladu si všimněte, že Lewisovy diagramy alkalických kovů jsou až na jejich chemické symboly totožné. To pěkně souhlasí s velmi podobným chemickým chováním alkalických kovů. Podobně vypadají Lewisovy diagramy pro všechny prvky v jiných skupinách, jako jsou alkalické zeminy nebo halogeny.
Lewisovy diagramy lze také použít k předpovědi valencí prvků. Lewis navrhl, že počet valencí atomu se rovná počtu elektronů v jeho valenční slupce nebo počtu elektronů, které by bylo třeba přidat do valenční slupky, aby bylo dosaženo struktury elektronické slupky dalšího vzácného plynu. Jako příklad této myšlenky uvažujme prvky Be a O. Jejich Lewisovy diagramy a diagramy vzácných plynů He a Ne jsou

Při porovnání Be s He vidíme, že první z nich má o dva elektrony více, a proto by měl mít valenci 2. U prvku O bychom mohli očekávat valenci 6 nebo valenci 2, protože má šest valenčních elektronů – o dva méně než Ne. Pomocí takto vypracovaných valenčních pravidel byl Lewis schopen vysvětlit pravidelné zvyšování a snižování dílčích indexů sloučenin v tabulce, kterou naleznete v části Valence a kterou zde reprodukujeme. Kromě toho byl schopen vysvětlit více než 50 % vzorců v tabulce. (Ty, které souhlasí s jeho představami, jsou v tabulce barevně vystínovány. Možná si nyní budete chtít tuto tabulku prohlédnout a ověřit si, že některé z uvedených vzorců odpovídají Lewisovým pravidlům). Lewisův úspěch v této souvislosti jasně naznačil, že nejdůležitějším faktorem, který drží atomy pohromadě při vzniku molekul, jsou elektrony.
Přes tyto úspěchy lze v Lewisových teoriích nalézt i potíže, zejména u prvků mimo vápník v periodické tabulce. Například prvek Br (Z = 35) má o 17 elektronů více než vzácný plyn Ar (Z = 18). To nás vede k závěru, že Br má 17 valenčních elektronů, z čehož je nepříjemné vysvětlit, proč se Br tak podobá Cl a F, přestože tyto dva atomy mají pouze sedm valenčních elektronů.
| Prvek | Atomová hmotnost | Vodík Sloučeniny | Sloučeniny kyslíku | Sloučeniny chloru |
|---|---|---|---|---|
| Vodík | 1.01 | H2 | H2O, H2O2 | HCl |
| Helium | 4.00 | Nevzniká | Nevzniká | Nevzniká |
| Lithium | 6.94 | LiH | Li2O, Li2O2 | LiCl |
| Berylium | 9.01 | BeH2 | BeO | BeCl2 |
| Boron | 10.81 | B2H6 | B2O3 | BCl3 |
| Uhlík | 12.01 | CH4, C2H6, C3H8 | CO2, CO, C2O3 | CCl4, C2Cl6 |
| Dusík | 14.01 | NH3, N2H4, HN3 | N2O, NO, NO2, N2O5 | NCl3 |
| Kyslík | 16.00 | H2O, H2O2 | O2, O3 | <Cl2O, ClO2, Cl2O7 |
| Fluor | 19.00 | HF | OF2, O2F2 | ClF, ClF3, ClF5 |
| Neon | 20.18 | Nevzniká | Nevzniká | Nevzniká |
| Sodík | 22.99 | NaH | Na2O, Na2O2 | NaCl |
| Hořčík | 24.31 | MgH2 | MgO | MgCl2 |
| Hliník | 26.98 | AlH3 | Al2O3 | AlCl3 |
| Křemík | 28.09 | SiH4, Si2H6 | SiO2 | SiCl4, Si2Cl6 |
| Fosfor | 30.97 | PH3, P2H4 | P4O10, P4O6 | PCl3, PCl5, P2Cl4 |
| Síra | 32.06 | H2S, H2S2 | SO2, SO3 | S2Cl2, SCl2, SCl4 |
| Chlor | 35.45 | HCl | Cl2O, ClO2, Cl2O7 | Cl2 |
| Draslík | 39.10 | KH | K2, K2O2, KO2 | KCl |
| Argon | 39.95 | Nevznikl | Nevznikl | Nevznikl |
| Vápník | 40.08 | CaH2 | CaO, CaO2 | CaCl2 |
| Skandium | 44.96 | Relativně nestabilní | Sc2O3 | ScCl3 |
| Titan | 47.90 | TiH2 | TiO2, Ti2O3, TiO | TiCl4, TiCl3, TiCl2 |
| Vanad | 50.94 | VH2 | V2O5, V2O3, VO2, VO | VCl4, VCl3, VCl2 |
| Chrom | 52.00 | CrH2 | Cr2O3, CrO2, CrO3 | CrCl3, CrCl2 |
Přispěvatelé
-
Ed Vitz (Kutztown University), John W. Moore (UW-Madison), Justin Shorb (Hope College), Xavier Prat-Resina (University of Minnesota Rochester), Tim Wendorff a Adam Hahn
.