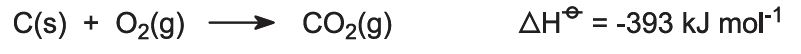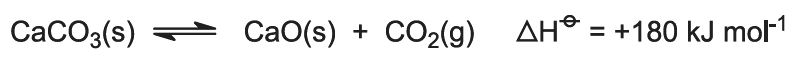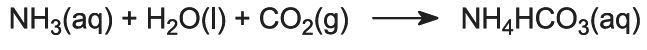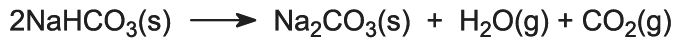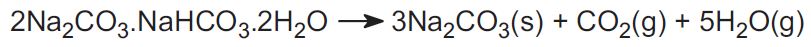- Zastosowanie węglanu sodu
- Roczna produkcja węglanu sodu
- Produkcja węglanu sodu
- (a) Z chlorku sodu i węglanu wapnia
- (1) Amonifikacja solanki
- (2) Tworzenie się tlenku wapnia i ditlenku węgla
- (3) Wieża Solvay’a
- (4) Oddzielanie stałego wodorowęglanu sodu
- (5) Tworzenie węglanu sodu
- (6) Tworzenie wodorotlenku wapnia
- (7) Regeneracja amoniaku
- (b) Z rud trony i nahcolitu
Zastosowanie węglanu sodu
Używane są dwie formy węglanu sodu (soda kalcynowana) – ciężka i lekka. Najpierw otrzymuje się postać lekką, a następnie część z nich przekształca się w postać ciężką. Lekki węglan sodu zawiera mniej niż 0,5% chlorku sodu. Ciężki węglan sodu jest otrzymywany przez uwodnienie lekkiego węglanu sodu do monohydratu (Na2CO3.H2O), a następnie odwodnienie go w celu otrzymania produktu o zwiększonej wielkości i gęstości kryształu.
Te dwa gatunki mają różne zastosowania.
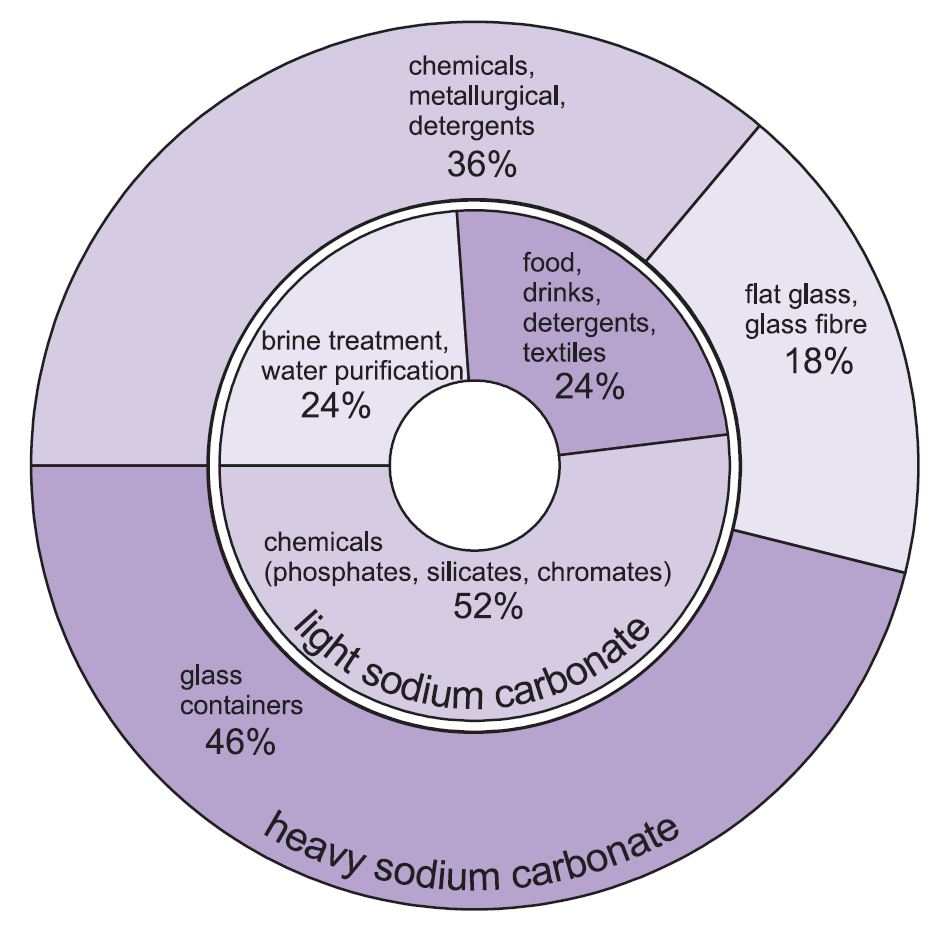
Główne zastosowania ciężkiego węglanu sodu są jako ciało stałe, szczególnie w produkcji szkła, gdzie jest używany jako topnik w topieniu krzemionki (piasku).
Zastosowanie lekkiego węglanu sodu jest tradycyjnie tam, gdzie substancja chemiczna jest wymagana w roztworze.
Rysunek 1 Zastosowania ciężkiego i lekkiego węglanu sodu.
Ogółem, około 50% całkowitej produkcji węglanu sodu jest wykorzystywane do produkcji szkła, 18% do produkcji innych chemikaliów i 10% w mydłach i detergentach.
Roczna produkcja węglanu sodu
Chiny są największym na świecie producentem węglanu sodu, stanowiąc 46% światowej produkcji, a USA 23%. (IHS Markit, 2015)
| Świat | 52 mln ton1,2 |
| Chiny | 25 mln ton3 |
| U.S.A. | 12 mln ton1 |
| Europa | 11 mln ton |
| Rosja | 0.71 mln ton4 |
Dane pochodzą z:
1. 2018 Elements of the Business of Chemistry, American Chemistry Council.
2. Spośród nich 14,7 ton jest wydobywanych. Zdecydowana większość wydobywana jest w Stanach Zjednoczonych (11,7 mln ton) i Turcji (2 mln ton). Pozostała część powstaje z chlorku sodu i węglanu wapnia.
3. IHS Markit, 2015
4. Federalna Służba Statystyki Państwowej: Federacja Rosyjska 2011
Produkcja węglanu sodu
Istnieją dwa główne źródła węglanu sodu:
a) z soli i węglanu wapnia (poprzez proces sodowania amoniakiem (Solvay))
b) z rud węglanu sodu i wodorowęglanu (trona i nahcolite)
(a) Z chlorku sodu i węglanu wapnia
Ogólna reakcja może być uważana za reakcję między węglanem wapnia i chlorkiem sodu:
Węglan wapnia jest jednak zbyt nierozpuszczalny, aby mógł reagować z roztworem soli. Zamiast tego produkt jest otrzymywany w serii siedmiu etapów.
Proces ten jest znany jako proces amoniakalno-sodowy lub proces Solvaya, nazwany tak na cześć belgijskiego chemika przemysłowego, który opatentował go w 186I.
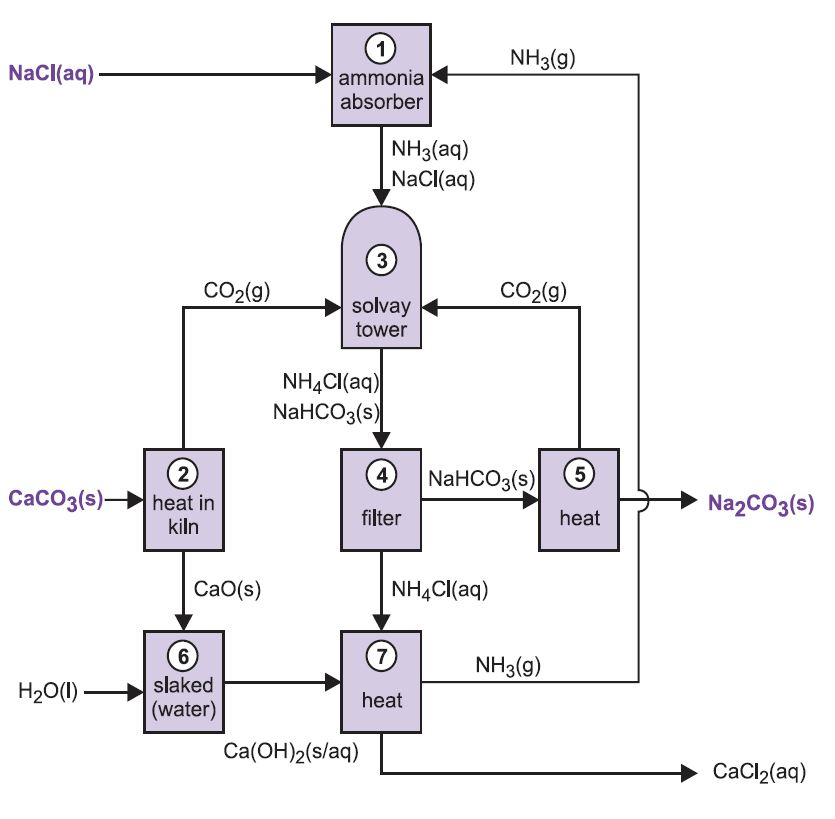
Różne etapy procesu Solvaya są ze sobą powiązane, jak widać na poniższym schemacie i opisie.
Rysunek 2 Różne etapy procesu Solvaya.
(1) Amonifikacja solanki
Amoniak jest absorbowany w stężonej solance, dając roztwór zawierający zarówno chlorek sodu, jak i amoniak. Obecne są jony Na+(aq), Cl-(aq), NH4+(aq), OH-(aq) i NH3(aq).
(2) Tworzenie się tlenku wapnia i ditlenku węgla
Kotły są zasilane mieszaniną wapienia i koksu (13:1 masowo). Koks spala się w przeciwprądzie wstępnie ogrzanego powietrza:
Ciepło spalania podnosi temperaturę pieca, a wapień ulega rozkładowi:
Gaz, zawierający około 40% dwutlenku węgla, jest uwalniany od pyłu wapiennego i przesyłany do wież karbonatyzacyjnych (Solvay). Pozostałość, tlenek wapnia, jest wykorzystywana do odzyskiwania amoniaku (patrz etap 7 poniżej).
(3) Wieża Solvay’a
Jest to kluczowy etap procesu. Solanka amoniakalna z etapu (1) jest przepuszczana w dół przez wieżę Solvaya, podczas gdy dwutlenek węgla z etapów (2) i (5) jest przepuszczany w górę. Wieża Solvaya jest wysoka i zawiera zestaw przegród w kształcie grzybka, które spowalniają i rozbijają przepływ cieczy, tak aby dwutlenek węgla mógł zostać skutecznie wchłonięty przez roztwór. Dwutlenek węgla, rozpuszczając się, reaguje z rozpuszczonym amoniakiem, tworząc wodorowęglan amonu:
Roztwór zawiera teraz jony Na+(aq), Cl-(aq), NH4+(aq) i HCO3-(aq). Spośród czterech substancji, które mogą powstać w wyniku różnych kombinacji tych jonów, wodorowęglan sodu (NaHCO3) jest najmniej rozpuszczalny. Wytrąca się on jako ciało stałe w dolnej części wieży, która jest schładzana. Proces netto jest następujący:
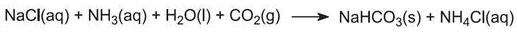
Z podstawy wieży wypływa zawiesina stałego wodorowęglanu sodu w roztworze chlorku amonu.
(4) Oddzielanie stałego wodorowęglanu sodu
Zawiesina jest filtrowana w celu oddzielenia stałego wodorowęglanu sodu od roztworu chlorku amonu, który jest następnie wykorzystywany w etapie (7).
(5) Tworzenie węglanu sodu
Wodorowęglan sodu jest ogrzewany w piecach obrotowych w temperaturze 450 K, tak że rozkłada się na węglan sodu, wodę i ditlenek węgla:
Ditlenek węgla jest przesyłany z powrotem do wieży Solvaya do wykorzystania w etapie (3). Produkt procesu, bezwodny węglan sodu, otrzymuje się jako drobny biały proszek znany jako lekki węglan sodu.
(6) Tworzenie wodorotlenku wapnia
Ostatnie dwa etapy, (6) i (7), dotyczą regeneracji amoniaku z chlorku amonu (wytworzonego w etapie 3). Wapno palone z etapu (2) jest rozcieńczane nadmiarem wody, co daje mleko wapienne:
(7) Regeneracja amoniaku
Ta zawiesina wodorotlenku wapnia jest mieszana z roztworem chlorku amonu pozostałym z etapu (4) i podgrzewana:
Amoniak jest w ten sposób odzyskiwany i przesyłany z powrotem do etapu (1). Chlorek wapnia jest jedynym produktem ubocznym całego procesu.
Całościowy proces jest elegancki. W teorii, jedynymi surowcami są wapień i solanka. Nieuchronnie występują straty amoniaku, które są wyrównywane przez dodanie dodatkowych dostaw, zgodnie z wymogami etapu (1).
(b) Z rud trony i nahcolitu
Proces Solvaya nie jest stosowany w USA. Zamiast tego, przemysł wykorzystuje dwie rudy i to stanowi około 30% światowej produkcji. Jedną z nich jest trona, występująca w ogromnych ilościach w Wyoming. Trona ma wzór:
Ruda jest wydobywana w postaci stałej i ogrzewana w celu usunięcia dwutlenku węgla, aby uzyskać węglan sodu:
Drugą rudą jest nahcolite, który jest wodorowęglanem sodu. Przy ogrzewaniu tworzy on węglan sodu.
.