- Normální sacharidová rovnováha a udržování hladiny glukózy v krviEdit
- PatofyziologieUpravit
- Zvýšený laktát a laktátová acidózaEdit
- Zvýšená hladina kyseliny močové a komplikaceUpravit
- Hyperlipidémie a účinky na plazmuUpravit
- HepatomegalieEdit
- Jaterní adenomyEdit
- Portální hypertenzeEdit
- OsteopenieEdit
- Účinky na ledvinyUpravit
- SplenomegalieEdit
- Účinky na střevaEdit
- Riziko infekceEdit
- Trombocytopenie a problémy se srážlivostí krveUpravit
- Vývojové účinkyEdit
Normální sacharidová rovnováha a udržování hladiny glukózy v krviEdit
Glykogen v játrech a (v menší míře) v ledvinách slouží jako forma uložené, rychle dostupné glukózy, aby bylo možné udržovat hladinu glukózy v krvi mezi jídly. Přibližně 3 hodiny po jídle obsahujícím sacharidy řídí vysoká hladina inzulínu jaterní buňky, aby odebíraly glukózu z krve, pomocí enzymu glukokinázy ji přeměňovaly na glukóza-6-fosfát (G6P) a přidávaly molekuly G6P na konce řetězců glykogenu (syntéza glykogenu). Přebytečný G6P se také přesouvá do výroby triglyceridů a vyváží se k uložení do tukové tkáně jako tuk.
Po dokončení trávení jídla klesne hladina inzulinu a enzymatické systémy v jaterních buňkách začnou odstraňovat molekuly glukózy z řetězců glykogenu ve formě G6P. Tento proces se označuje jako glykogenolýza. G6P zůstává v jaterní buňce, pokud není fosfát odštěpen glukóza-6-fosfatázou. Při této defosforylační reakci vzniká volná glukosa a volné anionty PO
4. Volné molekuly glukózy mohou být transportovány z jaterních buněk do krve, aby se udržel dostatečný přísun glukózy do mozku a dalších tělesných orgánů. Glykogenolýza dokáže pokrýt potřebu glukózy dospělého organismu na 12-18 hodin.
Pokud hladovění trvá déle než několik hodin, klesající hladina inzulínu umožňuje katabolismus svalových bílkovin a triglyceridů z tukové tkáně. Produkty těchto procesů jsou aminokyseliny (hlavně alanin), volné mastné kyseliny a kyselina mléčná. Volné mastné kyseliny z triglyceridů se přeměňují na ketony a na acetyl-CoA. Aminokyseliny a kyselina mléčná se používají k syntéze nového G6P v jaterních buňkách v procesu glukoneogeneze. Posledním krokem normální glukoneogeneze, stejně jako posledním krokem glykogenolýzy, je defosforylace G6P glukóza-6-fosfatázou na volnou glukózu a PO
Glukóza-6-fosfatáza tedy zprostředkovává poslední, klíčový krok v obou hlavních procesech tvorby glukózy během lačnění. Tento účinek je zesílen, protože výsledná vysoká hladina glukóza-6-fosfátu inhibuje dřívější klíčové kroky glykogenolýzy i glukoneogeneze.
PatofyziologieUpravit
Hlavními metabolickými účinky nedostatku glukóza-6-fosfatázy jsou hypoglykémie, laktátová acidóza, hypertriglyceridémie a hyperurikémie.

Hypoglykémie u GSD I se označuje jako „lačná“ nebo „postabsorpční“, obvykle asi 4 hodiny po úplném strávení jídla. Tato neschopnost udržet přiměřenou hladinu glukózy v krvi během lačnění je důsledkem kombinované poruchy glykogenolýzy i glukoneogeneze. Hypoglykémie nalačno je často nejvýznamnějším problémem u GSD I a obvykle vede k diagnóze. Chronická hypoglykémie vyvolává sekundární metabolické adaptace, včetně chronicky nízkých hladin inzulinu a vysokých hladin glukagonu a kortizolu.
Mléčná acidóza vzniká z poruchy glukoneogeneze. Kyselina mléčná vzniká v játrech i ve svalech a je oxidována pomocí NAD+ na kyselinu pyrohroznovou a poté přeměněna glukoneogenní cestou na G6P. Hromadění G6P inhibuje přeměnu laktátu na pyruvát. Hladina kyseliny mléčné stoupá během hladovění při poklesu glukózy. U lidí s GSD I nemusí klesnout zcela na normální hodnotu ani po obnovení normální hladiny glukózy.
Hypertriglyceridémie vyplývající ze zesílené produkce triglyceridů je dalším nepřímým účinkem poruchy glukoneogeneze, zesílené chronicky nízkou hladinou inzulinu. Během hladovění je narušena normální přeměna triglyceridů na volné mastné kyseliny, ketony a nakonec na acetyl-CoA. Hladiny triglyceridů u GSD I mohou dosahovat několikanásobku normálu a slouží jako klinický ukazatel „metabolické kontroly“.
Hyperurikémie je důsledkem kombinace zvýšené tvorby a sníženého vylučování kyseliny močové, která vzniká při metabolismu zvýšeného množství G6P cestou pentózového fosfátu. Je také vedlejším produktem degradace purinů. Kyselina močová soutěží s kyselinou mléčnou a dalšími organickými kyselinami o vylučování ledvinami v moči. U GSD I se zvýšená dostupnost G6P pro pentózofosfátovou dráhu, zvýšená rychlost katabolismu a snížené vylučování močí v důsledku vysokých hladin kyseliny mléčné kombinují tak, že hladina kyseliny močové je několikanásobně vyšší než normální. Ačkoli je hyperurikémie po léta asymptomatická, postupně dochází k poškození ledvin a kloubů.
Zvýšený laktát a laktátová acidózaEdit
Vysoké hladiny kyseliny mléčné v krvi jsou pozorovány u všech osob s GSD I v důsledku poruchy glukoneogeneze. Výchozí zvýšení se obvykle pohybuje od 4 do 10 mol/ml, což nezpůsobí žádný klinický dopad. Během a po epizodě nízké hladiny cukru v krvi se však hladina laktátu náhle zvýší a překročí 15 mol/ml, což je hranice pro vznik laktátové acidózy. Mezi příznaky laktátové acidózy patří zvracení a hyperpnoe, které mohou zhoršit hypoglykémii při GSD I. V případě akutní laktátové acidózy potřebují pacienti neodkladnou péči ke stabilizaci kyslíku v krvi a k obnovení glykémie. Správná identifikace laktátové acidózy u nediagnostikovaných dětí představuje problém, protože prvními příznaky jsou obvykle zvracení a dehydratace, které imitují dětské infekce, jako je gastroenteritida nebo pneumonie. Obě tyto běžné infekce navíc mohou u nediagnostikovaných dětí urychlit těžší hypoglykémii, což ztěžuje diagnostiku základní příčiny.
Při přetrvávání zvýšeného laktátu se dále zvyšuje aniontová mezera vlivem kyseliny močové, ketokyselin a volných mastných kyselin. U dospělých a dětí způsobují vysoké koncentrace laktátu značné potíže ve svalech. Tento diskomfort je zesílenou formou pocitu pálení, který může běžec pociťovat ve čtyřhlavém svalu stehenním po sprintu a který je způsoben krátkodobým nahromaděním kyseliny mléčné. Správná kontrola hypoglykémie u GSD I zcela vylučuje možnost vzniku laktátové acidózy.
Zvýšená hladina kyseliny močové a komplikaceUpravit
Vysoká hladina kyseliny močové se u pacientů s GSD I často vyskytuje jako důsledek zvýšené hladiny kyseliny mléčné. Při zvýšené hladině laktátu soutěží kyselina mléčná přenášená krví o stejný tubulární transportní mechanismus ledvin jako urát, což omezuje rychlost, s jakou může být urát ledvinami vylučován do moči. Pokud je přítomen zvýšený katabolismus purinů, je dalším přispívajícím faktorem. Hladiny kyseliny močové 6 až 12 mg/dl (530 až 1060 umol/l) jsou u pacientů s GSD I běžné, pokud není onemocnění řádně léčeno. U některých postižených osob je ke snížení hladiny urátů v krvi nutné užívání léku alopurinol. Mezi důsledky hyperurikémie u pacientů s GSD I patří vznik ledvinových kamenů a hromadění krystalů kyseliny močové v kloubech, což vede k onemocnění ledvin, respektive ke dně.
Hyperlipidémie a účinky na plazmuUpravit
Zvýšené triglyceridy u GSD I jsou důsledkem nízké hladiny inzulinu v séru u pacientů s častou dlouhodobou hypoglykémií. Může být také způsobeno intracelulární akumulací glukóza-6-fosfátu se sekundárním přesunem na pyruvát, který je přeměněn na acetyl-CoA, který je transportován do cytosolu, kde dochází k syntéze mastných kyselin a cholesterolu. Triglyceridy nad rozmezí 3,4 mmol/l (300 mg/dl) mohou způsobit viditelnou lipémii a dokonce mírnou pseudohyponatremii v důsledku snížené vodní frakce krevní plazmy. U GSD I je cholesterol obvykle jen mírně zvýšený ve srovnání s ostatními lipidy.
HepatomegalieEdit
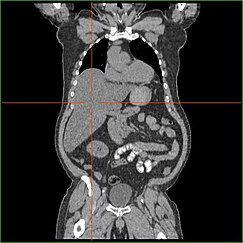
Narušení schopnosti jater provádět glukoneogenezi vede ke klinicky zjevné hepatomegalii. Bez tohoto procesu není tělo schopno uvolnit glykogen z jater a přeměnit jej na glukózu v krvi, což vede k hromadění uloženého glykogenu v játrech. Hepatomegalie z hromadění uloženého glykogenu v játrech se považuje za formu nealkoholického ztukovatění jater. Pacienti s GSD I mají určitý stupeň hepatomegalie po celý život, ale závažnost často souvisí s konzumací nadbytku sacharidů ve stravě. Snížení hmotnosti jater je možné, protože většina pacientů si zachovává reziduální jaterní funkci, která umožňuje uvolňování uloženého glykogenu v omezené míře.
Pacienti s GSD I mají často hepatomegalii již od narození. Ve fetálním vývoji mateřská glukóza přenesená na plod zabraňuje hypoglykémii, ale ukládání glukózy ve formě glykogenu v játrech vede k hepatomegalii. Neexistuje žádný důkaz, že by tato hepatomegalie představovala nějaké riziko pro správný vývoj plodu.
Hepatomegalie u GSD typu I se obvykle vyskytuje bez sympatického zvětšení sleziny. U pacientů s GSD Ib se může vyskytnout splenomegalie, ale ta souvisí s použitím filgrastimu k léčbě neutropenie u tohoto podtypu, nikoliv s komorbidní hepatomegalií. Hepatomegalie přetrvává v určitém stupni po celý život, často způsobuje vyklenutí břicha a v těžkých případech může být hmatná u pupku nebo pod ním. U nealkoholického ztukovatění jater souvisejícího s GSD je jaterní funkce obvykle zachována, jaterní enzymy a bilirubin zůstávají v normě. Jaterní funkce však mohou být v dospělosti ovlivněny dalšími jaterními komplikacemi, včetně vzniku jaterních adenomů.
Jaterní adenomyEdit
Specifická etiologie jaterních adenomů u GSD I zůstává i přes probíhající výzkum neznámá. Typickým pacientem s GSD I, u něhož se objeví alespoň jeden adenom, je dospělý člověk, ačkoli léze byly pozorovány i u čtrnáctiletých pacientů. Adenomy složené z heterogenních novotvarů se mohou vyskytovat jednotlivě nebo ve vícečetných skupinách. Odhady míry konverze hepatocelulárního adenomu v hepatocelulární karcinom u GSD I se pohybují od 0 % do 11 %, přičemž poslední údaj představuje novější výzkum. Jedním z důvodů zvyšujícího se odhadu je rostoucí populace pacientů s GSD I, kteří přežívají do dospělosti, kdy se vyvíjí většina adenomů.
Léčebné standardy nařizují pravidelné sledování jater pomocí MRI nebo CT ke sledování strukturálních abnormalit. Jaterní adenomy mohou být při zobrazovací diagnostice chybně identifikovány jako fokální nodulární hyperplazie, i když tento stav je vzácný. Jaterní adenomy u GSD I však jedinečně zahrnují difuzní Malloryho hyalinní depozita, která jsou jinak běžně pozorována u fokální nodulární hyperplazie. Na rozdíl od běžných jaterních adenomů souvisejících s perorální antikoncepcí je krvácení u pacientů s GSD I vzácné.
Přestože příčina vysokého výskytu adenomů u GSD I není jasná, výzkumy od 70. let 20. století uvádějí jako možnou příčinu sérový glukagon. Ve studiích se u pacientů, kterým byl nasazen dietní režim udržující hladinu cukru v krvi v normálním rozmezí zahrnujícím 72 až 108 mg/dl (4,0 až 6,0 mmol/l), prokázala snížená pravděpodobnost vzniku adenomů. U pacientů s dobře kontrolovanou hladinou glukózy v krvi se navíc trvale snižuje velikost a počet jaterních adenomů, což naznačuje, že adenomy mohou být způsobeny nerovnováhou hepatotropních látek, jako je sérový inzulín a zejména sérový glukagon v játrech.
Portální hypertenzeEdit
OsteopenieEdit
U pacientů s GSD I se často vyvine osteopenie. Konkrétní etiologie nízké minerální hustoty kostí u GSD není známa, ačkoli je silně spojena se špatnou metabolickou kontrolou. Osteopenie může být způsobena přímo hypoglykémií nebo následnými endokrinními a metabolickými důsledky. Bylo důsledně prokázáno, že zlepšení metabolické kontroly předchází klinicky významné osteopenii u pacientů s GSD I nebo ji zvrátí. V případech, kdy osteopenie postupuje s věkem, je hustota kostního minerálu v žebrech obvykle závažnější než v obratlích. V některých případech klesne T-skóre hustoty kostního minerálu pod -2,5, což svědčí o osteoporóze. Existují určité důkazy, že osteopenie může souviset s přidruženými abnormalitami ledvin u GSD I, zejména s glomulární hyperfiltrací. Zdá se, že tento stav také reaguje na suplementaci vápníkem. V mnoha případech může hustota kostních minerálů vzrůst a vrátit se do normálního rozmezí při správné metabolické kontrole a samotné suplementaci vápníkem, což zvrátí osteopenii.
Účinky na ledvinyUpravit
Ledviny jsou obvykle o 10 až 20 % zvětšeny uloženým glykogenem. U dospělých s GSD I může chronické glomerulární poškození podobné diabetické nefropatii vést k selhání ledvin. GSD I se může projevovat různými ledvinovými komplikacemi. Renální tubulární abnormality související s hyperlaktatemií se objevují již v raném věku, pravděpodobně proto, že prolongovaná laktátová acidóza se častěji vyskytuje v dětství. Často se projeví jako Fanconiho syndrom s mnohočetnými poruchami renální tubulární reabsorpce, včetně tubulární acidózy s úbytkem bikarbonátů a fosfátů. Tyto tubulární abnormality se u GSD I obvykle zjišťují a monitorují pomocí vápníku v moči. Dlouhodobě mohou tyto odchylky zhoršovat nefropatii způsobenou kyselinou močovou, která je jinak způsobena hyperlaktatemií. V dospívání a později se může nezávisle vyvinout glomerulární onemocnění, které se zpočátku projevuje jako glomerulární hyperfiltrace indikovaná zvýšenou eGFR moči.
SplenomegalieEdit
Zvětšení sleziny (splenomegalie) je u GSD I časté a má dvě základní příčiny. U GSD Ia může být splenomegalie způsobena vztahem mezi játry a slezinou, který způsobuje, že se jedna z nich zvětšuje nebo zmenšuje tak, aby odpovídala relativní velikosti druhé, v menší míře. U GSD Ib je vedlejším účinkem používání filgrastimu k léčbě neutropenie.
Účinky na střevaEdit
Postižení střev může způsobit mírnou malabsorpci s mastnou stolicí (steatorea), ale obvykle nevyžaduje žádnou léčbu.
Riziko infekceEdit
Neutropenie je charakteristickým znakem GSD Ib, u GSD Ia chybí. Mikrobiologická příčina neutropenie u GSD Ib není dobře známa. Obecně lze říci, že problém vzniká v důsledku narušeného buněčného metabolismu neutrofilů, což vede ke zrychlené apoptóze neutrofilů. Neutropenie u GSD je charakterizována jak poklesem absolutního počtu neutrofilů, tak sníženou funkcí neutrofilů. Neutrofily využívají specifickou metabolickou dráhu G6P, která je závislá na přítomnosti G6Pázy-β nebo G6PT k udržení energetické homeostázy v buňce. Absence G6PT u GSD Ib tuto dráhu omezuje, což vede ke stresu endoplazmatického retikula, oxidačnímu stresu uvnitř neutrofilů a spouští předčasnou apoptózu. Faktor stimulující kolonie granulocytů (G-CSF), dostupný pod názvem filgrastim, může snížit riziko infekce. V některých případech může být G-CSF formulovaný jako pegfilgrastim, prodávaný pod obchodním názvem Neulasta, použit jako pomalu působící alternativa, která vyžaduje méně časté dávkování.
Trombocytopenie a problémy se srážlivostí krveUpravit
Narušená agregace krevních destiček je neobvyklým důsledkem chronické hypoglykémie, který se vyskytuje u pacientů s GSD I. Výzkum prokázal sníženou funkci krevních destiček, která je charakterizována sníženou spotřebou protrombinu, abnormálními agregačními reakcemi, prodlouženou dobou krvácení a nízkou adhezivitou krevních destiček. Závažnost poruchy funkce krevních destiček obvykle koreluje s klinickým stavem, přičemž nejzávažnější případy korelují s laktátovou acidózou a těžkou lipidemií. Může způsobit klinicky významné krvácení, zejména epistaxi. U pacientů s GSD I se navíc může vyskytnout trombocytopenie jako důsledek splenomegalie. Při splenomegalii mohou být různé hematologické faktory sekvestrovány ve tkáních sleziny, protože krev je filtrována přes tento orgán. To může snížit hladinu krevních destiček dostupných v krevním řečišti, což vede k trombocytopenii.
Vývojové účinkyEdit
Opoždění vývoje je potenciálním sekundárním účinkem chronické nebo opakované hypoglykémie, kterému však lze alespoň teoreticky předcházet. Normální neuronální a svalové buňky neexprimují glukóza-6-fosfatázu, a proto na ně GSD I nemá přímý vliv. Bez správné léčby hypoglykémie však běžně dochází k selhání růstu v důsledku chronicky nízké hladiny inzulínu, přetrvávající acidózy, chronického zvýšení katabolických hormonů a kalorické nedostatečnosti (nebo malabsorpce). Nejdramatičtější vývojová opoždění jsou často příčinou závažných (nejen přetrvávajících) epizod hypoglykémie.
.