はじめに
多くの研究が、研究者や研究助成機関、規制当局、スポンサー、出版社が、新しい研究の開始や助成、規制、スポンサー、出版準備時に先行研究を利用しないことを示しています。 特に人や動物を対象とする研究の場合、すでに知られていることの証拠を体系的に見直すことなく研究に着手することは、非倫理的、非科学的、そして無駄です。

そのため、EBRのコンセプトは価値ある研究の確保に焦点を当てることにしました。
多くの課題に対する私たちの答え:
- 研究のパフォーマンスを評価するために科学的手法を用いる
- 研究の実施方法を改善するために科学的手法を用いる
- 研究の実践を長期的に監視する
これらの目的を達成するために私たちは次のことを推進しています。
- …新しい研究を正当化し設計する際に、体系的かつ透明性のあるアプローチを用いる
- …新しい結果を既存の証拠の文脈に置く際に、体系的かつ透明性のあるアプローチを用いる
- …systematic reviewの作成、更新、普及をより効率的に行う
THUS:

従来、研究者は新しい研究課題を策定する際に、科学的環境や文脈、個人の興味や野心、知識ベース(疫学研究や基礎科学研究の裏付け)などを利用しました。 EBRアプローチでは、それに加えて、すべての先行研究を明示的に利用し、エンドユーザーの視点を考慮した体系的かつ透明性のあるアプローチを取るべきであると提案しています

、J Clin Epi.より. 2020
質問1:科学的著者が先行研究の全体像に言及する頻度は?
科学的著者が先行研究の全体像に言及する頻度を分析した研究では、一般的に体系的アプローチが欠けていることが判明した。 主な結論は、研究著者の1人が言ったように:
「特定のテーマについてどれだけ多くの無作為化臨床試験が行われたとしても、約半数の臨床試験はどれも引用していないか、そのうちの1つだけを引用しています」。 私がそういうことにシニカルであるのと同様に、状況がこれほど悪いとは思いませんでした」
スティーブ・グッドマン博士、ニューヨークタイムズ、2011年1月17日
グッドマンが言及していたのは、カレン・ロビンソンと共著で2011年に発表した研究です。 彼らは、2004年に発表された、4つ以上の無作為化対照試験(RCT)を組み合わせたメタ分析を含む、医療に関する問題のすべてのシステマティックレビュー(SR)を調査し、同じ領域内の3つ以上の研究に言及する可能性のある研究を特定しました。 含まれる研究の多くが10以上の先行研究を参照している可能性があるにもかかわらず、これらの研究の参照数の中央値は一貫して2でした!

ANSWER 1.参照元を変更する。 以前の類似試験を引用する際に、体系的で透明性のあるアプローチはほとんど使われていません。
質問2: 新しい研究を正当化するためにシステマティックレビューは使われていますか?
2014年から2016年に発表された622件のRCTの記述的横断的分析では、新しい研究の正当化としてSRに明示的に言及したのは20%のみでした。 44%は一度もSRを引用していない!

回答2: 系統的で透明なアプローチは、新しい研究を正当化するために使用されることはほとんどありません
質問3:新しい研究の設計を知らせるために系統的レビューが使用されていますか?
新しいRCTの計画と設計にSRが使用されているかどうかを確認するために資金援助のためのアプリケーションを使用したレトロスペクティブ研究です。 第1コホート(2006~2008年)では46件中42件(89%)がSRを参照し、第2コホート(2013年)では34件中34件(100%)がSRを参照していた。 しかし、治療比較の正当化以上に、新しい試験のデザインにSRを利用した研究は非常に少なかった(両コホートで>90%)。

回答3:新しい研究の設計に、体系的で透明なアプローチが用いられることはほとんどない
質問4: 著者はその結果を以前の類似研究の文脈に置いていますか?
一連の研究で、クラークとチャルマースは、5つの最高位の医学雑誌(JAMA;BMJ;NEJM;LancetおよびAnnals of Internal Medicine)で5月に出版されたRCTはほとんどSRを使っていないことを繰り返し示しました。
2013年にClarkeとHopewellはこのシリーズを更新し、時間をかけてもまだ改善が見られないことを発見し、RCTのわずか3%がその結果を統合した最新のシステマティックレビューを含み、わずか37%が新しい結果を文脈に置くための系統的な試みをしていることが分かりました
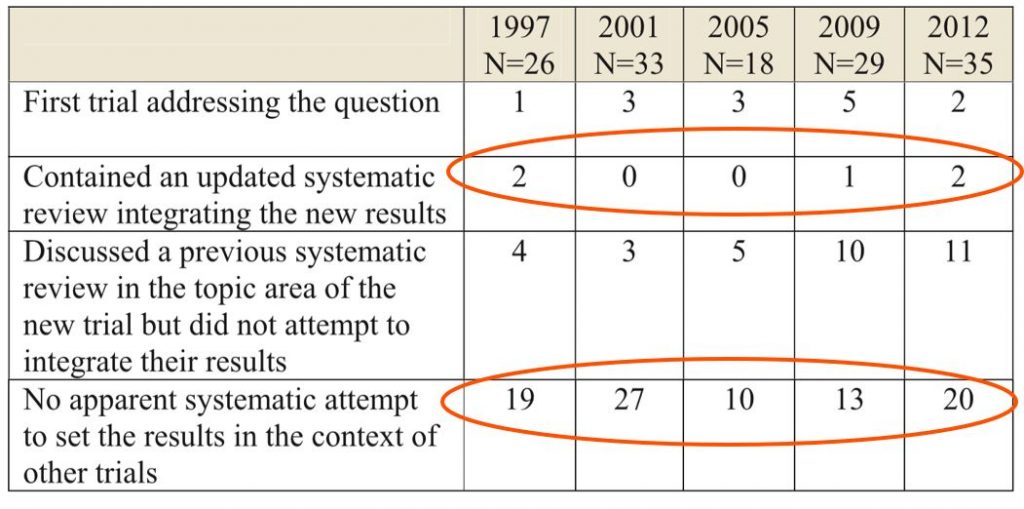
回答4:新しい結果を既存の結果の文脈に置くときに、体系的で透明なアプローチが用いられることはほとんどありません。
したがって、多くの人がすべての研究は証拠に基づいていると考えていますが、証拠はそうではないことを明確に示しています!
そのため:
- 我々は、研究者にもっと自分自身に要求を出し、それによってより信頼性があり価値のある成果を出すよう奨励しています。
- 我々は研究が自由でなければならないことに同意するが、無駄を増やすことを犠牲にしてはならない!
- 私たちは、新しい研究の計画や新しい結果の解釈を含め、研究のすべての段階が体系的かつ透明でなければならないと述べます
エビデンスに基づく研究ネットワーク

上記の問題に取り組むため、ノルウェー人とデンマーク人の研究者によるグループは、国際ネットワーク「エビデンスに基づく研究ネットワーク」を発足させたのでした。 EBRNetworkは、オーストラリア、カナダ、デンマーク、オランダ、ノルウェー、英国、米国の最初のパートナーと共に、2014年12月にノルウェーのベルゲンで設立された。
EBRNetworkの目的は、以下を促進することで研究の無駄を減らすことです:
- 既存のエビデンスのシステマティックレビューを事前に行わない新しい研究の禁止
- システマティックレビューの効率的な制作、更新、普及
EBRNetworkはシステマティックレビューの新しい作業定義を提案しています。
「システマティックレビューとは、あらかじめ定義された研究課題、包括基準、検索方法、選択手順、品質評価、データ抽出、データ分析からなる、オリジナル研究の構造的かつ計画的な統合のことである。 説明なしに意図的に除外される原著研究はなく、各研究の結果は結論を正当化するものでなければならない。”
2016年、EBRNetworkのメンバーは、BMJ「Towards evidence-based research」において、EBRと研究の無駄を防ぐための役割について論じた分析記事を発表しました。 この記事には、EBRの目的を満たすためのさまざまな関係者の責任を詳述したEBRステートメントと、EBRのフローチャートが含まれていました。

Lund H, et al BMJ. 2016
研究のパフォーマンスを評価するための科学的方法の使用
スコープレビュー(EBRNetworkが準備中)では、EBRコンセプトのさまざまな側面を扱う83のメタ研究研究が確認された。

2020年10月、Journal of Clinical Epidemiologyに、EBRの概念と新しい研究を正当化し結果を文脈に乗せるためのその使用をさらに展開する3つの論文が掲載された:
#1-根拠に基づく研究とは何か、なぜ重要か?
#2-価値を確認するために新しい研究を実施する前にEBRのアプローチを使用すること
#3-結論の有用性を確認するために研究を実施した後に結果を文脈に置くためにEBRのアプローチを使用すること
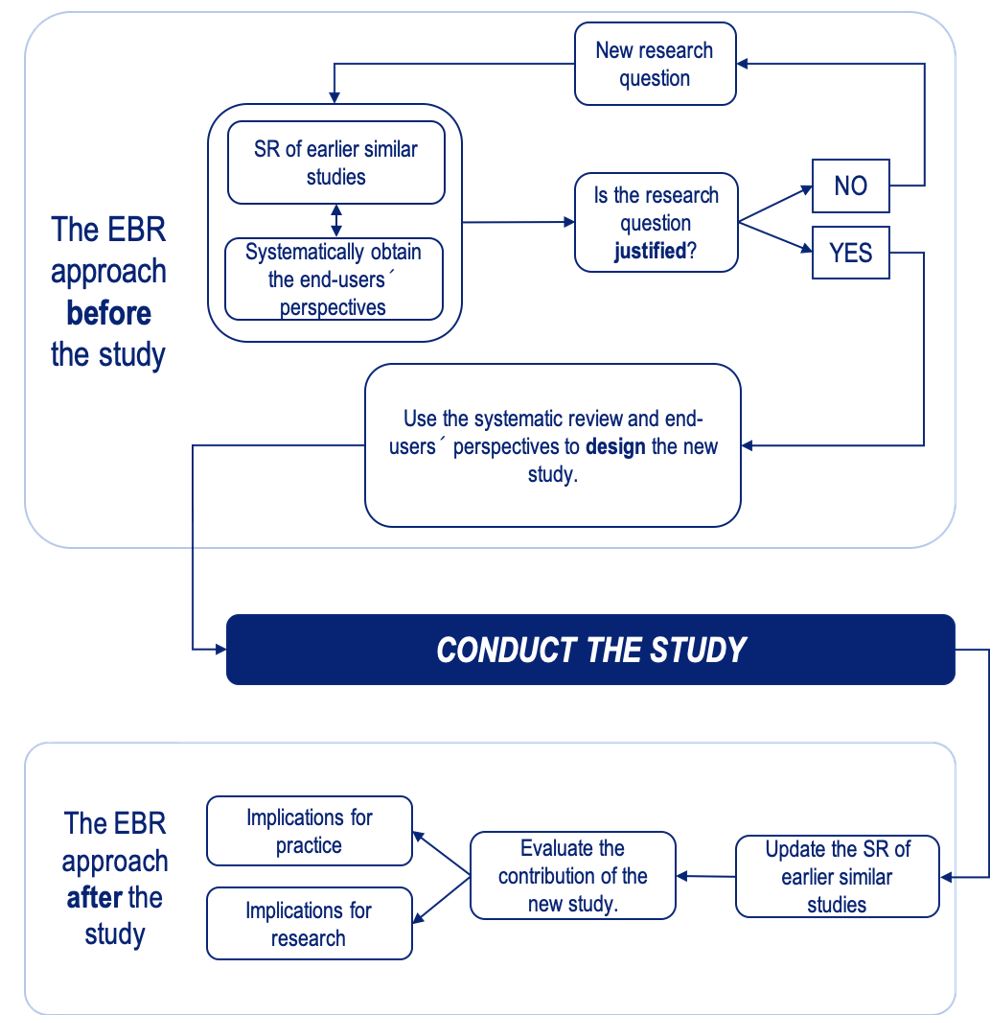
ロビンソンKAらより What Evidence-Based Research is and why is it important?
, J Clin Epi. 2020
EBR Mulitmedia Resources

。