Så længe der er substrat til rådighed til at binde sig til, vil en øget enzymkoncentration fremskynde den enzymatiske reaktion. Når alt substratet er bundet, vil reaktionen ikke længere blive fremskyndet med den stigende enzymkoncentration, da der ikke vil være noget for yderligere enzymer at binde sig til.
Hvordan virker enzymer?
Enzym er et katalytisk protein, som kan fremskynde den kemiske reaktion uden at blive ændret i reaktionsprocessen. I reaktionsprocessen dannes der ikke nogen binding mellem enzymet og substratet, så enzymet går tilbage til sin oprindelige form og kan bruges igen. Enzymet binder sig til substratet gennem det aktive sted for at danne et enzym-substratkompleks. De er meget specifikke i reaktionen og også i forhold til det substrat, de binder sig til. Når substratets form passer til enzymets aktive sted, er enzymets funktion korrekt, og deres funktion er afhængig af dets tredimensionelle struktur. De gør reaktionen lettere at finde sted ved at reducere aktiveringsenergien og aktivere flere molekyler og dermed udføre katalysatoren.
Effekt af enzymkoncentration
Enzymets koncentration er vigtig i en kemisk reaktion, da det er nødvendigt for at reagere med substratet. Ofte kan en lille mængde enzym forbruge en stor mængde substrat. Men med stigningen i enzymkoncentrationen øges også effektiviteten af de aktive steder, så disse aktive steder vil omdanne substratmolekylerne til produkter. Dette betyder grundlæggende, at hvis enzymkoncentrationen skal øges, skal der være et overskud af substrat, hvilket med andre ord betyder, at reaktionen skal være uafhængig af substratkoncentrationen.
Zero-order-reaktion
For at undersøge virkningen af en forøgelse af enzymkoncentrationen på reaktionshastigheden skal substratet være til stede i en overskydende mængde; dvs. reaktionen skal være uafhængig af substratkoncentrationen. Enhver ændring i mængden af produkt, der dannes i løbet af et bestemt tidsrum, vil være afhængig af den tilstedeværende enzymkoncentration. Grafisk kan dette fremstilles som:
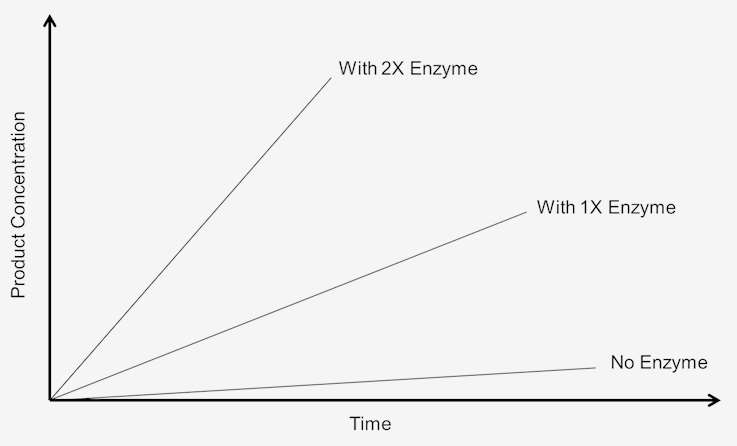 Figur 1. Reaktionshastighed i nul-orden er afhængig af substratkoncentrationen.
Figur 1. Reaktionshastighed i nul-orden er afhængig af substratkoncentrationen.
Disse reaktioner siges at være “nul-ordre-reaktioner”, fordi hastigheden er uafhængig af substratkoncentrationen. Produktdannelsen foregår med en hastighed, der er lineær med tiden. Tilsætning af mere substrat tjener ikke til at øge hastigheden. Ved nul-ordenskinetik resulterer det at lade assayet køre i dobbelt tid i dobbelt så meget produktmængde.
Mængden af enzym, der er til stede i en reaktion, måles ved den aktivitet, det katalyserer. Forholdet mellem aktivitet og koncentration påvirkes af mange faktorer som f.eks. temperatur, pH-værdi osv. Et enzymassay skal udformes således, at den observerede aktivitet er proportional med den tilstedeværende enzymmængde, således at enzymkoncentrationen er den eneste begrænsende faktor. Det er kun opfyldt, når reaktionen er nul-orden.
Relaterede tjenester
Enzymkinetik
Enzymologiassays
For at drøfte flere servicedetaljer bedes du kontakte os ved at ringe på 1-631-562-8517 eller sende os en e-mail på [email protected].