Amíg van szubsztrát, amelyhez kötődhet, az enzimkoncentráció növelése felgyorsítja az enzimatikus reakciót. Ha az összes szubsztrát megkötődött, a reakció már nem gyorsul fel az enzimkoncentráció növekedésével, mivel a további enzimeknek már nincs mihez kötődniük.
Hogyan működnek az enzimek?
Az enzim olyan katalitikus fehérje, amely képes felgyorsítani a kémiai reakciót anélkül, hogy a reakciófolyamat során megváltozna. A reakciófolyamat során az enzim és a szubsztrát között nem alakul ki kötés, így az enzim visszaalakul eredeti alakjába, és újra felhasználható. Az enzim az aktív központon keresztül kötődik a szubsztráthoz, így enzim-szubsztrát komplexet képez. Nagyon specifikusak a reakcióban és a szubsztrátra is, amelyhez kötődnek. Ha a szubsztrát alakja megegyezik az enzim aktív helyével, akkor az enzim működése megfelelő, és működésük a háromdimenziós szerkezetétől függ. Megkönnyítik a reakció lejátszódását azáltal, hogy csökkentik az aktiválási energiát, és több molekulát aktiválnak, így hajtják végre a katalizátort.
Az enzimkoncentráció hatása
A kémiai reakcióban fontos az enzim koncentrációja, mivel a szubsztráttal való reakcióhoz szükséges. Gyakran előfordul, hogy kis mennyiségű enzim nagy mennyiségű szubsztrátot képes elfogyasztani. Az enzimkoncentráció növekedésével azonban az aktív helyek hatékonysága is nő, így ezek az aktív helyek a szubsztrátmolekulákat termékké alakítják át. Ez alapvetően azt jelenti, hogy az enzim koncentrációjának növeléséhez szubsztrátfeleslegre van szükség, vagyis a reakciónak függetlennek kell lennie a szubsztrát koncentrációjától.
Zérórendű reakció
Az enzimkoncentráció növelésének a reakciósebességre gyakorolt hatásának vizsgálatához a szubsztrátnak felesleges mennyiségben kell jelen lennie, vagyis a reakciónak függetlennek kell lennie a szubsztrát koncentrációjától. A képződött termék mennyiségének változása egy meghatározott idő alatt a jelen lévő enzim mennyiségétől függ. Grafikusan ez a következőképpen ábrázolható:
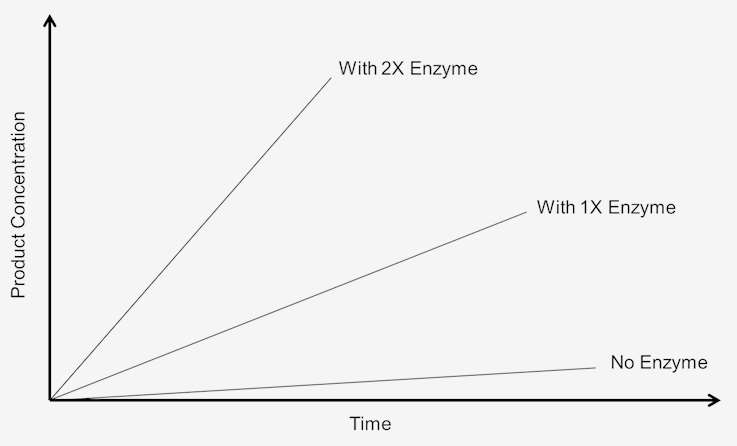 1. ábra. A null-rendű reakció sebessége függ a szubsztrátkoncentrációtól.
1. ábra. A null-rendű reakció sebessége függ a szubsztrátkoncentrációtól.
Ezeket a reakciókat “null-rendű reakcióknak” nevezzük, mivel a sebességek függetlenek a szubsztrátkoncentrációtól. A termékképződés olyan sebességgel megy végbe, amely lineárisan függ az időtől. Több szubsztrát hozzáadása nem szolgál a sebesség növelésére. Zérórendű kinetikában, ha a próbát kétszer annyi ideig hagyjuk futni, kétszer annyi termék keletkezik.
A reakcióban jelen lévő enzim mennyiségét az általa katalizált aktivitással mérjük. Az aktivitás és a koncentráció közötti kapcsolatot számos tényező befolyásolja, például a hőmérséklet, a pH stb. Egy enzimpróbát úgy kell megtervezni, hogy a megfigyelt aktivitás arányos legyen a jelen lévő enzim mennyiségével, hogy az enzimkoncentráció legyen az egyetlen limitáló tényező. Ez csak akkor teljesül, ha a reakció nulla rendű.
Kapcsolódó szolgáltatások
Enzimkinetika
Enzimológiai próbák
A szolgáltatás további részleteinek megbeszélése érdekében kérjük, vegye fel velünk a kapcsolatot az 1-631-562-8517-es telefonszámon, vagy írjon nekünk a [email protected] e-mail címre.