Michael D. Ober, MD
Christina M. Klais, MD
Emmett T. Cunningham Jr.さん。 MD, PhD, MPH
New York City
黄斑浮腫は、血液網膜障壁の破壊に対する非特異的反応として、主に叢状外層および内核層における網膜内の細胞外液の病的蓄積を表します。 MEは、糖尿病、網膜静脈閉塞症、ぶどう膜炎、眼科手術後の患者さんにおいて、視力低下の原因としてよく知られています。 網膜硝子体牽引、脈絡膜新生血管、その他多くの疾患では発生頻度は低くなります。 MEを管理するために多くの戦略が採用されているが、その成功は様々である。 この記事では、この一般的な症状に対する利用可能な治療法について概説します。
 |
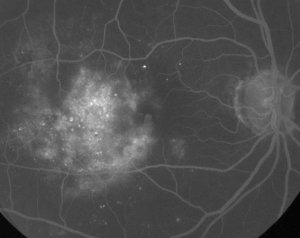 |
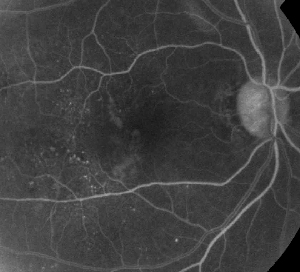
| 図1. A. 非増殖型糖尿病網膜症患者の初期段階のフルオレセイン血管造影。 微小動脈瘤は、窩洞の血管外層でのフルオレセイン漏出に加え、窩洞の側方に最も顕著に見られる。 | B. |
診断
MEの臨床診断は、コンタクトレンズと立体細隙灯眼底生物顕微鏡を用いて行うのが最も効果的である。 MEは通常、網膜内の不規則な隆起として現れ、しばしば網膜内脂質、微小動脈瘤、糖尿病、血管閉塞、または虚血に続発する場合の出血に隣接している。 網膜内液は、隣接する血管の異常の有無にかかわらず、眼窩傍網膜に限局した嚢胞状の空間に蓄積することもあります。 このような嚢胞性黄斑浮腫は、炎症、局所的な牽引、または手術後に生じることが最も一般的です。
フルオレセイン血管造影は、MEの診断に不可欠なツールである。 正常な眼では、フルオレセインは血液網膜関門によって網膜への通過が阻止される。 しかし、MEでは、フルオレセイン分子は血管内を出て網膜に入る。 患部は初期から中期にかけて過蛍光を示し、後期には面積と強度が増加します(図1参照)。 FAは浮腫を強調し、可視化と治療部位の特定を容易にするだけでなく、将来の比較のために恒久的な記録を作成することができる。 MEは4段階の定量的スケールが開発され、グレード0は眼窩周囲の過蛍光なし、グレード1は不完全な眼窩周囲の過蛍光、グレード2は軽度の360度過蛍光、グレード3は過蛍光部分が約1ディスク径の中程度の360度過蛍光、グレード4は過蛍光部分が約1.5ディスク径の重度の360度過蛍光である1,2。 FAはMEの存在を同定する感度の高い手段であるが、液の解剖学的分布(すなわち、びまん性か嚢胞性か網膜下か、および経時的な漏出の重症度)に関する情報は、比較的少ない。 FAは網膜肥厚に関する定量的な情報を提供しない。 したがって、この2次元のFAベースの等級付けシステムが全体として視力との相関が低いことは驚くべきことではない。3,4
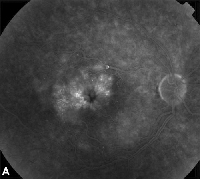
Optical Coherence Tomography (OCT III, Carl Zeiss) は非接触の非侵襲的イメージング技術で、MEの診断に役立つ補助手段を提供する。 近赤外光(830nm)を網膜表面に垂直に照射し、その反射の特性を解析する。 1.5秒で1本の線状の高解像度断面画像を作成します。 これらの画像は、浮腫部分に見られる肥厚した嚢胞状の網膜を表示し、さらに測定することができます。 また、網膜硝子体界面の特性を可視化するのにも有効で、硝子体牽引がMEの形成に関与している場合を効果的に示すことができます(図2参照)。
ある研究では、ぶどう膜炎に続発するMEの84眼をOCTで検査し、そのうちの41%と20%で、それぞれ網膜上膜と漿液性網膜剥離の存在を明らかにしたり確認したりすることができたという利点もある5。 この研究では、網膜の厚さと視力低下の間に中程度の相関があることがわかりましたが、相関の程度は研究によって異なり、他の研究者は糖尿病網膜症、ぶどう膜炎、CMEなどの多様な患者集団において、さまざまな統計手法を用いて弱い相関6、中程度7、強い相関8、9、10を報告しました。 A. 非増殖糖尿病網膜症と窩洞周辺に脂質の滲出を認める患者の左眼のカラー眼底写真。 B. 後期FAにより中心黄斑部に黄斑浮腫を認める。 C. 光干渉断層計は、黄斑浮腫と同様に異常な硝子体網膜界面を示す。
別のグループは、OCTがMEの検出においてFAと同等の効果を示し、液体の軸方向分布を記述する上でFAよりも優れていると報告している6。 OCTはまた、FAで最もよく可視化される種類の活動的な漏出が最小限または存在しない慢性CMEの特定の症例や、小惑星ヒアロシス患者のような中膜混濁の存在によって眼底検査が損なわれる場合のように、FAで可視化されないME患者を特定する能力を有する11
retinal thickness analyzer (RTA, Talia Technology, Israel) は同様の非接触イメージング技術で、網膜厚さの定量化が可能である。 これは、0.3秒かけて照射された緑色光(540nm)の斜め方向からの反射を解析し、3×3平方mmの網膜領域にわたって16の平行断面スキャンを生成するものである。 OCTとRTAはともに網膜厚の測定において優れた精度を示し、両技術を直接比較した結果、測定値には統計的に有意な相関があることが証明されています。 RTAは高速で取得でき、アーチファクトが少ないという利点があるが、中膜混濁がある場合にはOCTよりも網膜厚の測定に劣るようである12
別の研究では、30人の健康な眼でRTAとOCTによる窩洞厚を比較している。 健常眼の平均窩洞厚は,RTAで181μm,OCTで153μmと測定された。 一方、軽度の非増殖型糖尿病網膜症患者の解析では、糖尿病網膜症の初期段階における網膜肥厚領域の特定において、RTAはOCTよりも感度が高いことがわかった14
 |
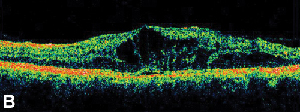 |
| 図3:糖尿病の初期段階における網膜肥厚領域の特定。 A.嚢胞性黄斑浮腫患者の後期フルオレセイン血管造影。 | B. |
治療 -医療
外用非ステロイド性抗炎症薬は白内障手術後のMEの最も一般的な治療である(図3参照)。 これらの薬剤は、MEの病因に関与しているとされる眼内プロスタグランジン濃度を低下させることを目的としている。 白内障手術を受けた患者を対象とした二重マスク無作為化有効プラセボ対照試験では、1%インドメタシン、0.03%フルルビプロフェン、0.5%ケトロラクおよび0.1%ジクロフェナク点眼液の局所適用による抗炎症効果が報告されている15、16が、この適応で食品医薬品局から特に承認されている唯一のNSAIDs局所適用はジクロフェナク 0.1% およびケトロラク 0.5% 眼科用剤である。 FDAの承認は得ていないが、術後のMEを予防するために、白内障手術前にNSAIDs外用薬を使用することが多い。
炎症性疾患および網膜色素変性症に続発するMEの治療では,特に局所NSAIDsおよびコルチコステロイドが効かない場合に,経口アセタゾラミドが使用されることがある。 様々な原因によるME患者を対象に,アセタゾラミドとプラセボを比較したマスク付きの前向きクロスオーバー試験がいくつか行われている。 41名の患者を対象とした5サイクルクロスオーバー試験では、遺伝性または炎症性網膜疾患を有する患者の半数以上で、MEの部分的または完全な消失として特徴づけられる再現性のある反応が認められたが、原発性網膜血管疾患を有する患者からは反応が得られなかった17。 この研究では、12人中10人に改善がみられた。
別のグループは、慢性虹彩毛細血管炎に起因するMEの55歳以下の患者は、高齢の患者よりもアセタゾラミド500mg2日投与に反応する傾向があると結論付けた。20
コルチコステロイドは強力な抗炎症薬で、MEの治療によく使用される。 血液網膜関門の安定化、炎症性メディエーターの抑制など、複数の作用機序がある。 投与方法には、局所投与、眼周囲注射、硝子体内注射、経口および静脈内投与がある。 コルチコステロイドの経口および静脈内投与は、確かに硝子体内で治療レベルに達しますが、患者を全身性合併症のリスクにさらすため、通常は全身性疾患があり、視力を脅かすぶどう膜炎の患者への投与に限定されています。 局所用コルチコステロイド点眼薬は、安全性の面でもう一方の端にありますが、後眼部に到達する能力は限られています。
最近では、糖尿病(図4参照)、網膜静脈閉塞症、炎症、その他の特発性に起因する難治性のMEを改善する強力な能力から、トリアムシノロンアセトニドの眼内注射(ケナログ、4.0 mg)の使用が増加しています23~26。 予備的な研究では、網膜肥厚の劇的な減少、フルオレセイン漏出の減少、視力の改善が見られ、患者によっては顕著な場合もあります。 効果は一時的で、通常3~6ヶ月以内しか持続しないが、MEは通常、再注入に反応する。 しかし、硝子体内コルチコステロイドの使用は、眼圧が持続的に上昇する30~40%のリスクと、手術を必要とする白内障の約10%のリスクと関連しています。 この研究では、網膜静脈閉塞症に起因する二次性ME患者を対象に、トリアムシノロン(1mgおよび4mg)の硝子体内注射と標準治療(観察および/または格子状レーザー治療)が比較されます。 本試験では、合計1,260人の患者を追跡調査し、36カ月間治療を継続します。
MEは、加齢黄斑変性症でも発生します(図5参照)。 現在、血管新生AMDの治療において、トリアムシノロンアセトニドの硝子体内注射を光線力学療法と併用することが検討されています(Visudyne with intravitreal Triamcinolone Acetonide, VisTA)。 ある研究では、黄斑浮腫とCNVを有する患者において、PDTの適用に先立ってTriamcinoloneを静脈内投与することの重要性が強調されている27 。著者らは、verteporfinが網膜内の嚢胞に漏れ、薬剤が光活性化すると隣の正常網膜の光受容体に障害を与える一方、網膜浮腫が事前に消失すればこの合併症を防止できると理論化している。
硝子体内注射自体、感染性眼内炎、網膜剥離、出血、眼圧上昇、白内障、低血圧など、重大かつ失明の恐れのある副作用のわずかではあるが確実なリスクと関連している28。最近発表された硝子体内注射のガイドラインでは、ますます使用されるようになったこの技術についてベストプラクティス的アプローチを確立しようというものである。 コンセンサス・パネルの勧告では、抗生物質、緑内障評価、手袋の使用、既存の眼瞼異常の治療を含む注射前の注意事項、また、手術前および手術中の過度の眼瞼操作を避けることの重要性が述べられています。 推奨される注入前後のレジメンは、局所および/または結膜下麻酔薬、局所ポビドンヨード、眼瞼鏡の使用などであった。 著者らは、視神経の灌流、トリアムシノロンの硝子体内位置、注入に関連した出血や網膜剥離がないことを確認するために、注入後に眼圧をモニターし、眼底を直接観察することの重要性を強調した。 また、潜在的な合併症の初期症状に対する患者教育や、徹底したフォローアップの重要性も強調した29。 A. 糖尿病黄斑浮腫の眼の光コヒーレンス・トモグラフィー画像と、それに対応するOCTによって生成された網膜厚マップB.。 C. 同じ患者の硝子体内トリアムシノロンアセトニド注射後1ヶ月のOCTとそれに対応する網膜厚さマップ。 D. 黄斑浮腫の消失。
いくつかの臨床試験では、眼内に使用する代替の長期的なコルチコステロイド投与デバイスが研究されています。 ある研究では、フルオシノロンアセトニドペレットをプラスチック支柱に埋め込んで外科的に設置し、3年間にわたりステロイドを制御して放出することが検討されています。 ボシュロム社とコントロール・デリバリー・システムズ社のEnvision眼内インプラントとして知られるこの製品は、眼窩から挿入され、強膜に縫合されます。 第II/III相ランダム化マスク試験において,フルオシノロンアセトニド0.5mgと2.0mgを比較する群と,レーザー光凝固または観察からなる標準治療群に無作為に割り付けた80人の患者を対象に,Envision TD implantを比較検討したところ,0.5mgと2.0mgを比較する群の方が,より高い効果が得られた。 6ヵ月後、0.5mgインプラントは標準治療と比較して、糖尿病網膜症の発症率および重症度を統計的に有意に減少させたことが確認されました。 また、重篤な有害事象の発生率にも差はありませんでした。 なお、2.0mg群については、2回目の試験で0.5mg群に対する優位性が認められなかったため、早期に試験を中止しています。 2番目の試験では、非感染性後部ぶどう膜炎患者278名が、患眼または両眼の場合はより重症の患眼にレティサート0.59mgまたは2.1mgを移植されるよう無作為に割り付けられました。 2回の投与と34週間の経過後、レティサートを埋め込んだ眼では再発率が有意に低く(10 vs 55.7%、p<0.0001)、全身コルチコステロイド/免疫抑制療法の使用も減少(ベースラインで59.0%、34週間で13.7%)、テノン下ステロイドや外用ステロイドの使用も減少していました。 視力には有意な改善がみられました(p<0.05)。 最も一般的な有害事象は白内障の進行と眼圧の上昇で、8.6%にフィルタリングの処置が必要とされました。 (Jaffe G. Invest Ophthalmol Vis Sci. 2004; 44 ARVO E-Abstract #3369)
もう一つの試験は、アラガンのPosurdex、硝子体腔に注入され50日から160日かけて薬が放出される生体吸収性のデキサメタゾンペレットに関係するものです。 第II相試験の結果、350μgと700μgのペレットは、プラセボと比較して、180日時点で2線以上の視力改善率(350μg:27.2%、700μg:35.7%)、3線以上の視力改善率(350μg:13%、700μg:19.4%)がともに有意に改善されることが明らかになりました。
治療法 -レーザー
最近では、アイテックとファイザーのMacugenが、糖尿病性ME患者172人を対象とした無作為化、ダブルマスク、多施設、用量設定、対照第II相試験で研究されています。 この試験では、3つの用量(0.3mg、1.0mg、3.0mg)を6週間ごとに3回注射する偽注射と比較検討しました。 本試験では、焦点・グリッドレーザーの照射を12週間以上延期しても差し支えないと思われる患者さんのみを登録するように指示されました。 18週目から30週目までは、治験責任医師の判断で追加注射や光凝固術が行われた。 最終評価は、計画された最後の注射の6週間後である36週目に行われた。 全体として、Macugenを投与された被験者では、偽薬の患者さんと比較して、視力が向上し、網膜中心部の厚みが減少し、追加のレーザー治療が必要になる可能性が低くなりました31。 EDTRSでは,焦点式レーザー光凝固術の適応となる患者を臨床的に有意なMEを有する患者と同定した。 これは、以下の3つの基準のうち1つを満たすものと定義された。 1)窩洞から500μm以内の網膜肥厚、2)窩洞から500μm以内の硬い滲出物で、隣接する網膜肥厚を伴う、3)ディスク径1以上の浮腫領域で、窩洞からディスク径1未満の部分にある、3つの基準のいずれかを満たすものと定義した。 しかし、EDTRSは、微小動脈瘤に隣接する網膜の局所的な肥厚に相当するfocal MEと、後極の全体的な肥厚を指すdiffuse MEを区別していない。 糖尿病性MEは局所的なレーザーがよく効くのに対し、びまん性MEはレーザー治療が効かないことが多く、別の治療が必要であることが報告されている
 |
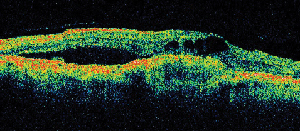 |
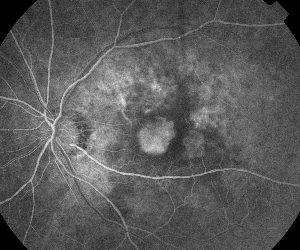
| 図5. A. 初期のフルオレセイン血管造影で、古典的な窩洞下新生血管を示す。 | B. 光干渉断層撮影では、網膜下および網膜内液の貯留領域と新生血管が確認できる(矢印)。 このことは、その後OCTで確認され、この術式の適応が改良された。低侵襲的治療に反応しない糖尿病性MEに対して硝子体手術を受けた患者の3大シリーズ35、36、37は、それぞれ59、58、65人の患者を分析した。 これらのシリーズでは、患者の47%、53%、45%がそれぞれ2線以上の視力改善を示したと報告している。 最後のグループは、網膜剥離(1.5%)、虹彩ルベオーシス(4.6%)、網膜上膜(13.8%)、再発硝子体出血(1.5%)、眼窩硬性滲出物(4.6%)などの術後重篤合併症を少数例で報告し、第2のグループは網膜上膜10.2%、フェイキックアイ63.2%に白内障などの合併症を明らかにしました。 他のいくつかのケースシリーズでも同様の結果が示されていますが、いずれも非ランダム化、プラセボ対照なし、異なる対象・除外基準を用いています。 さらに、手術方法も異なっており、CME患者における硝子体手術の正確な適応は解釈の余地がある。
CMEは、さまざまな治療法があるにもかかわらず、依然として視力低下の主な原因である。 レーザー光凝固は、糖尿病、虚血、血管閉塞によるMEの管理に不可欠な部分であることに変わりはない。 術後のMEをコントロールする方法としては、現在、NSAIDsとコルチコステロイドの外用が主であり、ブドウ膜炎や網膜色素変性症に続発するMEの一部の患者では、アセタゾラミドが依然として有効な治療手段である。 ME治療における硝子体内コルチコステロイドの役割は拡大しているが、副作用と効果の持続時間にはまだ限界がある。 また、薬物療法と眼内投与法の進歩は、すべての原因およびタイプのMEの予防と管理に役割を果たすことが期待されています。 オバー博士は、コロンビア大学医科外科のエドワード・S・ハークネス眼科研究所およびマンハッタン眼・耳・咽喉病院のLuEsther T. Mertz網膜研究センターで網膜硝子体手術の研究員として勤務しています。 連絡先: 210 East 64th St., 8th Fl, New York, NY 10021; e-mail: [email protected]; or (212) 605 3777 or fax (212) 605 3795. Klais 博士は LuEsther T. Mertz Retinal Research Center で Retina fellow として勤務しています。 連絡先は同住所、電話番号、ファックス番号、または電子メール([email protected]. Cunningham博士はニューヨーク大学医学部の眼科臨床教授で、ぶどう膜炎サービスのディレクターを務めています。 連絡先は Vitreous-Retina-Macula Consultants of New York, 460 Park Ave., New York, N.Y. 10022, e-mail [email protected], or phone/fax at (212) 861 9797. 1.Cunningham博士はニューヨーク大学医学部の眼科臨床教授であり、ぶどう膜炎サービスの責任者でもある。 Spaide RF, Yannuzzi LA, Sisco LJ. 慢性嚢胞性黄斑浮腫と視力の予測因子。 Ophthalmic Surg 1993;24:262-267. 2. Yannuzzi LA. 無水晶体嚢胞性黄斑浮腫の治療についての見解。 Surv Ophthalmol 1984;28:540-553 3. Chang A, Spaide RF, Yannuzzi LA.(チャン・エイ、スパイド・リーフ、ヤヌッツィ・ロー)。 術後の嚢胞性黄斑浮腫。 で。 において:Guyer DR, Yannuzzi LA, Chang S, et al.網膜、硝子体、黄斑部。 Saunders。 フィラデルフィア。 Nussenblatt RB, Kaufman SC, Palestine AG, et al.黄斑部肥厚と視力。 嚢胞性黄斑浮腫の患者における測定。 Ophthalmology 1987;94:1134-9. 5. このような場合、「虹彩炎患者における黄斑浮腫のパターン:光干渉断層計を用いた定性的および定量的評価」(邦訳『虹彩炎患者における黄斑浮腫のパターン:光干渉断層計を用いた定性的および定量的評価』、日本経済新聞出版社、2005年)。 Ophthalmology 2004;111:946-53. 6. Antcliff RJ, Stanford MR, Chauhan DS, et al. 光コヒーレンス・トモグラフィーと眼底フルオレセイン・アンギオグラフィーによるブドウ膜炎患者の嚢胞状黄斑浮腫検出の比較. 大谷 毅, 岸 晋, 丸山 泰史: 光干渉断層計による糖尿病性黄斑浮腫のパターン.日本眼科医学会雑誌, Vol.1, pp. 大谷敏彦、岸信介、丸山泰隆、光干渉断層計による糖尿病黄斑浮腫のパターン. 8. Hee MR, Puliafito CA, Wong C, et al. 光コヒーレンス・トモグラフィーを用いた黄斑浮腫の定量的評価。 Arch Ophthalmol 1995;113:1019-29. 9. Nussenblatt RB, Kaufman SC, Palestine AG, et al.黄斑部肥厚と視力. 嚢胞性黄斑浮腫の患者における測定。 眼科 1987;94:1134-9. 10. また、このような場合にも、「虹彩の光干渉断層計」を用いて、黄斑浮腫を評価することができる。 Ophthalmologica 2005;219:86-92. 11. Browning DJ, Fraser CM. 光コヒーレンス・トモグラフィーによるアステロイド・ヒアロースの存在下での黄斑浮腫の検出。 Am J Ophthalmol 2004;137:959-961. 12. Polito A, Shah SM, Haller JA et al. 黄斑疾患眼の眼窩厚評価における網膜厚測定器と光コヒーレンス・トモグラフィーの比較.Polito A, Shah SM, Haller JA et al. Am J Ophthalmol 2002;134:240-51。 13. Neubauer AS, Priglinger S, Ullrich S, et al. 網膜厚測定器と光コヒーレンス・トモグラフィで測定した眼窩厚の比較. Retina 2001;21:596-601. 14. Pires I、Bernardes RC、Lobo CL、Soares MA、Cunha-Vaz JG. 2型糖尿病患者における軽度非増殖性網膜症眼の網膜厚:網膜厚解析と光干渉断層計による測定値の比較。 Arch Ophthalmol 2002 Oct;120(10):1301-6. 15. Flach AJ. 眼科領域におけるシクロオキシゲナーゼ阻害剤. 眼科におけるシクロオキシゲナーゼ阻害剤。 Heier JS, Topping TM, Baumann W, Dirks MS, Chern S. Ketorolac versus prednisolone versus combination therapy in the treatment of acute pseudophakic cystoid macular edema. Ophthalmology 2000;107:2034-8. 17. Cox SN, Hay E, Bird AC. アセタゾラミドによる慢性黄斑浮腫の治療。 Arch Ophthalmol 1988;106:1190-5. 18. Fishman GA, Gilbert LD, Fiscella RG, Kimura AE, Jampol LM. 網膜色素変性症における慢性黄斑浮腫の治療におけるアセタゾラミド. Arch Ophthalmol 1989;107:1445-52. 19. Farber MD, Lam S, Tessler HH, Jennings TJ, Cross A, Rusin MM. 虹彩毛細血管炎の患者におけるアセタゾラミドによる黄斑浮腫の軽減:無作為化プロスペクティブクロスオーバー試験。 虹彩毛細血管炎の患者におけるアセタゾラミドによる黄斑浮腫の軽減:無作為前向きクロスオーバー試験」(Br J Ophthalmol 1994;78:4-7. 20. Giusti C, Forte R, Vingolo EM, Gargiulo P. Acetazolamide is effective in the treatment of diabetic macular edema? パイロットスタディ Int Ophthalmol 2001;24:79-88. 21. Jennings T、Rusin MM、Tessler HH、Cunha-Vaz JG. 嚢胞性黄斑浮腫を有するぶどう膜炎患者における副腎皮質ステロイドのテノン後方下注射。 Jpn J Ophthalmol 1988;32:385-91. 22. Helm CJ, Holland GN. 中間ぶどう膜炎患者におけるトリアムシノロンアセトニドの後方テノン下注入の効果。 Am J Ophthalmol 1995;120:55-64. 23. このような場合、「膀胱炎」、「眼精疲労」、「眼底出血」、「眼窩内出血」、「黄斑浮腫」などが考えられます。 Am J Ophthalmol 2003;135:246-9. 24. Jonas JB, Kreissig I, Degenring RF. 網膜中心静脈閉塞症における黄斑浮腫の治療としてのトリアムシノロンアセトニドの硝子体内投与。 Graefes Arch Clin Exp Ophthalmol. 2002;240:782-3. 25. 25. このような場合、「痒み」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」の4つの方法があります。 Ophthalmology 2002; 109: 920-7. 26. 26. スコット IU、フリン HW Jr.、ローゼンフェルド PJ. 特発性嚢胞性黄斑浮腫に対するトリアムシノロンアセトニドの硝子体内投与。 Am J Ophthalmol 2003;136:737-9. 27. 27. このような場合、「痒み」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」、「痒み止め」の5つの方法があります。 Arch Ophthalmol, In Press. 28. 28. Jager RD, Aiello LP, Patel SC, Cunningham ET Jr. 硝子体内注射のリスク:包括的レビュー。 網膜。 2004 Oct;24(5):676-98. 29. 29. 29. Aiello LP, Brucker AJ, Chang S, et al. Evolving guidelines for intravitreal injections(硝子体内注射の進化するガイドライン). Retina 2004 Oct;24(5 Suppl):S3-19. 30. .G.Jaffe, Fluocinolone Acetonide Uveitis Study Group. 後眼部に影響を及ぼすぶどう膜炎に対するフルオシノロンアセトニド硝子体内注入。 ARVO 2004, poster #3369. 31. マキュジェン糖尿病網膜症研究会。 糖尿病黄斑浮腫に対する抗血管内皮増殖因子アプタマーであるpegaptanibの第II相ランダム化二重マスク試験。 Ophthalmology, In press. 32. 30. 糖尿病黄斑浮腫に対する光凝固療法。 早期治療糖尿病網膜症研究報告書第1号。 Arch Ophthalmol 1985;103:1796-806. 33. Christoforidis JB, D’Amico DJ. 糖尿病黄斑浮腫の外科的治療とその他の治療:最新情報。 Int Ophthalmol Clin 2004;44:139-60. 34. ルイスH、エイブラムスGW、ブルメンクランツMS、カンポRV。 糖尿病黄斑部牽引と後部ヒアルロン酸牽引に伴う浮腫に対する硝子体手術。 Ophthalmology 1992;99:753-9. 35. Kaiser PK, Riemann CD, Sears JE, Lewis H. Macular traction detachment and diabetic macular edema associated with posterior hyaloidal traction(後部ヒアロイドトラクションに伴う黄斑牽引剥離と糖尿病性黄斑浮腫). Am J Ophthalmol 2001;131:44-9. 36. Lewis H. The role of vitrectomy in the treatment of diabetic macular edema. Am J Ophthalmol 2001;131:123-5. 37. Pendergast SD. 張った黄斑前膜後ヒアルロン酸を伴う糖尿病性黄斑浮腫に対する硝子体手術。 Curr Opin Ophthalmol 1998;9:71-5. 38. 糖尿病網膜症例におけるびまん性黄斑浮腫に対する硝子体手術. Am J Ophthalmol 1996;122:258-60. 39. 糖尿病黄斑浮腫に対する硝子体手術後の術後早期網膜厚変化と合併症の検討. Am J Ophthalmol 2003;135:14-9. . |