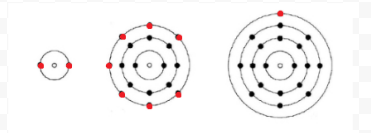
Lewis gebruikte eenvoudige diagrammen (nu Lewis-diagrammen genoemd) om bij te houden hoeveel elektronen aanwezig waren in de buitenste, of valentieschil, van een bepaald atoom. De kern van het atoom, d.w.z. de kern samen met de binnenste elektronen, wordt weergegeven door het chemische symbool, en alleen de valentie-elektronen worden getekend als stippen rond het chemische symbool. Zo kunnen de drie atomen uit figuur 1 van Elektronen en valentie worden voorgesteld met de volgende Lewisdiagrammen:

Als het atoom een edelgasatoom is, zijn er twee alternatieve procedures mogelijk. Ofwel beschouwen we het atoom als een atoom met nul valentie-elektronen, ofwel beschouwen we de buitenste gevulde schil als de valentieschil. De eerste drie edelgassen kunnen dus worden geschreven als:
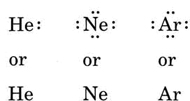
Voorbeeld (\PageIndex{1}\): Lewisstructuren
Teken Lewisdiagrammen voor een atoom van elk van de volgende elementen: Li, N, F, Na
Oplossing
Uit het periodiek systeem aan de binnenkant van de omslag kunnen we afleiden dat Li een atoomnummer heeft van 3. Het bevat dus drie elektronen, één meer dan het edelgas He. Dit betekent dat de buitenste schil slechts één elektron bevat en het Lewis-diagram is
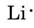
Volgens dezelfde redenering heeft N zeven elektronen, vijf meer dan He, terwijl F negen elektronen heeft, zeven meer dan He. Dit geeft
![]()
Na heeft negen elektronen meer dan He, maar acht daarvan bevinden zich in de kern, die overeenkomt met de acht elektronen in de buitenste schil van Ne. Aangezien Na slechts 1 elektron meer heeft dan Ne, is zijn Lewisdiagram
![]()
Merk uit het voorgaande voorbeeld op dat de Lewisdiagrammen van de alkalimetalen identiek zijn op hun chemische symbolen na. Dit komt mooi overeen met het zeer vergelijkbare chemische gedrag van de alkalimetalen. Op dezelfde manier zien Lewisdiagrammen voor alle elementen in andere groepen, zoals de aardalkalimetalen of halogenen, er hetzelfde uit.
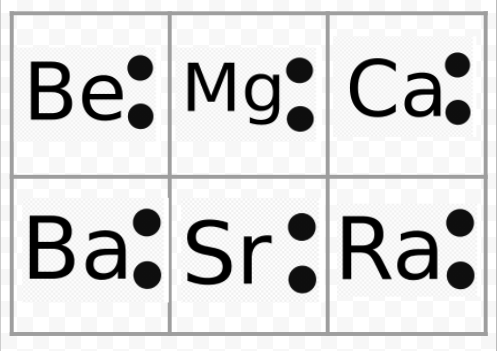
De Lewis-diagrammen kunnen ook worden gebruikt om de valenties van de elementen te voorspellen. Lewis stelde voor dat het aantal valenties van een atoom gelijk was aan het aantal elektronen in zijn valentieschil of aan het aantal elektronen dat aan de valentieschil zou moeten worden toegevoegd om de elektronische schilstructuur van het volgende edelgas te bereiken. Als voorbeeld van dit idee kunnen we de elementen Be en O nemen. Hun Lewisdiagrammen en die van de edelgassen He en Ne zijn

Vergelijkt men Be met He, dan ziet men dat eerstgenoemd element twee elektronen meer heeft en dus een valentie van 2 zou moeten hebben. Van het element O zou men een valentie van 6 of een valentie van 2 kunnen verwachten, aangezien het zes valentie-elektronen heeft – twee minder dan Ne. Met behulp van de valentie-regels die op deze manier zijn ontwikkeld, was Lewis in staat om de regelmatige toename en afname van de subscripts van de verbindingen te verklaren in de tabel die in het valentiegedeelte staat, en hier is weergegeven. Bovendien was hij in staat om meer dan 50% van de formules in de tabel te verklaren. (De formules die met zijn ideeën overeenkomen zijn in de tabel in kleur gearceerd. Misschien wilt u die tabel nu raadplegen en controleren of sommige van de aangegeven formules de regels van Lewis volgen). Lewis’ succes in dit verband gaf een duidelijke aanwijzing dat elektronen de belangrijkste factor waren in het bij elkaar houden van atomen bij de vorming van moleculen.
Ondanks deze successen zijn er ook moeilijkheden te vinden in Lewis’ theorieën, in het bijzonder voor elementen voorbij calcium in het periodiek systeem. Het element Br (Z = 35), bijvoorbeeld, heeft 17 elektronen meer dan het edelgas Ar (Z = 18). Dit leidt tot de conclusie dat Br 17 valentie-elektronen heeft, wat het lastig maakt te verklaren waarom Br zo sterk lijkt op Cl en F, hoewel deze twee atomen slechts zeven valentie-elektronen hebben.
| Element | Atomair Gewicht | Waterstof Verbindingen | Zuurstofverbindingen | Chloorverbindingen |
|---|---|---|---|---|
| Waterstof | 1.01 | H2 | H2O, H2O2 | HCl |
| Helium | 4.00 | Niet gevormd | Niet gevormd | Niet gevormd |
| Lithium | 6.94 | LiH | Li2O, Li2O2 | LiCl |
| Beryllium | 9.01 | BeH2 | BeO | BeCl2 |
| Boron | 10.81 | B2H6 | B2O3 | BCl3 |
| Carbon | 12.01 | CH4, C2H6, C3H8 | CO2, CO, C2O3 | CCl4, C2Cl6 |
| Stikstof | 14.01 | NH3, N2H4, HN3 | N2O, NO, NO2, N2O5 | NCl3 |
| Zuurstof | 16.00 | H2O, H2O2 | O2, O3 | <Cl2O, ClO2, Cl2O7 |
| Fluorine | 19.00 | HF | OF2, O2F2 | ClF, ClF3, ClF5 |
| Neon | 20.18 | Niet gevormd | Niet gevormd | Niet gevormd |
| Natrium | 22.99 | NaH | Na2O, Na2O2 | NaCl |
| Magnesium | 24.31 | MgH2 | MgO | MgCl2 |
| Aluminium | 26.98 | AlH3 | Al2O3 | AlCl3 |
| Silicon | 28.09 | SiH4, Si2H6 | SiO2 | SiCl4, Si2Cl6 |
| Fosfor | 30.97 | PH3, P2H4 | P4O10, P4O6 | PCl3, PCl5, P2Cl4 |
| Zwavel | 32.06 | H2S, H2S2 | SO2, SO3 | S2Cl2, SCl2, SCl4 |
| Chloor | 35.45 | HCl | Cl2O, ClO2, Cl2O7 | Cl2 |
| Potassium | 39.10 | KH | K2, K2O2, KO2 | KCl |
| Argon | 39.95 | Niet gevormd | Niet gevormd | Niet gevormd |
| Calcium | 40.08 | CaH2 | CaO, CaO2 | CaCl2 |
| Scandium | 44.96 | Relatief Onstabiel | Sc2O3 | ScCl3 |
| Titanium | 47.90 | TiH2 | TiO2, Ti2O3, TiO | TiCl4, TiCl3, TiCl2 |
| Vanadium | 50.94 | VH2 | V2O5, V2O3, VO2, VO | VCl4, VCl3, VCl2 |
| Chromium | 52.00 | CrH2 | Cr2O3, CrO2, CrO3 | CrCl3, CrCl2 |
Bijdragers
-
Ed Vitz (Kutztown University), John W. Moore (UW-Madison), Justin Shorb (Hope College), Xavier Prat-Resina (University of Minnesota Rochester), Tim Wendorff, en Adam Hahn.