Atâta timp cât există substrat disponibil de care să se lege, creșterea concentrației enzimei va accelera reacția enzimatică. Odată ce tot substratul este legat, reacția nu va mai accelera odată cu creșterea concentrației enzimei, deoarece nu va mai exista nimic de care să se lege alte enzime.
Cum funcționează enzimele?
Enzima este o proteină catalitică care poate accelera reacția chimică fără a fi alterată în procesul de reacție. În procesul de reacție, nu se formează nicio legătură între enzimă și substrat, astfel încât enzima revine la forma sa inițială și poate fi utilizată din nou. Enzima se leagă de substrat prin intermediul situsului activ pentru a forma un complex enzimă-substrat. Acestea sunt foarte specifice în ceea ce privește reacția și, de asemenea, substratul cu care se leagă. Atunci când forma substratului se potrivește cu situsul activ al enzimei, funcția enzimei este corectă, iar funcționarea lor depinde de structura sa tridimensională. Ele facilitează producerea reacției prin reducerea energiei de activare și activarea mai multor molecule, realizând astfel catalizatorul.
Efectul concentrației enzimei
Concentrația enzimei este importantă în reacția chimică, deoarece este necesară pentru a reacționa cu substratul. Adesea, o cantitate mică de enzimă poate consuma o cantitate mare de substrat. Cu toate acestea, odată cu creșterea concentrației enzimei, crește și eficiența situsurilor active, astfel încât aceste situsuri active vor transforma moleculele de substrat în produse. Acest lucru înseamnă, în esență, că dacă se dorește creșterea concentrației enzimei, trebuie să existe un exces de substrat, cu alte cuvinte, ceea ce înseamnă că reacția trebuie să fie independentă de concentrația substratului.
Reacția de ordin zero
Pentru a studia efectul creșterii concentrației enzimei asupra vitezei de reacție, substratul trebuie să fie prezent într-o cantitate excesivă; adică, reacția trebuie să fie independentă de concentrația substratului. Orice modificare a cantității de produs format pe o anumită perioadă de timp va depinde de nivelul de enzimă prezentă. Din punct de vedere grafic, acest lucru poate fi reprezentat astfel:
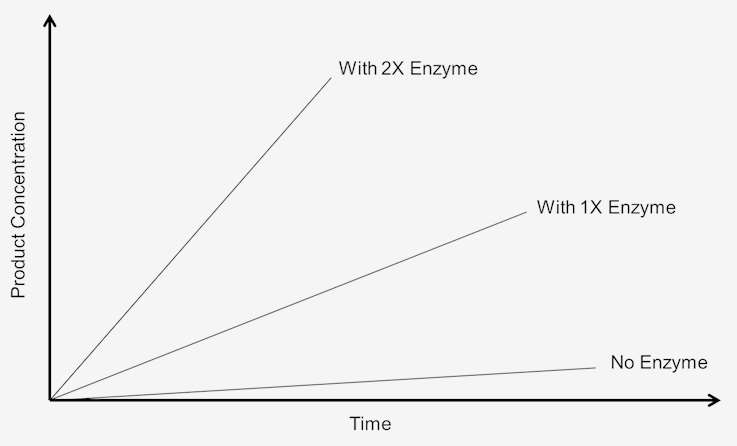 Figura 1. Figura 1. Viteza reacției de ordin zero depinde de concentrația substratului.
Figura 1. Figura 1. Viteza reacției de ordin zero depinde de concentrația substratului.
Aceste reacții sunt numite „reacții de ordin zero” deoarece vitezele sunt independente de concentrația substratului. Formarea produsului are loc cu o viteză care este liniară cu timpul. Adăugarea de mai mult substrat nu servește la creșterea vitezei. În cazul cineticii de ordin zero, dacă se permite ca analiza să se desfășoare timp dublu, se obține o cantitate dublă de produs.
Cantitatea de enzimă prezentă într-o reacție se măsoară prin activitatea pe care o catalizează. Relația dintre activitate și concentrație este afectată de mulți factori, cum ar fi temperatura, pH-ul etc. Un test enzimatic trebuie conceput astfel încât activitatea observată să fie proporțională cu cantitatea de enzimă prezentă pentru ca concentrația enzimei să fie singurul factor limitativ. Aceasta este satisfăcută doar atunci când reacția este de ordin zero.
Servicii conexe
Cinetică enzimatică
Sesizări enzimologice
Pentru a discuta mai multe detalii despre servicii, vă rugăm să ne contactați la numărul de telefon 1-631-562-8517, sau să ne trimiteți un e-mail la [email protected].
.