Rena ämnen och blandningar
En ren kemisk substans är en materia som har en fast kemisk sammansättning och karakteristiska egenskaper. Syre är till exempel ett rent kemiskt ämne som är en färglös, luktfri gas vid 25 °C. Mycket få prover av materia består av rena ämnen; i stället är de flesta blandningar, som är kombinationer av två eller flera rena ämnen i varierande proportioner där de enskilda ämnena behåller sin identitet. Luft, kranvatten, mjölk, blåmögelost, bröd och smuts är alla blandningar. Om alla delar av ett material är i samma tillstånd, inte har några synliga gränser och är enhetliga överallt, är materialet homogent. Exempel på homogena blandningar är luften vi andas och kranvattnet vi dricker. Homogena blandningar kallas också lösningar. Luft är således en lösning av kväve, syre, vattenånga, koldioxid och flera andra gaser; kranvatten är en lösning av små mängder av flera ämnen i vatten. Den specifika sammansättningen av båda dessa lösningar är dock inte bestämd utan beror både på källan och platsen; till exempel är sammansättningen av kranvatten i Boise, Idaho, inte densamma som sammansättningen av kranvatten i Buffalo, New York. Även om de flesta lösningar som vi möter är flytande kan lösningar också vara fasta. Den grå substans som fortfarande används av vissa tandläkare för att fylla hål i tänderna är en komplex fast lösning som innehåller 50 % kvicksilver och 50 % av ett pulver som huvudsakligen innehåller silver, tenn och koppar, med små mängder zink och kvicksilver. Fasta lösningar av två eller flera metaller kallas vanligen för legeringar.
Om sammansättningen av ett material inte är helt enhetlig är det heterogent (t.ex. chokladkaksdeg, blåmögelost och smuts). Blandningar som verkar vara homogena visar sig ofta vara heterogena efter en mikroskopisk undersökning. Mjölk verkar till exempel vara homogen, men när den undersöks i mikroskop är det tydligt att den består av små fett- och proteinkulor som är utspridda i vatten. Komponenterna i heterogena blandningar kan vanligtvis separeras med enkla medel. Blandningar av fasta och flytande ämnen, t.ex. sand i vatten eller teblad i te, kan lätt separeras genom filtrering, vilket innebär att blandningen passerar genom en barriär, t.ex. en sil, med hål eller porer som är mindre än de fasta partiklarna. I princip kan blandningar av två eller flera fasta ämnen, t.ex. socker och salt, separeras genom mikroskopisk inspektion och sortering. Mer komplicerade operationer är dock vanligtvis nödvändiga, t.ex. när man separerar guldklimpar från flodgrus genom panorering. Först filtreras fast material från flodvattnet och sedan separeras de fasta ämnena genom inspektion. Om guldet är inbäddat i berg kan det behöva isoleras med hjälp av kemiska metoder.
-and-Milk-(left).jpg?revision=1)
Figur 1.2.2: En heterogen blandning. I mikroskop är helmjölk i själva verket en heterogen blandning som består av klumpar av fett och protein som är utspridda i vatten. Figur används med tillstånd från Wikipedia
Homogena blandningar (lösningar) kan separeras till sina ingående ämnen genom fysiska processer som bygger på skillnader i någon fysikalisk egenskap, t.ex. skillnader i kokpunkt. Två av dessa separationsmetoder är destillation och kristallisering. Destillation utnyttjar skillnader i flyktighet, ett mått på hur lätt ett ämne omvandlas till gas vid en viss temperatur. En enkel destillationsapparat för att separera en blandning av ämnen, varav minst ett är en vätska. Den mest flyktiga komponenten kokar först och kondenseras tillbaka till en vätska i den vattenkylda kondensorn, varifrån den flödar in i den mottagande kolven. Om till exempel en lösning av salt och vatten destilleras samlas den mer flyktiga komponenten, rent vatten, i mottagarkolven, medan saltet stannar kvar i destillationskolven.

Figur 1.2.3: Destillation av en lösning av bordssalt i vatten. Lösningen av salt i vatten värms upp i destillationskolven tills den kokar. Den resulterande ångan är berikad på den mer flyktiga komponenten (vatten), som kondenserar till en vätska i den kalla kondensorn och sedan samlas upp i mottagarkolven.
Blandningar av två eller flera vätskor med olika kokpunkter kan separeras med en mer komplicerad destillationsapparat. Ett exempel är raffinering av råolja till en rad användbara produkter: flygbränsle, bensin, fotogen, dieselbränsle och smörjolja (i ungefärlig ordning med minskande flyktighet). Ett annat exempel är destillation av alkoholhaltiga spritdrycker som konjak eller whisky. Detta relativt enkla förfarande orsakade mer än en del huvudvärk för de federala myndigheterna på 1920-talet under förbudstiden, när illegala destillerier spreds i avlägsna områden i USA.
Kristallisation separerar blandningar baserat på skillnader i löslighet, ett mått på hur mycket fast substans som förblir löst i en given mängd av en specificerad vätska. De flesta ämnen är mer lösliga vid högre temperaturer, så en blandning av två eller flera ämnen kan lösas upp vid en förhöjd temperatur och sedan sakta svalna. Alternativt kan man låta vätskan, som kallas lösningsmedlet, avdunsta. I båda fallen bildar det minst lösliga av de upplösta ämnena, det som är minst sannolikt att förbli i lösning, vanligtvis kristaller först, och dessa kristaller kan avlägsnas från den återstående lösningen genom filtrering.

Figur 1.2.4: Kristallisation av natriumacetat från en koncentrerad lösning av natriumacetat i vatten. Tillsatsen av en liten ”frökristall” (a) leder till att föreningen bildar vita kristaller som växer och så småningom upptar större delen av kolven. Videon finns här: https://www.youtube.com/watch?v=BLq5NibwV5g
De flesta blandningar kan separeras i rena ämnen, som kan vara antingen grundämnen eller föreningar. Ett grundämne, t.ex. grått, metalliskt natrium, är ett ämne som inte kan delas upp i enklare ämnen genom kemiska förändringar; en förening, t.ex. vit, kristallin natriumklorid, innehåller två eller flera grundämnen och har kemiska och fysikaliska egenskaper som vanligen skiljer sig från egenskaperna hos de grundämnen som den består av. Med bara några få undantag har en viss förening samma grundämnessammansättning (samma grundämnen i samma proportioner) oberoende av dess ursprung eller historia. Ett ämnes kemiska sammansättning förändras i en process som kallas kemisk förändring. Omvandlingen av två eller flera grundämnen, t.ex. natrium och klor, till en kemisk förening, natriumklorid, är ett exempel på en kemisk förändring, ofta kallad en kemisk reaktion. För närvarande är cirka 115 grundämnen kända, men miljontals kemiska föreningar har framställts av dessa 115 grundämnen. De kända grundämnena finns förtecknade i det periodiska systemet.
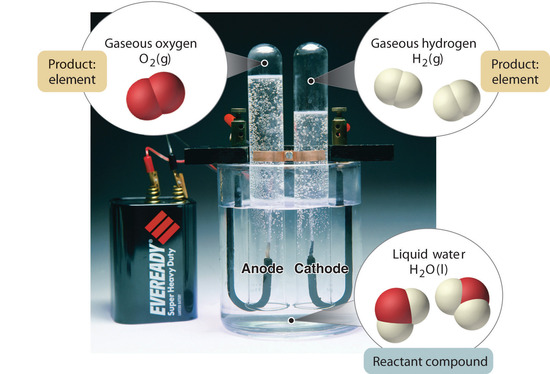
Figur 1.2.5: Nedbrytning av vatten till väte och syre genom elektrolys. Vatten är en kemisk förening; väte och syre är grundämnen.
I allmänhet bryter en omvänd kemisk process ner föreningar till deras grundämnen. Vatten (en förening) kan till exempel sönderdelas till väte och syre (båda grundämnen) genom en process som kallas elektrolys. Vid elektrolys tillhandahåller elektricitet den energi som behövs för att separera en förening till dess beståndsdelar (figur 1.2.5). En liknande teknik används i stor skala för att få fram rent aluminium, ett grundämne, från dess malm, som är en blandning av föreningar. Eftersom det krävs mycket energi för elektrolys är elkostnaden den överlägset största utgiften vid tillverkning av rent aluminium. Återvinning av aluminium är därför både kostnadseffektivt och miljövänligt. Materiens övergripande organisation och de metoder som används för att separera blandningar sammanfattas i figur 1.2.6.
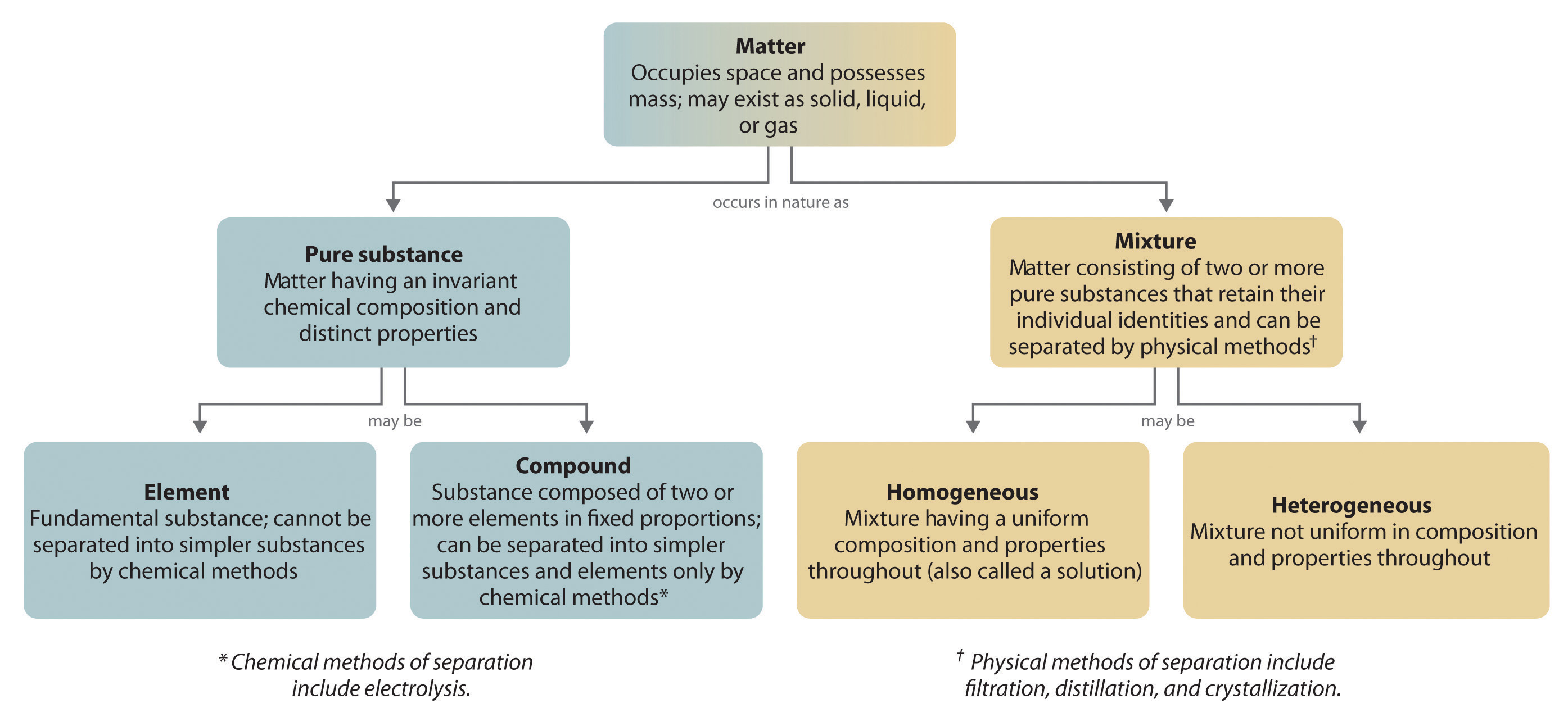
Figur 1.2.6: Förhållanden mellan ämnestyperna och de metoder som används för att separera blandningar
Exempel 1.2.1
Identifiera varje ämne som en förening, ett grundämne, en heterogen blandning eller en homogen blandning (lösning).
- filtrerat te
- friskt pressad apelsinjuice
- en cd-skiva
- aluminiumoxid, ett vitt pulver som innehåller en 2:3 förhållande mellan aluminium- och syreatomer
- selen
Givet: ett kemiskt ämne
Fråga om: dess klassificering
Strategi:
- Besluta om ett ämne är kemiskt rent. Om det är rent är ämnet antingen ett grundämne eller en förening. Om ett ämne kan delas upp i sina grundämnen är det en förening.
- Om ett ämne inte är kemiskt rent är det antingen en heterogen blandning eller en homogen blandning. Om dess sammansättning är enhetlig överallt är det en homogen blandning.
Lösning:
- Ett te är en lösning av föreningar i vatten, så det är inte kemiskt rent. Det separeras vanligtvis från tebladen genom filtrering. B Eftersom lösningens sammansättning är enhetlig i hela lösningen är det en homogen blandning.
- A Apelsinjuice innehåller både partiklar av fast substans (fruktkött) och vätska; den är inte kemiskt ren. B Eftersom dess sammansättning inte är enhetlig överallt är apelsinjuice en heterogen blandning.
- A En cd-skiva är ett fast material som innehåller mer än ett grundämne, med områden med olika sammansättningar som är synliga längs dess kant. Därför är en cd-skiva inte kemiskt ren. B Områden med olika sammansättning tyder på att en compact disc är en heterogen blandning.
- A Aluminiumoxid är en enda, kemiskt ren förening.
- A Selen är ett av de kända grundämnena.
Övning 1.2.1
Identifiera varje ämne som en förening, ett grundämne, en heterogen blandning eller en homogen blandning (lösning).
- vitt vin
- kvicksilver
- ranka-stil salladsdressing
- bordssocker (sackaros)
Svar:
- lösning
- element
- heterogen blandning
- förening
Sammanfattning
Materia kan klassificeras enligt fysiska och kemiska egenskaper. Materia är allt som upptar utrymme och har massa. Materiens tre tillstånd är fast, flytande och gas. En fysisk förändring innebär att ett ämne övergår från ett materietillstånd till ett annat utan att dess kemiska sammansättning ändras. Den mesta materian består av blandningar av rena ämnen, som kan vara homogena (enhetlig sammansättning) eller heterogena (olika områden har olika sammansättning och egenskaper). Rena ämnen kan vara antingen kemiska föreningar eller grundämnen. Föreningar kan brytas ner till grundämnen genom kemiska reaktioner, men grundämnen kan inte separeras till enklare ämnen på kemisk väg. Ämnenas egenskaper kan klassificeras som antingen fysiska eller kemiska. Forskare kan observera fysiska egenskaper utan att ändra ämnets sammansättning, medan kemiska egenskaper beskriver ett ämnes tendens att genomgå kemiska förändringar (kemiska reaktioner) som ändrar dess kemiska sammansättning. Fysiska egenskaper kan vara intensiva eller omfattande. Intensiva egenskaper är desamma för alla prover, beror inte på provets storlek och omfattar till exempel färg, fysiskt tillstånd samt smält- och kokpunkt. Omfattande egenskaper beror på mängden material och omfattar massa och volym. Förhållandet mellan två extensiva egenskaper, massa och volym, är en viktig intensiv egenskap som kallas densitet.
Contributors
Modified by Joshua Halpern (Howard University)