

Atomová teorie Johna Daltona položila základy moderní chemie.
Raný život a vzdělání Johna Daltona
John Dalton se narodil 6. září 1766 v Eaglesfieldu v Anglii
Oba jeho rodiče byli kvakeři. Přestože kvakeři byli křesťané, etablovaná anglikánská církev je považovala za disidenty. V důsledku toho byly možnosti vyššího vzdělání Johna Daltona omezeny na disidentská vzdělávací místa.
Jeho otec byl tkadlec, který vlastnil dům a malé množství půdy.
John Dalton byl inteligentní dítě, které se zajímalo o svět kolem sebe a snažilo se o všem dozvědět co nejvíce.
Do svých 11 let navštěvoval vesnickou školu a poté začal vypomáhat jako učitel.
V 15 letech začal pomáhat svému staršímu bratrovi Johnovi vést kvakerskou internátní školu ve městě Kendal, vzdáleném 40 mil od jeho domova. Po celou dobu pokračoval ve výuce přírodních věd, matematiky, latiny, řečtiny a francouzštiny. V devatenácti letech se stal ředitelem školy a v této funkci pokračoval až do svých 26 let.
Zdá se, že žáci školy byli rádi, že je Dalton učí, jeden z nich vzpomíná:
„Všichni chlapci (byli) rádi, že je učí John Dalton, protože měl mírnější povahu; a kromě toho byla jeho mysl tak zaměstnána matematikou, že mu jejich chyby unikaly.“
Stává se vědcem
V první polovině roku 1793, ve věku 26 let, přijal Dalton místo učitele matematiky a přírodní filozofie na manchesterské New College, disidentské koleji.
V roce 1794 napsal svou první vědeckou práci, kterou nazval: „Vědecké práce:
Byl to vůbec první článek, který pojednával o barvosleposti. Dalton si uvědomil, že tato porucha je dědičná, protože ji měl on i další členové jeho rodiny. Nakonec byla Daltonova teorie o barvosleposti chybná, ale protože byl vůbec prvním člověkem, který ji zkoumal, stal se tento stav známým jako daltonismus.
Po tomto článku publikoval další výzkumné práce z oblasti fyzikálních věd zabývající se vedením tepla, rozpínáním plynů teplem, vlastnostmi světla, polární září a meteorologií.
V roce 1800 Dalton odešel z New College, která měla finanční potíže, a začal pracovat jako soukromý učitel přírodních věd a matematiky.
Teorie atomů
Chování plynů
V roce 1801 Dalton přednesl v Manchesteru sérii přednášek, jejichž obsah byl publikován v roce 1802. V těchto přednáškách prezentoval výzkum, který prováděl v oblasti plynů a kapalin. Tento výzkum byl průlomový a nabídl velké nové poznatky o povaze plynů.
Především Dalton správně uvedl, že nepochybuje o tom, že všechny plyny lze zkapalnit, pokud je jejich teplota dostatečně nízká a tlak dostatečně vysoký.
Poté uvedl, že pokud je v nádobě udržován konstantní objem, mění se tlak plynu přímo úměrně jeho teplotě.
Toto bylo první veřejné vyjádření toho, co se nakonec stalo známým jako Gay-Lussacův zákon, pojmenovaný podle Josepha Gay-Lussaca, který jej publikoval v roce 1809.
V roce 1803 publikoval Dalton svůj zákon parciálních tlaků, který dodnes používá každý univerzitní student chemie a který říká, že ve směsi nereagujících plynů je celkový tlak plynu roven součtu parciálních tlaků jednotlivých plynů.
Daltonova práce ho vyzdvihla jako vědce první kategorie a byl pozván, aby přednášel v Královském institutu v Londýně.
Dalton a atomy
Studium plynů vedlo Daltona k úvahám o tom, z čeho se tyto neviditelné látky vlastně skládají.
Myšlenku atomů poprvé navrhl o více než 2000 let dříve Démokritos ve starém Řecku. Démokritos věřil, že vše se skládá z malých částic zvaných atomy a že tyto atomy nelze rozdělit na menší částice. Měl Démokritos pravdu? To nikdo nevěděl!
Dalton se nyní chystal tuto 2000 let starou záhadu vyřešit.
Provedl nespočet chemických reakcí a v roce 1808 ve své knize Nový systém chemické filosofie publikoval to, čemu dnes říkáme Daltonův zákon:
Tvoří-li dva prvky mezi sebou více než jednu sloučeninu, pak poměry hmotností druhého prvku, které se spojí s pevnou hmotností prvního prvku, budou poměry malých celých čísel.
Příklad Dalton zjistil, že 12 gramů uhlíku může reagovat se 16 gramy kyslíku za vzniku sloučeniny, kterou dnes nazýváme oxid uhelnatý.
Zjistil také, že 12 gramů uhlíku může reagovat s 32 gramy kyslíku za vzniku oxidu uhličitého.
Tento poměr 32:16, který zjednodušeně znamená 2:1, Daltona zaujal.
Analýzou všech shromážděných údajů Dalton vyjádřil své přesvědčení, že hmota existuje jako atomy. Šel ještě dál než Démokritos, když uvedl, že atomy různých prvků mají různou hmotnost. Zveřejnil také diagramy, které znázorňují například:
1. Jak se atomy spojují za vzniku molekul
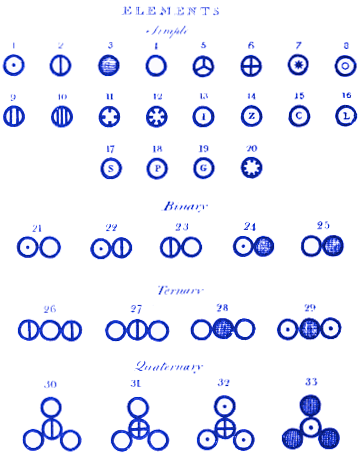

V horní části svého diagramu Dalton přiřadil atomu 1 vodík, 2 dusík, 3 uhlík, 4 kyslík, 5 fosfor atd.
Poté ukázal, jak mohou vypadat molekuly, když se atomy spojí za vzniku sloučenin. Například molekula 21 je voda (OH), 22 je amoniak (NH) a 23 je oxid dusný (NO). Moderní čtenáři si všimnou, že Dalton se v molekulách 21 a 22 spletl. To však není tak důležité jako skutečnost, že Daltonův systém atomů a molekul je téměř totožný s tím, jak bychom je mohli znázornit dnes. Například Daltonova molekula 28 je oxid uhličitý. Dnes bychom oxid uhličitý stále kreslili tímto způsobem.
Amedeo Avogadro brzy publikoval práci, která na Daltona navazovala a opravila některé Daltonovy chyby – Avogadro například uvedl, že voda se má psát H20. Bohužel Avogadrova práce byla po mnoho let ignorována, částečně proto, že nesouhlasila s Daltonovou prací.
2. Jak mohou vypadat molekuly vody v ledu
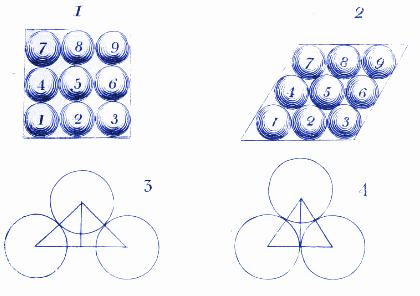

Tady Dalton ukazuje, jak se mohou uspořádat molekuly vody, když jsou zmrzlé v ledu. Podobné diagramy dnes používáme k tomu, abychom ukázali, jak se atomy a molekuly uspořádávají v krystalech.
Daltonova atomová teorie říká, že:
1. Prvky se skládají z atomů, což jsou nepatrné částice, příliš malé na to, abychom je viděli.
2. Všechny atomy určitého prvku jsou stejné.
3. Atomy různých prvků mají různé vlastnosti: liší se jejich hmotnosti a liší se i jejich chemické reakce.
4. Atomy nelze vytvořit, zničit ani rozdělit.
5. Prvky se skládají z atomů. Při chemické reakci se atomy navzájem spojují nebo oddělují.
6. Atomy se spojují v jednoduchých celočíselných poměrech a tvoří sloučeniny.
Přestože jsme se dozvěděli, že atomy téhož prvku mohou mít různé hmotnosti (izotopy) a mohou se štěpit při jaderných reakcích, většina Daltonovy atomové teorie platí i dnes, více než 200 let poté, co ji popsal. Je to základ, na kterém byla postavena moderní chemie.
 „Trvalá pověst pana Daltona bude spočívat v tom, že objevil jednoduchý princip, univerzálně použitelný pro fakta chemie – při stanovení poměrů, v nichž se tělesa spojují, a položil tak základ pro budoucí práci… jeho zásluhy se v tomto ohledu podobají zásluhám Keplera v astronomii.“
„Trvalá pověst pana Daltona bude spočívat v tom, že objevil jednoduchý princip, univerzálně použitelný pro fakta chemie – při stanovení poměrů, v nichž se tělesa spojují, a položil tak základ pro budoucí práci… jeho zásluhy se v tomto ohledu podobají zásluhám Keplera v astronomii.“
Honors
Dalton se neoženil a neměl děti. Po celý život zůstal věrným kvakerem a žil skromně.
V roce 1810 odmítl pozvání stát se členem Královské společnosti. V roce 1822 byl bez svého vědomí zvolen. V roce 1826 mu byla udělena Královská medaile Společnosti za jeho atomovou teorii.
V roce 1833 ho Francouzská akademie věd zvolila jedním ze svých osmi zahraničních členů. V roce 1834 ho Americká akademie věd a umění zvolila za svého zahraničního člena.
Konec
Když bylo Daltonovi 71 let, prodělal malou mozkovou mrtvici – neboli ochrnutí, jak se tehdy říkalo. O rok později ho postihla výraznější mrtvice, po níž nebyl schopen mluvit tak zřetelně jako kdysi. V roce 1844, když mu bylo 77 let, ho postihla další mrtvice. Zemřel ve věku 77 let 27. července 1844.
Jeho vědecká pověst byla tak velká, že když bylo jeho tělo uloženo na radnici v Manchesteru, přišlo se mu poklonit více než 40 000 lidí. John Dalton byl pohřben v Manchesteru na hřbitově v Ardwicku.