

John Dalton legde met zijn Atoomtheorie de grondslag voor de moderne scheikunde.
John Dalton’s vroege leven en opvoeding
John Dalton werd geboren op 6 september 1766 in Eaglesfield, Engeland, UK.
Beide van zijn ouders waren Quakers. Hoewel Quakers christenen waren, werden zij door de gevestigde Kerk van Engeland als andersdenkenden beschouwd. Als gevolg hiervan waren de hogere onderwijskansen van John Dalton beperkt tot andersgezinde opleidingsinstituten.
Zijn vader was wever en bezat een huis en een kleine hoeveelheid land.
John Dalton was een intelligent kind, dat belangstelling had voor de wereld om hem heen en probeerde overal zoveel mogelijk over te leren.
Hij ging tot zijn 11e naar de dorpsschool en begon toen te helpen als onderwijzer.
Op 15-jarige leeftijd begon hij zijn oudere broer John te helpen bij het leiden van een Quaker kostschool in de stad Kendal, 40 mijl van zijn huis. Al die tijd bleef hij zichzelf wetenschappen, wiskunde, Latijn, Grieks en Frans leren. Tegen de tijd dat hij 19 was, was hij het hoofd van de school geworden, en hij bleef deze rol vervullen tot hij 26 jaar oud was.
Het lijkt erop dat de leerlingen van de school het prettig vonden om les te krijgen van Dalton, een van hen herinnert zich:
“De jongens (waren) allemaal blij om les te krijgen van John Dalton, omdat hij een zachtere inborst had; en bovendien was zijn geest zo bezig met wiskunde, dat hun fouten aan zijn aandacht ontsnapten.”
Wetenschapper worden
In de eerste helft van 1793, 26 jaar oud, aanvaardde Dalton de functie van leraar wiskunde en natuurfilosofie aan Manchester’s New College, een dissenting college.
In 1794 schreef hij zijn eerste wetenschappelijke verhandeling die hij noemde: Extraordinary Facts Relating to the Vision of Colours.
Dit was het allereerste artikel over kleurenblindheid. Dalton had zich gerealiseerd dat de aandoening erfelijk was, omdat hij en andere leden van zijn familie het hadden. Uiteindelijk was Dalton’s theorie over kleurenblindheid fout, maar omdat hij de eerste was die er ooit onderzoek naar deed, werd de aandoening bekend als Daltonisme.
Daarna publiceerde hij meer onderzoekspapers in de natuurwetenschappen over warmtegeleiding, gasexpansie door warmte, de eigenschappen van licht, de aurora borealis, en meteorologie.
In 1800 nam Dalton ontslag bij New College, dat in financiële moeilijkheden verkeerde, en ging hij werken als privéleraar natuurwetenschappen en wiskunde.
Atomaire theorie
Het gedrag van gassen
In 1801 gaf Dalton een serie lezingen in Manchester waarvan de inhoud in 1802 werd gepubliceerd. In deze lezingen presenteerde hij onderzoek dat hij had verricht naar gassen en vloeistoffen. Dit onderzoek was baanbrekend en bood grote nieuwe inzichten in de aard van gassen.
Ten eerste verklaarde Dalton terecht dat hij er niet aan twijfelde dat alle gassen vloeibaar konden worden gemaakt, mits hun temperatuur voldoende laag was en de druk voldoende hoog.
Hij stelde vervolgens dat wanneer het volume in een vat constant wordt gehouden, de druk van een gas recht evenredig varieert met de temperatuur.
Dit was de eerste openbare verklaring van wat uiteindelijk bekend werd als de Wet van Gay-Lussac, genoemd naar Joseph Gay-Lussac die deze in 1809 publiceerde.
In 1803 publiceerde Dalton zijn Wet van de Partiële Druk, die nog steeds door elke universitaire scheikundestudent wordt gebruikt, en die stelt dat in een mengsel van gassen die niet met elkaar reageren, de totale gasdruk gelijk is aan de som van de partiële drukken van de afzonderlijke gassen.
Dalton’s werk onderscheidde hem als een wetenschapper van de eerste rang, en hij werd uitgenodigd om lezingen te geven aan het Royal Institution in Londen.
Dalton en Atomen
Dalton’s studie van gassen bracht Dalton ertoe zich af te vragen waar deze onzichtbare stoffen eigenlijk van gemaakt waren.
Het idee van atomen was meer dan 2000 jaar eerder voor het eerst geopperd door Democritus in het oude Griekenland. Democritus geloofde dat alles was opgebouwd uit minuscule deeltjes, atomen genaamd, en dat deze atomen niet in kleinere deeltjes konden worden gesplitst. Had Democritus gelijk? Niemand wist het!
Dalton ging nu dit 2000 jaar oude mysterie oplossen.
Hij voerde talloze chemische reacties uit en publiceerde in 1808 in zijn boek A New System of Chemical Philosophy wat wij nu de Wet van Dalton noemen:
Als twee elementen onderling meer dan één verbinding vormen, dan zullen de verhoudingen van de massa’s van het tweede element die met een vaste massa van het eerste element samengaan, verhoudingen van kleine gehele getallen zijn.
Zo ontdekte Dalton bijvoorbeeld dat 12 gram koolstof met 16 gram zuurstof kon reageren tot de verbinding die we nu koolstofmonoxide noemen.
Hij ontdekte ook dat 12 gram koolstof met 32 gram zuurstof kon reageren tot koolstofdioxide.
Deze verhouding van 32:16, die vereenvoudigd kan worden tot 2:1, intrigeerde Dalton.
Alle gegevens die hij verzamelde analyserend, verklaarde Dalton zijn overtuiging dat materie bestaat als atomen. Hij ging verder dan Democritus, door te stellen dat atomen van verschillende elementen verschillende massa’s hebben. Hij publiceerde ook diagrammen die bijvoorbeeld laten zien:
1. Hoe atomen combineren om moleculen te vormen
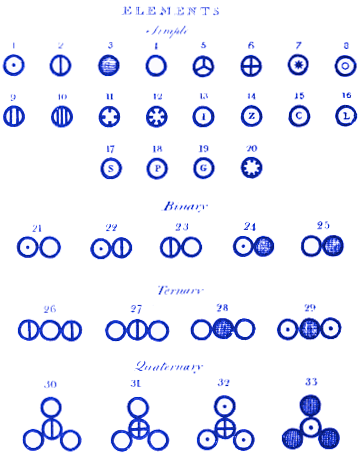

Bovenaan zijn diagram wijst Dalton atoom 1 toe aan waterstof, 2 aan stikstof, 3 aan koolstof, 4 aan zuurstof, 5 aan fosfor, enz.
Hij laat dan zien hoe moleculen eruit zouden kunnen zien wanneer de atomen combineren om samenstellingen te vormen. Bijvoorbeeld, molecule 21 is water (OH), 22 is ammoniak (NH) en 23 is stikstofoxide (NO). Moderne lezers zullen zien dat Dalton moleculen 21 en 22 fout heeft. Dit is minder belangrijk dan het feit dat Dalton’s systeem van atomen en moleculen bijna identiek is aan hoe wij ze vandaag zouden voorstellen. Dalton’s molecuul 28 is bijvoorbeeld koolstofdioxide. Vandaag de dag zouden we kooldioxide nog steeds op deze manier tekenen.
Amedeo Avogadro publiceerde al snel werk dat voortbouwde op dat van Dalton en enkele van Dalton’s fouten corrigeerde – Avogadro zei bijvoorbeeld dat water H20 moest worden geschreven. Helaas werd Avogadro’s werk jarenlang genegeerd, deels omdat het niet overeenkwam met dat van Dalton.
2. Hoe watermoleculen er in ijs uit zouden kunnen zien
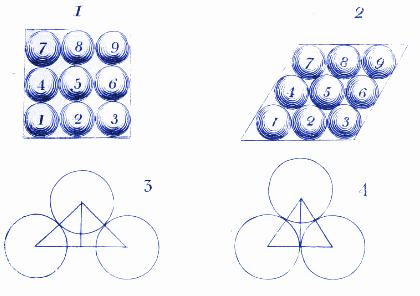

Hier laat Dalton zien hoe watermoleculen zich zouden kunnen rangschikken als ze in ijs bevroren zijn. Tegenwoordig gebruiken we soortgelijke diagrammen om te laten zien hoe atomen en moleculen zich rangschikken in kristallen.
Dalton’s Atoomtheorie stelt dat:
1. De elementen zijn gemaakt van atomen, dat zijn kleine deeltjes, te klein om te zien.
2. Alle atomen van een bepaald element zijn identiek.
3. Atomen van verschillende elementen hebben verschillende eigenschappen: hun massa’s zijn verschillend, en hun chemische reacties zijn verschillend.
4. Atomen kunnen niet worden gemaakt, vernietigd, of gesplitst.
5. In een chemische reactie verbinden atomen zich met elkaar, of scheiden ze zich van elkaar.
6. Atomen verbinden zich in eenvoudige verhoudingen van hele getallen om verbindingen te vormen.
Hoewel we geleerd hebben dat atomen van hetzelfde element verschillende massa’s kunnen hebben (isotopen), en in kernreacties gesplitst kunnen worden, blijft het grootste deel van Dalton’s Atoomtheorie vandaag de dag nog overeind, meer dan 200 jaar nadat hij haar beschreef. Het is het fundament waarop de moderne scheikunde is gebouwd.
 “De blijvende reputatie van de heer Dalton zal berusten op het feit dat hij een eenvoudig principe heeft ontdekt, universeel toepasbaar op de feiten van de scheikunde – in het vaststellen van de verhoudingen waarin lichamen zich vermengen, en daarmee de basis heeft gelegd voor toekomstige werkzaamheden… zijn verdiensten in dit opzicht lijken op die van Kepler in de astronomie.”
“De blijvende reputatie van de heer Dalton zal berusten op het feit dat hij een eenvoudig principe heeft ontdekt, universeel toepasbaar op de feiten van de scheikunde – in het vaststellen van de verhoudingen waarin lichamen zich vermengen, en daarmee de basis heeft gelegd voor toekomstige werkzaamheden… zijn verdiensten in dit opzicht lijken op die van Kepler in de astronomie.”
Honors
Dalton huwde niet en had geen kinderen. Hij bleef zijn hele leven een trouwe Quaker en leefde bescheiden.
In 1810 sloeg hij een uitnodiging af om lid te worden van de Royal Society. In 1822 werd hij zonder zijn medeweten gekozen. In 1826 ontving hij de Royal Medal van de Society voor zijn atoomtheorie.
In 1833 verkoos de Franse Academie van Wetenschappen hem tot een van haar acht buitenlandse leden. In 1834 verkoos de American Academy of Arts and Sciences hem tot buitenlands lid.
The End
Toen hij 71 jaar oud was, kreeg Dalton een kleine beroerte – of verlamming zoals dat toen heette. Een jaar later kreeg hij een zwaardere beroerte waardoor hij niet meer zo duidelijk kon spreken als hij ooit had gekund. In 1844, toen hij 77 was, werd hij opnieuw getroffen door een beroerte. Hij stierf op 77-jarige leeftijd op 27 juli 1844.
Zijn wetenschappelijke reputatie was zo groot dat toen zijn lichaam in het stadhuis van Manchester werd bijgezet, het werd bezocht door meer dan 40.000 mensen die hun respect betuigden. John Dalton werd begraven in Manchester op het Ardwick kerkhof.