Sikäli kuin saatavilla on substraattia, johon sitoutua, entsyymin konsentraation lisääminen nopeuttaa entsymaattista reaktiota. Kun kaikki substraatti on sitoutunut, reaktio ei enää nopeudu entsyymikonsentraation kasvaessa, koska ylimääräisille entsyymeille ei ole enää mitään, mihin sitoutua.
Miten entsyymit toimivat?
Ensyymi on katalyyttinen proteiini, joka voi nopeuttaa kemiallista reaktiota muuttumatta reaktioprosessissa. Reaktioprosessissa entsyymin ja substraatin välille ei muodostu sidosta, joten entsyymi palaa alkuperäiseen muotoonsa ja sitä voidaan käyttää uudelleen. Entsyymi sitoutuu substraattiin aktiivisen alueen kautta muodostaen entsyymi-substraatti-kompleksin. Ne ovat hyvin spesifisiä reaktiossa ja myös substraatille, johon ne sitoutuvat. Kun substraatin muoto vastaa entsyymin aktiivista kohdetta, entsyymin toiminta on oikea, ja niiden toiminta on riippuvainen sen kolmiulotteisesta rakenteesta. Ne helpottavat reaktion tapahtumista pienentämällä aktivaatioenergiaa ja aktivoimalla useampia molekyylejä, jolloin katalyytti toteutuu.
Ensiymin konsentraation vaikutus
Kemiallisessa reaktiossa entsyymin konsentraatiolla on suuri merkitys, koska sitä tarvitaan reagoimaan substraatin kanssa. Usein pieni määrä entsyymiä voi kuluttaa suuren määrän substraattia. Kuitenkin entsyymin konsentraation kasvaessa myös aktiivisten paikkojen tehokkuus kasvaa, joten nämä aktiiviset paikat muuttavat substraattimolekyylit tuotteiksi. Tämä tarkoittaa periaatteessa sitä, että jos entsyymin konsentraatiota halutaan nostaa, substraattia on oltava ylimäärin eli reaktion on oltava riippumaton substraatin konsentraatiosta.
Zero-Order Reaction
Voidaksemme tutkia entsyymin konsentraation kasvattamisen vaikutusta reaktionopeuteen, substraattia on oltava ylimäärin eli reaktion on oltava riippumaton substraatin konsentraatiosta. Kaikki muutokset muodostuvan tuotteen määrässä tietyn ajan kuluessa riippuvat läsnä olevan entsyymin määrästä. Graafisesti tämä voidaan esittää seuraavasti:
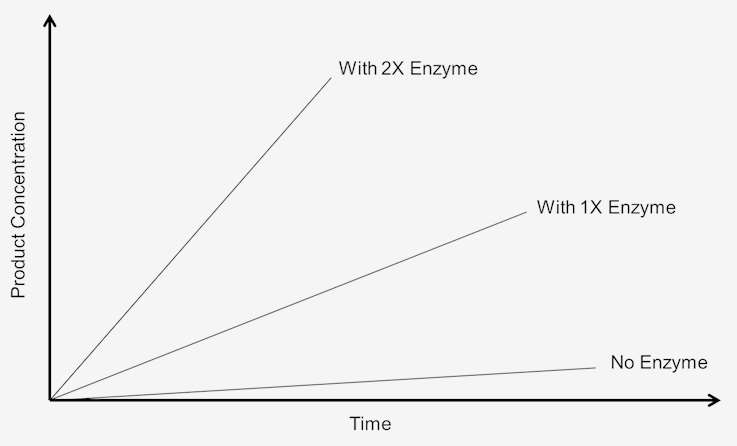 Kuva 1. Nollajärjestyksen reaktionopeus on riippuvainen substraatin konsentraatiosta.
Kuva 1. Nollajärjestyksen reaktionopeus on riippuvainen substraatin konsentraatiosta.
Näitä reaktioita sanotaan ”nollajärjestyksen reaktioiksi”, koska nopeudet ovat riippumattomia substraatin konsentraatiosta. Tuotteen muodostuminen etenee nopeudella, joka on lineaarinen ajan kanssa. Substraatin lisääminen ei lisää nopeutta. Nollajärjestyksen kinetiikassa, jos kokeen annetaan kulua kaksinkertainen aika, saadaan kaksinkertainen määrä tuotetta.
Reaktiossa olevan entsyymin määrää mitataan sen katalysoimalla aktiivisuudella. Aktiivisuuden ja konsentraation väliseen suhteeseen vaikuttavat monet tekijät, kuten lämpötila, pH jne. Entsyymimääritys on suunniteltava siten, että havaittu aktiivisuus on verrannollinen läsnä olevan entsyymin määrään, jotta entsyymin konsentraatio on ainoa rajoittava tekijä. Se täyttyy vain silloin, kun reaktio on nollajärjestyksessä.
Seuraavat palvelut
Enzymikineettiset
entsymologiset määritykset
Keskustellaksesi lisäpalveluiden yksityiskohdista, ota yhteyttä soittamalla numeroon 1-631-562-8517 tai lähettämällä sähköpostia osoitteeseen [email protected].