Nombre genérico: dextrano de hierro
Forma farmacéutica: inyección
Revisado médicamente por Drugs.com. Actualizado por última vez el 1 de diciembre de 2019.
- Descripción general
- Efectos secundarios
- Dosificación
- Profesional
- Interacciones
- Más
Se han producido reacciones de tipo anafiláctico, incluso mortales, tras la administración parenteral de hierro dextrano inyectable.
- Disponer de un equipo de reanimación y de personal formado en la detección y tratamiento de reacciones de tipo anafiláctico durante la administración de Infed®.
- Administrar una dosis de prueba de Infed® antes de la primera dosis terapéutica. Si no hay signos o síntomas de reacciones de tipo anafiláctico después de la dosis de prueba, administre la dosis terapéutica completa de Infed®.
- Durante todas las administraciones de Infed®, observe si hay signos o síntomas de reacciones de tipo anafiláctico. Se han producido reacciones mortales después de la dosis de prueba de la inyección de dextrano de hierro. También se han producido reacciones mortales en situaciones en las que se toleró la dosis de prueba.
- Utilice Infed® sólo en pacientes en los que las investigaciones clínicas y de laboratorio hayan establecido un estado de deficiencia de hierro no susceptible de tratamiento con hierro oral.
- Los pacientes con antecedentes de alergia a medicamentos o con alergias a múltiples medicamentos pueden tener un mayor riesgo de reacciones de tipo anafiláctico a Infed®.
- DESCRIPCIÓN:
- FARMACOLOGÍA CLÍNICA:
- INDICACIONES Y USO:
- CONTRAINDICACIONES:
- ADVERTENCIAS:
- PRECAUCIONES:
- REACCIONES ADVERSAS:
- Sobredosis:
- DOSIFICACIÓN Y ADMINISTRACIÓN:
- Cómo se suministra:
- Etiqueta de muestra
- Más información sobre Infed (hierro dextrano)
- Recursos para el consumidor
- Recursos para el profesional
- Guías de tratamiento relacionadas
DESCRIPCIÓN:
Infed (Iron Dextran Injection USP) es un complejo líquido estéril de color marrón oscuro, ligeramente viscoso, de hidróxido férrico y dextrano para uso intravenoso o intramuscular.
Cada mL contiene el equivalente a 50 mg de hierro elemental (como complejo de hierro dextrano), aproximadamente 0,9% de cloruro de sodio, en agua para inyección. Puede haberse utilizado hidróxido de sodio y/o ácido clorhídrico para ajustar el pH. El pH de la solución está entre 4,5 y 7,0.
Clase terapéutica: Hematínico
FARMACOLOGÍA CLÍNICA:
General: Tras la inyección intramuscular, el dextrano de hierro se absorbe desde el lugar de la inyección hacia los capilares y el sistema linfático. El dextrano de hierro circulante es eliminado del plasma por las células del sistema reticuloendotelial, que dividen el complejo en sus componentes de hierro y dextrano. El hierro se une inmediatamente a las proteínas disponibles para formar hemosiderina o ferritina, las formas fisiológicas del hierro, o en menor medida a la transferrina. Este hierro, que está sujeto a un control fisiológico, repone la hemoglobina y las reservas de hierro agotadas.
El dextrano, una poliglucosa, se metaboliza o se excreta. Se pierden cantidades insignificantes de hierro por vía urinaria o alimentaria tras la administración de dextrano de hierro.
La mayor parte de las inyecciones intramusculares de dextrano de hierro se absorbe en un plazo de 72 horas; la mayor parte del hierro restante se absorbe a lo largo de las 3 a 4 semanas siguientes.
Varios estudios en los que se administró por vía intravenosa dextrano de hierro 59Fe a sujetos con deficiencia de hierro, algunos de los cuales tenían enfermedades coexistentes, han arrojado valores de vida media que oscilan entre 5 horas y más de 20 horas. El valor de 5 horas se determinó para el dextrano de hierro 59Fe a partir de un estudio que utilizó métodos de laboratorio para separar el dextrano de hierro 59Fe circulante del 59Fe unido a la transferrina. El valor de 20 horas refleja una vida media determinada por la medición del 59Fe total, tanto circulante como ligado. Debe entenderse que estos valores de vida media no representan la eliminación del hierro del cuerpo. El hierro no se elimina fácilmente del organismo y su acumulación puede ser tóxica.
Los estudios in vitro han demostrado que la eliminación del hierro dextrano por diálisis es insignificante.1,2 Se investigaron seis membranas de dializador diferentes (polisulfona, cuprofano, acetato de celulosa, triacetato de celulosa, polimetilmetacrilato y poliacrilonitrilo), incluidas las consideradas de alta eficacia y alto flujo.
INDICACIONES Y USO:
Las inyecciones intravenosas o intramusculares de Infed están indicadas para el tratamiento de pacientes con deficiencia de hierro documentada en los que la administración oral es insatisfactoria o imposible.
CONTRAINDICACIONES:
Hipersensibilidad al producto. Todas las anemias no asociadas a la deficiencia de hierro.
ADVERTENCIAS:
Riesgo de reacciones de tipo anafiláctico: Después de la administración parenteral de dextrano de hierro se han producido reacciones de tipo anafiláctico, incluso mortales. Durante la administración de Infed se debe disponer siempre de un equipo de reanimación y de personal formado en la detección y tratamiento de reacciones de tipo anafiláctico. Antes de la primera dosis terapéutica, administrar una dosis de prueba de Infed de 0,5 mL. (Ver DOSIFICACIÓN Y ADMINISTRACIÓN.) Aunque las reacciones suelen ser evidentes en pocos minutos, observe a los pacientes durante al menos una hora antes de administrar la dosis terapéutica. Durante todas las administraciones de Infed, observe a los pacientes para detectar signos o síntomas de reacciones de tipo anafiláctico. Se han producido reacciones mortales después de la dosis de prueba de dextrano de hierro y también han ocurrido en situaciones en las que la dosis de prueba fue tolerada. Utilice Infed sólo en pacientes en los que las investigaciones clínicas y de laboratorio hayan establecido un estado de deficiencia de hierro no susceptible de tratamiento con hierro oral.
Los factores que afectan al riesgo de reacciones de tipo anafiláctico a los productos de dextrano de hierro no se conocen completamente, pero los limitados datos clínicos sugieren que el riesgo puede ser mayor entre los pacientes con antecedentes de alergia a medicamentos o alergias a múltiples medicamentos. Además, el uso concomitante de medicamentos inhibidores de la enzima convertidora de la angiotensina puede aumentar el riesgo de reacciones a un producto de dextrano de hierro. El grado de riesgo de reacciones de tipo anafiláctico tras la exposición a cualquier producto específico de dextrano de hierro es desconocido y puede variar entre los productos.
Los productos de dextrano de hierro difieren en sus características químicas y pueden diferir en sus efectos clínicos. Los productos de dextrano de hierro no son clínicamente intercambiables.
Reacciones retardadas: Las grandes dosis intravenosas, como las utilizadas con las infusiones de dosis total (TDI), se han asociado con una mayor incidencia de efectos adversos. Los efectos adversos son frecuentemente reacciones retardadas (1-2 días) tipificadas por uno o más de los siguientes síntomas: artralgia, dolor de espalda, escalofríos, mareos, fiebre moderada a alta, dolor de cabeza, malestar, mialgia, náuseas y vómitos. La aparición suele ser a las 24-48 horas de la administración y los síntomas suelen remitir en 3-4 días. Se desconoce la etiología de estas reacciones. El potencial de una reacción retardada debe considerarse al estimar el riesgo/beneficio del tratamiento.
La dosis máxima diaria no debe exceder de 2 mL de dextrano de hierro sin diluir.
Riesgo en pacientes con enfermedades subyacentes: Infed debe utilizarse con extremo cuidado en pacientes con deterioro grave de la función hepática. No debe utilizarse durante la fase aguda de una enfermedad renal infecciosa.
Las reacciones adversas experimentadas tras la administración de Infed pueden exacerbar las complicaciones cardiovasculares en pacientes con enfermedades cardiovasculares preexistentes.
Carcinogénesis: La inyección intramuscular de complejos de hierro y carbohidratos puede conllevar un riesgo de carcinogénesis. Se ha comprobado que dichos complejos producen sarcoma en condiciones experimentales cuando se administran grandes dosis o pequeñas dosis inyectadas repetidamente en el mismo lugar a ratas, ratones y conejos, y posiblemente en hámsters.
El largo período de latencia entre la inyección de un carcinógeno potencial y la aparición de un tumor hace imposible medir con precisión el riesgo en el hombre. Sin embargo, se han publicado varios informes en los que se describen tumores en el lugar de la inyección en seres humanos que habían recibido previamente inyecciones intramusculares de complejos de hierro y carbohidratos.
PRECAUCIONES:
Generalidades: La terapia injustificada con hierro parenteral provocará un exceso de almacenamiento de hierro con la consiguiente posibilidad de una hemosiderosis exógena. Dicha sobrecarga de hierro es particularmente apta para ocurrir en pacientes con hemoglobinopatías y otras anemias refractarias que podrían ser diagnosticadas erróneamente como anemias por deficiencia de hierro.
Infed debe utilizarse con precaución en individuos con antecedentes de alergias significativas y/o asma. Se han notificado reacciones de anafilaxia y otras reacciones de hipersensibilidad después de dosis de prueba sin complicaciones, así como de dosis terapéuticas de hierro dextrano inyectable. Por lo tanto, administre una dosis de prueba antes de la primera dosis terapéutica de Infed. (Ver ADVERTENCIA EN EL CUADRO y DOSIFICACIÓN: ADMINISTRACIÓN.)
Se debe disponer inmediatamente de epinefrina en caso de reacciones de hipersensibilidad agudas. (Dosis habitual en adultos: 0,5 mL de una solución 1:1000, por inyección subcutánea o intramuscular). Nota: Los pacientes que utilizan agentes betabloqueantes pueden no responder adecuadamente a la epinefrina. En estos pacientes puede ser necesario el uso de isoproterenol o agentes beta-agonistas similares.
Los pacientes con artritis reumatoide pueden presentar una exacerbación aguda del dolor y la inflamación articular tras la administración de Infed.
Los informes en la literatura de países fuera de los Estados Unidos (en particular, Nueva Zelanda) han sugerido que el uso de hierro dextrano intramuscular en neonatos se ha asociado con un aumento de la incidencia de sepsis gramnegativa, principalmente debida a E. Coli.
Información para los pacientes: Se debe informar a los pacientes de las posibles reacciones adversas asociadas al uso de Infed.
Interacciones entre medicamentos y pruebas de laboratorio: Se ha notificado que grandes dosis de dextrano de hierro (5 mL o más) dan un color marrón al suero de una muestra de sangre extraída 4 horas después de la administración.
El medicamento puede causar valores falsamente elevados de bilirrubina sérica y valores falsamente disminuidos de calcio sérico. Las determinaciones de hierro en suero (especialmente mediante ensayos colorimétricos) pueden no ser significativas durante las 3 semanas siguientes a la administración de dextrano de hierro.
La ferritina en suero alcanza un pico aproximadamente entre 7 y 9 días después de una dosis intravenosa de Infed y vuelve lentamente a la línea de base después de unas 3 semanas.
El examen de la médula ósea en busca de reservas de hierro puede no ser significativo durante períodos prolongados después de la terapia con dextrano de hierro porque el dextrano de hierro residual puede permanecer en las células reticuloendoteliales.
Se ha notificado que las exploraciones óseas con 99m Tc-difosfonato muestran una zona densa y semilunar de actividad en las nalgas, siguiendo el contorno de la cresta ilíaca, de 1 a 6 días después de las inyecciones intramusculares de dextrano de hierro.
Se ha notificado que las exploraciones óseas con agentes buscadores de hueso marcados con 99m Tc, en presencia de niveles elevados de ferritina sérica o tras infusiones de dextrano de hierro, muestran una reducción de la captación ósea, una marcada actividad renal y una acumulación excesiva en la sangre y en los tejidos blandos.
Carcinogénesis, mutagénesis, deterioro de la fertilidad: Ver ADVERTENCIAS.
Embarazo: Se ha demostrado que el dextrano de hierro es teratogénico y embriofílico en ratones, ratas, conejos, perros y monos cuando se administra en dosis de aproximadamente 3 veces la dosis máxima en humanos.
No se han observado efectos fetales adversos consistentes en ratones, ratas, conejos, perros y monos a dosis de 50 mg de hierro/kg o menos. Se ha notificado toxicidad fetal y materna en monos con una dosis intravenosa total de 90 mg de hierro/kg durante un periodo de 14 días. Se observaron efectos similares en ratones y ratas con la administración de una dosis única de 125 mg de hierro/kg. Se observaron anomalías fetales en ratas y perros con dosis de 250 mg de hierro/kg y superiores. Los animales utilizados en estas pruebas no presentaban deficiencias de hierro. No existen estudios adecuados y bien controlados en mujeres embarazadas. Infed debe utilizarse durante el embarazo sólo si el beneficio potencial justifica el riesgo potencial para el feto.
Transferencia placentaria: Diversos estudios en animales y en humanos embarazados han demostrado resultados no concluyentes con respecto a la transferencia placentaria del dextrano de hierro como dextrano de hierro. Parece que algo de hierro llega al feto, pero la forma en que atraviesa la placenta no está clara.
Madres lactantes: Debe tenerse precaución cuando se administre Infed a una mujer en periodo de lactancia. En la leche humana se excretan trazas de hierro dextrano sin metabolizar.
Uso pediátrico: No se recomienda su uso en lactantes menores de 4 meses. (Véase POSOLOGÍA Y ADMINISTRACIÓN.)
REACCIONES ADVERSAS:
Graves/Fatales: Se han notificado reacciones anafilácticas con el uso de hierro dextrano inyectable; en ocasiones estas reacciones han sido mortales. Dichas reacciones, que se producen con mayor frecuencia en los primeros minutos de la administración, se han caracterizado generalmente por la aparición repentina de dificultad respiratoria y/o colapso cardiovascular. Dado que se han notificado reacciones anafilácticas mortales después de la administración de la inyección de dextrano de hierro, el fármaco debe administrarse sólo cuando se disponga de técnicas de reanimación y tratamiento del shock anafiláctico y anafilactoide. (Ver ADVERTENCIA DE LA CAJA y PRECAUCIONES: GENERAL, relativas a la disponibilidad inmediata de epinefrina.)
Cardiovascular: Dolor en el pecho, opresión en el pecho, shock, paro cardíaco, hipotensión, hipertensión, taquicardia, bradicardia, rubor, arritmias. (El enrojecimiento y la hipotensión pueden producirse por inyecciones demasiado rápidas por vía intravenosa.)
Dermatológico: Urticaria, prurito, púrpura, erupción, cianosis.
Gastrointestinal: Dolor abdominal, náuseas, vómitos, diarrea.
Hematológico/linfático: Leucocitosis, linfadenopatía.
Musculoesquelético/tejidos blandos: Artralgia, artritis (puede representar una reactivación en pacientes con artritis reumatoide quiescente – Ver PRECAUCIONES: GENERAL), mialgia; dolor de espalda; absceso estéril, atrofia/fibrosis (lugar de la inyección intramuscular); decoloración marrón de la piel y/o del tejido subyacente (tinción), dolor o molestia en o cerca de los lugares de la inyección intramuscular; celulitis; hinchazón; inflamación; flebitis local en o cerca del lugar de la inyección intravenosa.
Neurológico: Convulsiones, ataques, síncope, dolor de cabeza, debilidad, falta de respuesta, parestesia, episodios febriles, escalofríos, mareos, desorientación, entumecimiento, pérdida de conocimiento.
Respiratorio: Parada respiratoria, disnea, broncoespasmo, sibilancias.
Urológico: Hematuria.
Reacciones retardadas: Artralgia, dolor de espalda, escalofríos, mareos, fiebre, dolor de cabeza, malestar, mialgia, náuseas, vómitos. (Ver ADVERTENCIAS).
Varios: Episodios febriles, sudoración, escalofríos, malestar general, alteración del gusto.
Sobredosis:
Es poco probable que la sobredosis con hierro dextrano se asocie con alguna manifestación aguda. Las dosis de dextrano de hierro que excedan los requerimientos para la restauración de la hemoglobina y la reposición de las reservas de hierro pueden dar lugar a hemosiderosis. La monitorización periódica de los niveles de ferritina sérica puede ser útil para reconocer una acumulación progresiva nociva de hierro resultante del deterioro de la captación de hierro del sistema reticuloendotelial en condiciones médicas concurrentes como la insuficiencia renal crónica, la enfermedad de Hodgkin y la artritis reumatoide. La DL50 del dextrano de hierro no es inferior a 500 mg/kg en el ratón.
DOSIFICACIÓN Y ADMINISTRACIÓN:
El hierro oral debe suspenderse antes de la administración de Infed.
Dosificación:
I. Anemia por deficiencia de hierro: La determinación hematológica periódica (hemoglobina y hematocrito) es una técnica sencilla y precisa para monitorizar la respuesta hematológica, y debe utilizarse como guía en la terapia. Debe reconocerse que el almacenamiento de hierro puede ir por detrás de la aparición de una morfología sanguínea normal. El hierro sérico, la capacidad total de fijación del hierro (TIBC) y el porcentaje de saturación de la transferrina son otras pruebas importantes para detectar y monitorizar el estado de deficiencia de hierro.
Después de la administración del complejo de dextrano de hierro, la evidencia de una respuesta terapéutica puede verse en pocos días como un aumento en el recuento de reticulocitos.
Aunque la ferritina sérica suele ser una buena guía para las reservas de hierro corporal, la correlación de las reservas de hierro corporal y la ferritina sérica puede no ser válida en pacientes en diálisis renal crónica que también están recibiendo complejo de dextrano de hierro.
Aunque hay variaciones significativas en la constitución corporal y la distribución del peso entre hombres y mujeres, la tabla y la fórmula adjuntas representan un medio conveniente para estimar el hierro total requerido. Este requerimiento total de hierro refleja la cantidad de hierro necesaria para restaurar la concentración de hemoglobina a niveles normales o casi normales, más una cantidad adicional para proporcionar una reposición adecuada de las reservas de hierro en la mayoría de los individuos con niveles de hemoglobina moderada o gravemente reducidos. Hay que recordar que la anemia ferropénica no aparecerá hasta que se hayan agotado prácticamente todas las reservas de hierro. Por lo tanto, la terapia debe tener como objetivo no sólo la reposición del hierro de la hemoglobina, sino también de las reservas de hierro.
Los factores que contribuyen a la fórmula se muestran a continuación.
 Basado en los factores anteriores, los individuos con niveles normales de hemoglobina tendrán aproximadamente 33 mg de hierro en sangre por kilogramo de peso corporal (15 mg/lb).
Basado en los factores anteriores, los individuos con niveles normales de hemoglobina tendrán aproximadamente 33 mg de hierro en sangre por kilogramo de peso corporal (15 mg/lb).
Nota: La tabla y la fórmula que la acompaña son aplicables para la determinación de la dosis sólo en pacientes con anemia ferropénica; no deben utilizarse para la determinación de la dosis en pacientes que requieran un reemplazo de hierro por pérdida de sangre.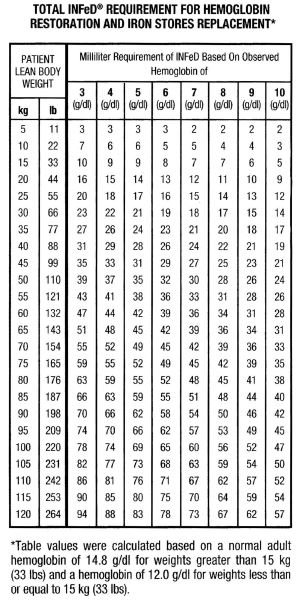
La cantidad total de Infed en mL requerida para tratar la anemia y reponer las reservas de hierro puede aproximarse como sigue:
II. Reposición de hierro por pérdida de sangre: Algunos individuos sufren pérdidas de sangre de forma intermitente o repetitiva. Dichas pérdidas de sangre pueden producirse periódicamente en pacientes con diátesis hemorrágicas (telangiectasia familiar; hemofilia; hemorragia gastrointestinal) y de forma repetitiva por procedimientos como la hemodiálisis renal.
La terapia con hierro en estos pacientes debe dirigirse a la sustitución de la cantidad equivalente de hierro representada en la pérdida de sangre. La tabla y la fórmula descritas en el apartado I. Anemia ferropénica no son aplicables para los valores simples de reposición de hierro.
Las estimaciones cuantitativas de la pérdida periódica de sangre y del hematocrito del individuo durante el episodio hemorrágico proporcionan un método conveniente para el cálculo de la dosis de hierro necesaria.
La fórmula que se muestra a continuación se basa en la aproximación de que 1 mL de hematíes normocíticos y normocrómicos contiene 1 mg de hierro elemental:
Hierro de reposición (en mg) = Pérdida de sangre (en mL) x hematocrito
Ejemplo: Pérdida de sangre de 500 mL con 20% de hematocrito
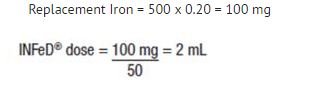
Administración:
La cantidad total de Infed necesaria para el tratamiento de la anemia ferropénica o la reposición de hierro por pérdida de sangre se determina a partir de la tabla o de la fórmula adecuada. (Ver Dosificación).
1. Inyección intravenosa – ANTES DE LA PRIMERA DOSIS TERAPÉUTICA INTRAVENOSA, ADMINISTRAR UNA DOSIS INTRAVENOSA DE PRUEBA DE 0,5 ML. ADMINISTRAR LA DOSIS DE PRUEBA A UN RITMO GRADUAL DURANTE AL MENOS 30 SEGUNDOS. Aunque las reacciones anafilácticas que se conocen tras la administración de Infed suelen ser evidentes a los pocos minutos, o antes, se recomienda que transcurra un periodo de una hora o más antes de administrar el resto de la dosis terapéutica inicial.
Pueden administrarse diariamente dosis individuales de 2 mL o menos hasta alcanzar la cantidad total calculada necesaria. Infed se administra sin diluir a un ritmo lento y gradual que no supere los 50 mg (1 mL) por minuto.
2. Inyección intramuscular – ANTES DE LA PRIMERA DOSIS TERAPÉUTICA INTRAMUSCULAR DE INFED, ADMINISTRAR UNA DOSIS INTRAMUSCULAR DE PRUEBA DE 0,5 ML. (La dosis de prueba debe administrarse en la nalga utilizando la misma técnica descrita en el último párrafo de esta sección. Aunque las reacciones anafilácticas que se conocen tras la administración de Infed suelen ser evidentes en pocos minutos o antes, se recomienda que transcurra al menos una hora o más antes de administrar el resto de la dosis terapéutica inicial.
Si no se observan reacciones adversas, Infed puede administrarse de acuerdo con el siguiente programa hasta alcanzar la cantidad total calculada requerida. La dosis de cada día no debe exceder normalmente de 0,5 mL (25 mg de hierro) para los lactantes de menos de 5 kg (11 libras); 1,0 mL (50 mg de hierro) para los niños de menos de 10 kg (22 libras); y 2,0 mL (100 mg de hierro) para los demás pacientes.
Infed debe inyectarse sólo en la masa muscular del cuadrante superior externo de la nalga -nunca en el brazo u otras zonas expuestas- y debe inyectarse profundamente, con una aguja de 2 ó 3 pulgadas de calibre 19 ó 20. Si el paciente está de pie, debe apoyar su peso en la pierna opuesta al lugar de la inyección, o si está en la cama, debe estar en posición lateral con el lugar de la inyección más arriba. Para evitar la inyección o la fuga en el tejido subcutáneo, se recomienda una técnica de vía Z (desplazamiento de la piel lateralmente antes de la inyección).
NOTA: No mezcle Infed con otros medicamentos ni lo añada a soluciones de nutrición parenteral para infusión intravenosa.
Los productos farmacéuticos parenterales deben inspeccionarse visualmente para detectar partículas y decoloración antes de su administración, siempre que la solución y el envase lo permitan.
Cómo se suministra:
Infed (Iron Dextran Injection USP), que contiene 50 mg de hierro elemental por mL, se presenta en viales ámbar monodosis de 2 mL (para uso intramuscular o intravenoso) en cajas de 10 unidades (NDC 0023-6082-10).
Almacenar a 20 -25°C (68 -77°F).
Sólo con receta

Para cualquier consulta médica contactar con:
Allergan
Comunicaciones Médicas
1-800-678-1605
Distribuido por:
Allergan USA, Inc.
Madison, NJ 07940
Fabricado por:
Patheon Italia S.p.A.
Ferentino, Italia 03013
© 2019 Allergan. Todos los derechos reservados.
Infed® es una marca registrada de Allergan Sales, LLC.
Allergan® y su diseño son marcas comerciales de Allergan, Inc.
Contenido actualizado: Noviembre de 2018
v.1.1USPI6082
Etiqueta de muestra


| Infed inyección de dextrano de hierro |
||||||||||||
|
||||||||||||
|
||||||||||||
|
||||||||||||
|
||||||||||||
|
||||||||||||
Etiquetadora – Inyectables generales & Vacunas, Inc. (108250663)
Más información sobre Infed (hierro dextrano)
- Efectos secundarios
- Durante el embarazo o la lactancia
- Información sobre la dosis
- Interacciones con otros medicamentos
- Precios &Cupones
- En español
- Clase de medicamentos: productos de hierro
Recursos para el consumidor
- Información para el paciente
- Infed (lectura avanzada)
Recursos para el profesional
- Información para la prescripción
- Hierro Dextrano hidrogenado (FDA)
Otras marcas Dexferrum
Guías de tratamiento relacionadas
- Anemia asociada a la insuficiencia renal crónica
- Anemia ferropénica
Descargo de responsabilidad médica