INTRODUZIONE
La malattia di Chagas o tripanosomiasi americana è una parassitosi originaria del continente americano. Carlos Chagas descrisse la malattia all’inizio del 20° secolo e continua a rappresentare una delle sfide più significative per la salute pubblica in America Latina.
Le tendenze epidemiologiche degli ultimi 20 anni rivelano chiaramente una riduzione generale della trasmissione del vettore grazie ai programmi di controllo e ai miglioramenti nelle abitazioni rurali, così come l’interruzione della trasmissione del vettore in Cile, Uruguay e recentemente in Brasile, tutto ciò ha contribuito ad una riduzione dell’incidenza della malattia in tutto il continente.1-3
Nell’ambiente naturale, il Trypanosoma cruzi è trasmesso attraverso una varietà di specie di insetti triatomini, che agiscono come vettori. Tuttavia, altri meccanismi di trasmissione non vettoriali sono stati descritti attraverso prodotti ematici, trapianto di organi e trasmissione verticale. Nelle regioni in cui l’infezione è endemica, la trasmissione orale è stata descritta anche attraverso l’ingestione di cibo contaminato da feci di insetti infetti.4,5
Oggi la malattia di Chagas colpisce da 10 a 12 milioni di individui in tutto il mondo.6 La sua distribuzione geografica si estende dal 40° parallelo nord, nella parte meridionale del Nord America, al 45° parallelo sud, in Argentina e Cile.7 L’urbanizzazione latinoamericana, che si è intensificata nella seconda metà del XX secolo, ha alterato il profilo epidemiologico della malattia, e i movimenti migratori dai paesi endemici hanno portato alla diagnosi della malattia di Chagas in regioni in cui non è endemica.8,9
La Spagna è diventata uno dei paesi europei che ricevono il maggior numero di immigrati dall’America Latina. Al 31 dicembre 2005, quasi un milione di individui provenienti dall’America Latina erano inclusi nei registri dei cittadini stranieri in possesso di una carta d’identità spagnola,10 anche se i registri del censimento municipale per l’anno 2005 indicavano cifre più alte (1 445 796 individui). Unità e servizi specializzati in medicina tropicale e salute internazionale in Spagna hanno già iniziato a diagnosticare e trattare le persone affette dalla malattia.11
La recente riunione dell’Organizzazione Panamericana della Salute a Montevideo ha discusso questa situazione e nel suo rapporto finale ha menzionato le necessità dei paesi che ricevono immigrati da aree endemiche per affrontare la malattia di Chagas e per essere in grado di fornire un trattamento adeguato alle persone colpite, così come per prevenire la trasmissione verticale e per via ematica del T cruzi.12
PATOGENESI E STORIA NATURALE DELLA MALATTIA DEL CUORE NELLA MALATTIA DI CHAGAS
Dopo la fase acuta dell’infezione, la malattia di Chagas non trattata entra in una fase cronica che inizialmente è asintomatica o non riconosciuta. Successivamente, il 20%-30% dei pazienti sviluppa anomalie cardiache (forma cardiaca), il 10% disturbi digestivi (forma digestiva) o entrambi (forma mista), e meno del 5% dei pazienti sviluppa una forma neurologica della malattia. Il resto rimarrà asintomatico, senza manifestazioni cliniche per tutta la vita.13
A causa della potenziale gravità delle complicazioni cardiache della malattia e della loro frequenza, il secondo workshop sulla malattia di Chagas importata si è concentrato sulle caratteristiche cliniche della malattia cardiaca cronica di Chagas e sui requisiti per una corretta diagnosi, gestione e trattamento. La patogenesi della malattia non è chiara, anche se la comprensione attuale punta verso un’eziologia mista, in cui il parassita sarebbe direttamente coinvolto nella produzione del danno miocardico14,15 e un fenomeno autoimmune associato.16,17 Altri meccanismi patogenetici descritti includono alterazioni microvascolari e denervazione autonoma.18-21
La cardiopatia di Chagas presenta alcune caratteristiche che la differenziano da altre condizioni cardiache più comuni in Spagna:
È una malattia fibrotica che si localizza generalmente nella regione postero-inferiore e apicale del ventricolo sinistro, nel nodo del seno e nel sistema di conduzione al di sotto del fascio, e porta ad anomalie prevalentemente segmentali della contrattilità
È una cardiomiopatia dilatativa con tendenza alla formazione di aneurismi, in particolare nella regione apicale
Ha un potente potenziale aritmogeno e le aritmie ventricolari sono comuni, spesso associate a bradiaritmie (di origine atrioventricolare o derivanti dal nodo del seno)
È associata ad un alto tasso di eventi tromboembolici
Può presentarsi come dolore precordiale, generalmente atipico anche se occasionalmente può simulare una cardiopatia ischemica.
Nel corso naturale della malattia, le anomalie cardiache appaiono progressivamente intorno ai 20-30 anni dopo l’infezione.22 Tuttavia, dal 5% al 10% dei pazienti mostra una miocardite durante la fase acuta che progredisce rapidamente verso una forma grave di cardiopatia di Chagas.23,24 Meno comunemente, i pazienti che sono nella fase cronica della malattia, con un lieve coinvolgimento cardiaco, possono mostrare un’improvvisa esacerbazione con intensa parassitemia e sintomi di insufficienza cardiaca acuta; anche gli immunosoppressori favoriscono queste esacerbazioni.25
VALUTAZIONE DEI PAZIENTI CON SOSPETTO DI MALATTIA DI CHAGAS E MALATTIA DI CUORE DI CHAGAS
Diagnosi dell’infezione da T cruzi
La diagnosi della malattia di Chagas in Spagna è stata affrontata nel documento di consenso del primo workshop sulla malattia di Chagas importata.26 In sintesi, si basa sul rispetto di 2 criteri:
Anamnesi compatibile con l’epidemiologia della malattia: la storia del paziente deve includere almeno 1 elemento che avrebbe reso possibile la trasmissione del T cruzi attraverso una delle vie di infezione descritte (individui provenienti da zone endemiche o figli di madri provenienti da zone endemiche; viaggiatori con soggiorni in regioni endemiche e con uno stile di vita che li mette a rischio di infezione)
Diagnosi microbiologica: gli individui sono considerati infetti quando hanno un risultato positivo in parassitologia o 2 risultati positivi con 2 tecniche sierologiche che utilizzano antigeni diversi. In caso di risultati ambigui o incoerenti, si dovrebbe utilizzare una terza tecnica. Esistono vari test sierologici per la diagnosi della malattia di Chagas che utilizzano diverse tecniche (saggio di immunosorbimento legato ad un enzima, ELISA modificato o ELISA con antigeni ricombinanti, immunofluorescenza, emoagglutinazione indiretta e immunocromatografia). La reazione a catena della polimerasi (PCR) è forse la tecnica più sensibile per l’analisi parassitologica della malattia di Chagas cronica, ma il suo uso non elimina la necessità di test sierologici
Esame cardiaco di base nei pazienti con infezione da T cruzi
Per escludere il coinvolgimento cardiaco nei pazienti con infezione da T cruzi, un’anamnesi completa e un esame fisico completo dovrebbero essere eseguiti insieme a elettrocardiografia, radiografia del torace ed ecocardiografia. I sintomi e i segni della malattia cardiaca di Chagas visti all’esame fisico sono gli stessi della cardiomiopatia in generale e nessuno è caratteristico della malattia.
Anamnesi medica
Lo scopo principale dell’anamnesi è di rilevare i sintomi di una possibile malattia cardiaca sottostante. La tabella 1 mostra i segni e i sintomi che sono più spesso associati alla malattia cardiaca dovuta a T cruzi. È anche importante valutare i disturbi digestivi (disfagia, costipazione, ecc.), poiché entrambe le forme possono talvolta coesistere.

Quando viene presa l’anamnesi del paziente, è importante ricordare che le differenze linguistiche e culturali possono interferire con la comunicazione tra paziente e medico. A volte, i pazienti non applicano lo stesso significato a parole particolari (per esempio, i termini usati in spagnolo per mancanza di respiro, vertigini o palpitazioni) e può essere necessario definire ciò a cui ci si riferisce in ogni caso. Inoltre, gli immigrati spesso soffrono di difficoltà di adattamento, nostalgia di casa e disturbi dell’umore legati alla loro situazione sociale e familiare27 che possono causare problemi nell’identificare con precisione il sintomo cardinale o il motivo della consultazione. Infine, si deve tener conto anche delle condizioni di lavoro sfavorevoli (orari di lavoro lunghi, paura di perdere il lavoro, contratti illegali, ecc) che rappresentano un ulteriore ostacolo alla partecipazione agli appuntamenti programmati. Poiché la malattia è familiare a questi pazienti e li fa preoccupare, la notifica di un risultato positivo per l’infezione o la malattia di Chagas richiede un attento processo di comunicazione attraverso il quale si costruisce la fiducia.12 I mediatori culturali svolgono un ruolo importante in questo processo.
Esame fisico
Si dovrebbe eseguire un esame fisico dettagliato con particolare attenzione al sistema cardiovascolare. Il soffio cardiaco dovuto alla disfunzione valvolare può apparire come risultato della dilatazione delle camere. Nelle fasi più avanzate, si osservano i soliti segni di congestione e ipoperfusione periferica. La cachessia cardiaca è anche un indicatore delle fasi più avanzate della malattia cardiaca di Chagas e ha un alto valore prognostico.
Elettrocardiogramma
Un elettrocardiogramma convenzionale a 12 derivazioni (ECG) con una registrazione lunga (30 secondi) in DII dovrebbe essere eseguito in tutti i pazienti con infezione da T cruzi. Nella fase cronica dell’infezione, le alterazioni ECG appaiono un certo numero di anni prima dei sintomi e della cardiomegalia (Tabella 2). Sebbene non ci sia un pattern caratteristico nell’ECG, queste alterazioni, specialmente il blocco di fascio destro, isolato o associato all’emiblocco anteriore sinistro nei pazienti con sierologia positiva, possono essere considerate indicatori della cardiopatia cronica di Chagas.28-30 Tuttavia, data la loro mancanza di specificità, la diagnosi richiede una conferma, poiché la sua presenza non significa necessariamente un’eziologia chagasica.

Un ECG normale esclude la presenza di una disfunzione ventricolare sinistra moderata o grave, con un valore predittivo negativo vicino al 100%: D’altra parte, maggiore è il numero di cambiamenti ECG, peggiore è la funzione ventricolare.31
Le alterazioni della conduzione intraventricolare e l’allargamento del complesso QRS appaiono presto nella cardiopatia cronica di Chagas, quando le anomalie della contrazione miocardica non sono ancora presenti, il che significa che non hanno il valore prognostico che hanno in altre malattie cardiache.32
Radiografia del torace
La radiografia del torace ha una bassa sensibilità per il rilevamento della cardiopatia di Chagas, poiché la disfunzione ventricolare può verificarsi pur ottenendo una radiografia normale. Tuttavia, l’evidenza di cardiomegalia potrebbe essere predittiva di morte improvvisa nei pazienti con malattia di Chagas cronica.33 Dovrebbe essere eseguita con il paziente in una situazione clinicamente compensata, valutando l’ipertensione venoso-capillare, l’espansione delle camere o un indice cardiotoracico superiore a 0,6 come segni positivi.
Ecocardiografia
Dato che l’ecocardiografia è una tecnica non invasiva ampiamente disponibile che è molto utile per la valutazione della funzione ventricolare, tutti i pazienti con malattia di Chagas sono candidati per un ecocardiogramma di base.
Le alterazioni ecocardiografiche più comuni sono riassunte nella tabella 3.34,35 Le seguenti raccomandazioni sono utili per l’ecocardiografia:

È consigliabile eseguire un esame ecocardiografico transtoracico convenzionale, seguendo un sistema specifico.
1. Utilizzare un trasduttore ad alta frequenza.
2. Ottenere un ecocardiogramma trasversale (per l’analisi segmentale della regione inferoposteriore), una vista apicale a 2 camere e viste intermedie tra 2 e 4 camere, per individuare possibili aneurismi apicali.
3. Particolare attenzione dovrebbe essere prestata alla regione postero-inferiore del ventricolo sinistro, compreso l’apice cardiaco, nel tentativo di identificare ipocinesia segmentale o acinesia, insieme con aneurismi apicali. È anche comune osservare iperecogenicità e restringimento della parete, simile a quello descritto nella cardiopatia ischemica; questo è un substrato per lo sviluppo di aritmie ventricolari rientranti.
4. Si raccomanda di prestare particolare attenzione alla ricerca di contrasto eco spontaneo e l’esistenza di trombi nelle camere.
5. Valutare specificamente la funzione diastolica e la funzione ventricolare destra in tutti i pazienti con sospetta cardiopatia di Chagas. L’alterazione della funzione diastolica del ventricolo sinistro si verifica precocemente nella malattia di Chagas e la sua gravità è solitamente correlata al grado di disfunzione sistolica.36,37
6. L’esame transesofageo è indicato quando la finestra transtoracica non permette la valutazione delle camere sinistre.
La riduzione della frazione di eiezione ventricolare sinistra, l’aumento del diametro endosistolico e un modello di flusso mitrale restrittivo sono i migliori indicatori prognostici ottenuti dall’ecocardiografia nei pazienti con la malattia di Chagas.38,39
Negli stadi avanzati della malattia, quando è presente un’insufficienza cardiaca congestizia, il profilo ecocardiografico predominante comporta una diffusa ipocinesia biventricolare con allargamento di tutte e 4 le camere.
Altri esami cardiologici in pazienti con sospetta cardiopatia di Chagas
Oltre agli studi di base menzionati, altri esami complementari possono essere utili in certi pazienti o circostanze:
Monitoraggio Holter a 24 ore
Il monitoraggio Holter a 24 ore è raccomandato nei pazienti con i seguenti sintomi:
Sintomi suggestivi di aritmia cardiaca (sincope, presincope o palpitazioni)
La presenza di alcune aritmie cardiache nell’ECG, come bradiaritmie sinusali (con una frequenza cardiaca media inferiore a 40 battiti al minuto e/o pause sinusali prolungate), blocchi atrioventricolari di secondo grado, e extrasistoli ventricolari frequenti e/o ripetitivi (burst)
Il monitoraggio Holter di ventiquattro ore permetterà di valutare la possibile associazione dei sintomi con un’aritmia, di identificare i pazienti a rischio di morte improvvisa e di identificare la disfunzione autonomica.33,40 Episodi di tachicardia ventricolare non sostenuta sono registrati in circa il 90% dei pazienti con cardiopatia di Chagas e disfunzione ventricolare o insufficienza cardiaca.41
Il monitoraggio Holter deve essere eseguito con una tecnica convenzionale, preferibilmente con un sistema a 3 canali. La sensibilità della registrazione Holter è bassa quando gli episodi di aritmia sono poco frequenti e altre tecniche come l’Holter impiantabile possono essere utilizzate in questi casi.
Studio elettrofisiologico
Lo scopo di uno studio elettrofisiologico in questi pazienti è di identificare anomalie di conduzione atrioventricolare e intraventricolare e di valutare l’induzione di aritmie ventricolari maligne. Le indicazioni sono le stesse della valutazione di altri disturbi con un rischio di morte improvvisa:
Pazienti con sintomi suggestivi di aritmia (sincope o presincope) non confermati in studi precedenti
Tachicardia ventricolare sostenuta, con o senza sintomi, indipendentemente dal grado di funzione ventricolare
Paziente rianimato da morte improvvisa
Pazienti che mostrano alterazioni nell’ECG o nel monitoraggio Holter che sono associate ad un rischio aumentato di morte improvvisa: extrasistoli ventricolari ripetute o appaiate, episodi di tachicardia ventricolare non sostenuta e aumento dell’intervallo QT associato alla presenza di disfunzione ventricolare.42 In questo sottogruppo di pazienti, se uno studio elettrofisiologico non è possibile, l’amiodarone può essere somministrato empiricamente finché non ci sono controindicazioni.
Test da sforzo
I test da sforzo sarebbero indicati principalmente nei seguenti casi:
Valutazione della capacità funzionale
Valutazione della risposta cronotropa
In presenza di dolore toracico e di cardiopatia di Chagas, il test da sforzo è poco utile per determinare l’eziologia del dolore; in questi casi deve essere eseguita l’angiografia coronarica
Coronarografia
L’angiografia coronarica è indicata secondo i criteri della Società Spagnola di Cardiologia,43 tenendo conto delle considerazioni relative al test da sforzo.
Biopsia miocardica
La biopsia miocardica non è attualmente considerata una tecnica diagnostica nella cardiopatia di Chagas a causa del suo rischio e della sua specificità limitata.
Gestione dei pazienti con infezione da T CRUZI
Pazienti asintomatici con elettrocardiogramma e radiografia del torace normali
Il rischio di cardiopatia di Chagas è maggiore nella seconda e terza decade dopo l’infezione.44 Nei pazienti con evidenza di infezione da T cruzi e con ECG normale o con anomalie minime che non sono suggestive di malattia cardiaca cronica da Chagas, il rischio annuale di progressione verso la malattia cardiaca è tra il 2% e il 5%.45,46 Di conseguenza, si raccomanda un ecocardiogramma di base.
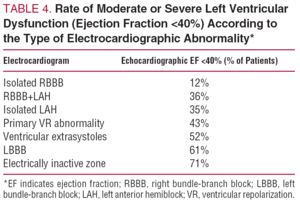
Pazienti asintomatici con anomalie ECG
L’ecocardiografia di base è raccomandata nei pazienti asintomatici con anomalie ECG. I risultati sono molto variabili, e la disfunzione ventricolare sinistra (frazione di eiezione inferiore al 40%) viene rilevata in circa il 30% dei casi. La tabella 4 mostra la prevalenza della disfunzione ventricolare sinistra in base al pattern ECG.47 In generale, la prognosi è determinata dal grado di disfunzione ventricolare.48
La frequenza con cui l’ecocardiografia deve essere ripetuta dipende dalle condizioni cliniche del paziente. Anche se gli studi non sono disponibili, la progressione della malattia è lenta nei pazienti asintomatici con un ecocardiogramma normale; di conseguenza, è sufficiente ripetere la valutazione entro i 5 anni successivi in questo gruppo, finché non compaiono sintomi. Quando lo studio iniziale rivela anomalie, deve essere ripetuto in un periodo da 1 a 3 anni, a causa dell’aumento del rischio di progressione,49 soprattutto se c’è una disfunzione ventricolare significativa (frazione di eiezione inferiore al 40%). In qualsiasi paziente, la comparsa di nuovi sintomi o anomalie ECG dovrebbe essere considerata un’indicazione per un nuovo ecocardiogramma.
Lo scopo del follow-up ecocardiografico è quello di identificare i pazienti con disfunzione moderata o grave, che spesso sono ancora asintomatici ma che potrebbero beneficiare della fornitura precoce di farmaci per la gestione della malattia cardiaca.50
Pazienti sintomatici
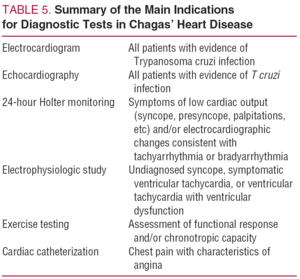
I pazienti con malattia cardiaca di Chagas sintomatica (Tabella 1) dovrebbero essere considerati a maggior rischio di morte improvvisa. Sintomi aspecifici come debolezza o barcollamento hanno molto più significato in questo contesto in quanto potrebbero essere predittivi di un episodio di sincope. È importante ricordare che la morte improvvisa può spesso essere la prima manifestazione della malattia cardiaca di Chagas.51,52 La tabella 5 riassume le principali indicazioni per i test diagnostici nella valutazione della cardiopatia di Chagas.
Trattamento dei pazienti con cardiopatia di Chagas
Gestione della disfunzione ventricolare e dell’insufficienza cardiaca
In generale, la gestione di questi pazienti ha molto in comune con quella di altre malattie cardiache. Si deve anche tener conto del fatto che spesso vengono applicate alla cardiopatia di Chagas misure generali che non sono specificamente convalidate per l’uso in questa malattia. I β-bloccanti (con le precauzioni menzionate nel paragrafo seguente) e gli inibitori dell’enzima di conversione dell’angiotensina (ACEI) sono i farmaci raccomandati per l’uso nei pazienti con disfunzione ventricolare moderata o grave (frazione di eiezione 53
Ci sono peculiarità nella malattia cardiaca di Chagas che sono importanti da prendere in considerazione per la gestione terapeutica di questi pazienti:
La cardiopatia cronica di Chagas è associata ad un alto tasso di bradiaritmie (blocco atrioventricolare, disfunzione del nodo del seno, ecc.) Di conseguenza, farmaci come i glicosidi digitalici, i β-bloccanti, alcuni antagonisti dei canali del calcio e l’amiodarone devono essere usati con cautela, iniziando il trattamento a basse dosi e monitorando attentamente la possibile comparsa di complicazioni
I pazienti con insufficienza cardiaca refrattaria possono essere valutati come candidati al trapianto di cuore. Nonostante la descrizione di alcuni casi di riattivazione della malattia di Chagas, le serie di casi pubblicate mostrano risultati soddisfacenti e una migliore sopravvivenza in questi pazienti rispetto ai pazienti con cardiopatia ischemica o cardiomiopatia dilatativa idiopatica54
Non c’è indicazione per la cardiomioplastica o la chirurgia ricostruttiva in questa malattia
L’utilità della terapia di risincronizzazione in questi pazienti è ancora in discussione e i criteri ecocardiografici ed ECG dovrebbero essere usati per valutare il rischio. criteri ecocardiografici ed ECG dovrebbero essere usati per valutare la sua indicazione
Alcuni risultati preliminari non pubblicati sono stati ottenuti sul miglioramento della funzione miocardica attraverso l’uso di cellule staminali in pazienti con malattia di Chagas
Gestione e prevenzione del tromboembolismo
L’alto tasso di eventi trombotici ed embolici dovrebbe essere preso in considerazione nei pazienti con malattia di Chagas. La maggior parte di questi eventi sono incidenti ischemici cerebrali e molti pazienti presentano cause cardiovascolari che spiegano il fenomeno, anche se ci sono altri fattori coinvolti.55,56
In uno studio condotto in Brasile, sono stati identificati 4 predittori di incidente cerebrovascolare embolico in pazienti con malattia cardiaca di Chagas sottostante: età superiore a 48 anni, anomalia primaria nella ripolarizzazione ventricolare, aneurisma apicale e frazione di eiezione ventricolare sinistra inferiore al 50%.57 La presenza di questi 4 predittori era associata a un’incidenza annuale di incidente cerebrovascolare del 4%. In assenza di prove più definitive, la prevenzione del tromboembolismo nei pazienti con cardiopatia cronica di Chagas dovrebbe comunque essere guidata dalle raccomandazioni cliniche standard: pazienti con fibrillazione atriale, precedenti eventi embolici e/o esistenza di trombi di parete. Il ruolo dei farmaci antiaggreganti nella prevenzione degli eventi tromboembolici deve ancora essere determinato.
Gestione delle bradiaritmie
Le bradiaritmie sintomatiche sono talvolta candidate all’impianto di un pacemaker. Le linee guida internazionali sull’impianto di pacemaker sono utili nei pazienti con la cardiopatia di Chagas.
Gestione delle aritmie ventricolari
I pazienti con la cardiopatia di Chagas presentano spesso extrasistoli ventricolari e tachicardie, più comunemente associate al danno miocardico che genera fenomeni di rientro. La maggior parte delle tachiaritmie ventricolari sostenute nei pazienti con cardiopatia di Chagas non derivano dall’aneurisma apicale del ventricolo sinistro ma piuttosto dalla regione inferolaterale.58,59
Poiché si tratta di un’anomalia progressiva con foci aritmogeni multipli, l’ablazione con radiofrequenza non dovrebbe essere considerata una tecnica di prima scelta.
Al contrario, e nonostante l’assenza di studi specifici nella cardiopatia cronica di Chagas, l’impianto di un defibrillatore cardioverter impiantabile è raccomandato per ridurre il rischio di morte improvvisa nelle seguenti situazioni:
Tachicardia ventricolare sostenuta. Inoltre, in questi pazienti si consiglia di somministrare empiricamente amiodarone nel tentativo di ridurre il tasso di scarica e abbassare la probabilità di tempesta elettrica. Se il paziente riceve troppe scariche nonostante questo trattamento, deve essere presa in considerazione l’ablazione con radiofrequenza60,61
Tachicardia ventricolare monomorfa sostenuta durante lo studio elettrofisiologico
La somministrazione di amiodarone è una possibilità nei pazienti con tachicardia ventricolare non sostenuta e studio elettrofisiologico normale (non inducibile).
Gestione del dolore anginoso
Il dolore al petto costituisce talvolta una manifestazione clinica della malattia cardiaca di Chagas e anche della malattia di Chagas esofagea. Si postula che il meccanismo fisiopatologico alla base di questo sintomo sia un’anormale microvasculatura miocardica.
Se il dolore al petto è il sintomo primario o predominante della cardiopatia di Chagas, la diagnosi differenziale dovrebbe includere la valutazione della cardiopatia ischemica associata mediante cateterismo cardiaco. La valutazione della perfusione miocardica con tecniche che impiegano isotopi radioattivi può essere utilizzata, anche se la loro utilità per la diagnosi differenziale del dolore anginoso è limitata dalla presenza di aree di fibrosi miocardica in pazienti con malattia cardiaca di Chagas. Non è disponibile alcun trattamento specifico per questi casi.
Trattamento etiologico nella malattia di Chagas cronica
È noto che nella fase cronica della malattia, il tasso di guarigione negli adulti varia dall’8% al 25%.62 La riduzione del titolo di anticorpi nel siero è usata come marker di guarigione, ma la lentezza con cui avvengono i cambiamenti sierologici, le possibili infezioni ripetute nelle aree endemiche e la mancanza di marcatori clinici hanno reso difficile determinare chiaramente l’efficacia del trattamento. Di conseguenza, e come risultato dei potenziali effetti avversi dei farmaci, non esiste un consenso internazionale sul trattamento eziologico in questa fase della malattia. Tuttavia, uno studio recente ha mostrato una riduzione della progressione della malattia di Chagas nei pazienti trattati con benznidazolo.63 Secondo il documento di consenso del 2005,26 i pazienti con test parassitologici positivi dovrebbero ricevere il trattamento eziologico e dovrebbe essere preso in considerazione per gli altri; si dovrebbe stabilire un accordo tra medico e paziente e fornire adeguate informazioni sui potenziali effetti avversi del farmaco.
Considerazioni aggiuntive
La malattia di Chagas dovrebbe essere sospettata in tutti i pazienti la cui storia è compatibile con l’epidemiologia della malattia e che hanno sintomi di coinvolgimento cardiaco. Le caratteristiche differenziali della malattia di Chagas, le limitate informazioni disponibili sulla malattia in Spagna e l’alto tasso di aritmie e di morte improvvisa come potenziali manifestazioni primarie della malattia rendono prioritaria la preparazione e la distribuzione di protocolli di diagnosi e trattamento per la cura di questi pazienti al fine di migliorare la comprensione della malattia da parte dei professionisti della salute coinvolti nella sua individuazione e gestione.
In alcuni contesti, le tecniche necessarie potrebbero non essere disponibili per una corretta diagnosi e trattamento dei pazienti con sospetta malattia di Chagas o malattia cardiaca di Chagas. Se un paziente con un’anamnesi compatibile con l’epidemiologia della malattia mostra segni e sintomi di malattia cardiaca, si raccomanda che l’individuo venga indirizzato a uno specialista in cardiologia e a un ospedale specializzato in malattie importati. In entrambi i casi, il rinvio non dovrebbe implicare che il medico di base, responsabile della valutazione iniziale del paziente, non ottenga una buona anamnesi ed esegua una valutazione clinica, un ECG convenzionale e una radiografia del torace prima di rinviare il paziente.
E’ chiaro che la gestione della malattia cardiaca cronica di Chagas è stata, e continua ad essere, un argomento di discussione scientifica nei paesi endemici. Per ulteriori informazioni, i lettori sono indirizzati ai rapporti di consenso della Società argentina di cardiologia e della Società brasiliana di cardiologia64,65 ; questi documenti sono disponibili in internet.
Il workshop sulla malattia di Chagas importata si è svolto il 6 e 7 marzo 2006 ed è stato finanziato dall’Agència de Gestió d’Ajuts Universitaris i de Recerca (AGAUR; 2005/ARCS2/00040) del Governo Regionale Catalano, dal Ministero spagnolo dell’Educazione e della Scienza (SAF-200524601-E) e dalla Rete di Medicina Tropicale del Fondo Spagnolo per la Ricerca Sanitaria (RICET). Diverse persone coinvolte nella preparazione del documento di consenso partecipano alla rete RICET e alla rete catalana per il monitoraggio epidemiologico delle malattie tropicali e importate (RIVEMTI).
Corrispondenza: Dr. J. Gascón.
Secció Medicina Tropical. Centro di Salute Internazionale. Hospital Clínic.
Villarroel, 170. 08036 Barcellona. España.
E-mail: [email protected]