INTRODUCCIÓN
La enfermedad de Chagas o tripanosomiasis americana es una parasitosis originada en el continente americano. Carlos Chagas describió la enfermedad a principios del siglo XX y sigue representando uno de los retos más importantes de la salud pública en América Latina.
Las tendencias epidemiológicas de los últimos 20 años revelan claramente una reducción general de la transmisión vectorial debido a los programas de control y a las mejoras en las viviendas rurales, así como a la interrupción de la transmisión vectorial en Chile, Uruguay y, recientemente, Brasil, todo lo cual ha contribuido a reducir la incidencia de la enfermedad en todo el continente.1-3
En el medio natural, Trypanosoma cruzi se transmite a través de una variedad de especies de insectos triatominos, que actúan como vectores. Sin embargo, se han descrito otros mecanismos de transmisión no vectorial a través de productos sanguíneos, trasplante de órganos y transmisión vertical. En regiones donde la infección es endémica, también se ha descrito la transmisión oral a través de la ingestión de alimentos contaminados con heces de chinches infectadas.4,5
Actualmente, la enfermedad de Chagas afecta a entre 10 y 12 millones de individuos en todo el mundo.6 Su distribución geográfica se extiende desde el paralelo 40 norte, en el sur de América del Norte, hasta el paralelo 45 sur, en Argentina y Chile.7 La urbanización latinoamericana, que se intensificó en la segunda mitad del siglo XX, ha alterado el perfil epidemiológico de la enfermedad, y los movimientos migratorios desde los países endémicos han hecho que se diagnostique la enfermedad de Chagas en regiones en las que no es endémica.8,9
España se ha convertido en uno de los países europeos que más inmigrantes recibe de Latinoamérica. A 31 de diciembre de 2005, cerca de un millón de individuos procedentes de América Latina figuraban en los registros de extranjeros con tarjeta de identidad de residente en España,10 aunque los registros del padrón municipal del año 2005 indicaban cifras superiores (1 445 796 individuos). Unidades y servicios especializados en medicina tropical y salud internacional en España ya han comenzado a diagnosticar y tratar a individuos con la enfermedad.11
En la reciente reunión de la Organización Panamericana de la Salud en Montevideo se discutió esta situación y en su informe final se mencionaron las necesidades de los países que reciben inmigrantes de zonas endémicas para hacer frente a la enfermedad de Chagas y poder proporcionar un tratamiento adecuado a los individuos afectados, así como para prevenir la transmisión vertical y sanguínea de T cruzi.12
PATOGÉNESIS E HISTORIA NATURAL DE LAS ENFERMEDADES DEL CORAZÓN EN LA ENFERMEDAD DE CHAGAS
Después de la fase aguda de la infección, la enfermedad de Chagas no tratada entra en una fase crónica que inicialmente es asintomática o no se reconoce. Posteriormente, entre el 20% y el 30% de los pacientes desarrollan anomalías cardíacas (forma cardíaca), el 10% molestias digestivas (forma digestiva) o ambas (forma mixta), y menos del 5% de los pacientes desarrollan una forma neurológica de la enfermedad. El resto permanecerá asintomático, sin manifestaciones clínicas a lo largo de su vida.13
Debido a la gravedad potencial de las complicaciones cardíacas de la enfermedad y a su frecuencia, el segundo taller sobre la enfermedad de Chagas importada se centró en las características clínicas de la cardiopatía chagásica crónica y en los requisitos para su correcto diagnóstico, manejo y tratamiento. La patogénesis de la enfermedad no está clara, aunque los conocimientos actuales apuntan a una etiología mixta, en la que el parásito estaría directamente implicado en la producción de daño miocárdico14,15 y un fenómeno autoinmune asociado.16,17 Otros mecanismos patogénicos descritos incluyen alteraciones microvasculares y denervación autonómica.18-21
La cardiopatía de Chagas presenta ciertas características que la diferencian de otras afecciones cardíacas más frecuentes en España:
Es una enfermedad fibrótica que se localiza generalmente en la región posteroinferior y apical del ventrículo izquierdo, el nódulo sinusal y el sistema de conducción por debajo de la rama del haz, y da lugar a anomalías predominantemente segmentarias de la contractilidad
Es una miocardiopatía dilatada con tendencia a la formación de aneurismas, especialmente en la región apical
Tiene un potente potencial arritmogénico y son frecuentes las arritmias ventriculares, a menudo asociadas a bradiarritmias (de origen auriculoventricular o que surgen en el nodo sinusal)
Se asocia a una alta tasa de eventos tromboembólicos
Puede presentarse como dolor precordial, generalmente atípico aunque ocasionalmente puede simular una cardiopatía isquémica.
En el curso natural de la enfermedad, las anomalías cardíacas aparecen progresivamente alrededor de 20 a 30 años después de la infección.22 Sin embargo, entre el 5% y el 10% de los pacientes muestran una miocarditis durante la fase aguda que progresa rápidamente hacia una forma grave de cardiopatía chagásica.23,24 Con menor frecuencia, los pacientes que se encuentran en la fase crónica de la enfermedad, con una afectación cardíaca leve, pueden mostrar una exacerbación repentina con parasitemia intensa y síntomas de insuficiencia cardíaca aguda; los inmunosupresores también favorecen estas exacerbaciones.25
Evaluación de los pacientes con sospecha de enfermedad de Chagas y cardiopatía chagásica
Diagnóstico de la infección por T cruzi
El diagnóstico de la enfermedad de Chagas en España se abordó en el documento de consenso del primer taller sobre la enfermedad de Chagas importada26. En resumen, se basa en el cumplimiento de 2 criterios:
Antecedentes compatibles con la epidemiología de la enfermedad: los antecedentes del paciente deben incluir al menos 1 elemento que haya posibilitado la transmisión de T cruzi por alguna de las vías de infección descritas (individuos procedentes de zonas endémicas o hijos de madres procedentes de zonas endémicas; viajeros con estancias en regiones endémicas y con un estilo de vida que les ponga en riesgo de infección)
Diagnóstico microbiológico: se considera que los individuos están infectados cuando tienen un resultado positivo en parasitología o 2 resultados positivos con 2 técnicas serológicas que emplean antígenos diferentes. En caso de resultados ambiguos o inconsistentes, se debe utilizar una tercera técnica. Existen varias pruebas serológicas para el diagnóstico de la enfermedad de Chagas que utilizan diferentes técnicas (ensayo inmunoenzimático, ELISA modificado o ELISA con antígenos recombinantes, inmunofluorescencia, hemaglutinación indirecta e inmunocromatografía). La reacción en cadena de la polimerasa (PCR) es quizás la técnica más sensible para el análisis parasitológico de la enfermedad de Chagas crónica, pero su uso no elimina la necesidad de realizar pruebas serológicas
Examen cardíaco básico en pacientes con infección por T cruzi
Para descartar la afectación cardíaca en pacientes con infección por T cruzi, debe realizarse una anamnesis completa y una exploración física completa junto con electrocardiografía, radiografía de tórax y ecocardiografía. Los síntomas y signos de la cardiopatía chagásica que se observan en la exploración física son los mismos que los de la miocardiopatía en general y ninguno es característico de la enfermedad.
Antecedentes médicos
El objetivo principal de la anamnesis es detectar síntomas de una posible cardiopatía subyacente. La tabla 1 muestra los signos y síntomas que se asocian con mayor frecuencia a la cardiopatía por T cruzi. También es importante evaluar los trastornos digestivos (disfagia, estreñimiento, etc.), ya que a veces pueden coexistir ambas formas.

Cuando se realiza la historia del paciente, es importante recordar que las diferencias lingüísticas y culturales pueden interferir en la comunicación entre el paciente y el médico. En ocasiones, los pacientes no aplican el mismo significado a determinadas palabras (por ejemplo, los términos utilizados en español para referirse a la disnea , los mareos o las palpitaciones ) y puede ser necesario definir a qué se refiere en cada caso. Además, los inmigrantes suelen sufrir dificultades de adaptación, añoranza y trastornos del estado de ánimo relacionados con su situación social y familiar27 que pueden causar problemas para identificar con precisión el síntoma cardinal o el motivo de consulta. Por último, también hay que tener en cuenta las condiciones laborales desfavorables (largas jornadas de trabajo, miedo a perder el empleo, contratos ilegales, etc.), ya que suponen un obstáculo adicional para acudir a las citas programadas. Dado que la enfermedad es familiar para estos pacientes y les causa preocupación, la notificación de un resultado positivo para la infección o la enfermedad de Chagas requiere un cuidadoso proceso de comunicación a través del cual se construye la confianza.12 Los mediadores culturales desempeñan un papel importante en este proceso.
Examen físico
Se debe realizar un examen físico detallado con especial atención al sistema cardiovascular. Pueden aparecer soplos cardíacos debidos a la disfunción valvular como resultado de la dilatación de las cámaras. En fases más avanzadas, se observan los signos habituales de congestión e hipoperfusión periférica. La caquexia cardíaca también es un indicador de estadios más avanzados de la cardiopatía chagásica y tiene un alto valor pronóstico.
Electrocardiograma
En todos los pacientes con infección por T cruzi debe realizarse un electrocardiograma (ECG) convencional de 12 derivaciones con un registro largo (30 segundos) en DII. En la fase crónica de la infección, las alteraciones del ECG aparecen varios años antes de los síntomas y la cardiomegalia (Tabla 2). Aunque no existe un patrón característico en el ECG, estas alteraciones, especialmente el bloqueo de rama derecha, de forma aislada o asociado a hemibloqueo anterior izquierdo en pacientes con serología positiva, pueden considerarse indicadores de cardiopatía chagásica crónica28-30. No obstante, dada su falta de especificidad, el diagnóstico requiere confirmación, ya que su presencia no significa necesariamente etiología chagásica.

Un ECG normal descarta la presencia de disfunción ventricular izquierda moderada o grave, con un valor predictivo negativo cercano al 100%: En cambio, cuanto mayor es el número de alteraciones del ECG, peor es la función ventricular.31
Las alteraciones de la conducción intraventricular y el ensanchamiento del complejo QRS aparecen de forma precoz en la cardiopatía chagásica crónica, cuando aún no están presentes las anomalías de la contracción miocárdica, por lo que carecen del valor pronóstico que muestran en otras cardiopatías.32
Radiografía de tórax
La radiografía de tórax tiene una baja sensibilidad para la detección de la cardiopatía chagásica, ya que puede producirse una disfunción ventricular mientras se obtiene una radiografía normal. Sin embargo, la evidencia de cardiomegalia podría ser predictiva de muerte súbita en pacientes con enfermedad de Chagas crónica.33 Debe realizarse con el paciente en situación clínica compensada, valorando como signos positivos la hipertensión venocapilar, la dilatación de las cámaras o un índice cardiotorácico superior a 0,6.
Ecocardiografía
Dado que la ecocardiografía es una técnica no invasiva ampliamente disponible y muy útil para la valoración de la función ventricular, todos los pacientes con enfermedad de Chagas son candidatos a un ecocardiograma de base.
Las alteraciones ecocardiográficas más frecuentes se resumen en la Tabla 3.34,35 Las siguientes recomendaciones son útiles para la realización de la ecocardiografía:

Es aconsejable realizar un examen de ecocardiografía transtorácica convencional, siguiendo un sistema específico.
1. Utilizar un transductor de alta frecuencia.
2. Obtener un ecocardiograma transversal (para el análisis segmentario de la región inferoposterior), una vista apical de 2 cámaras y vistas intermedias entre 2 y 4 cámaras, para detectar posibles aneurismas apicales.
3. Debe prestarse especial atención a la región posteroinferior del ventrículo izquierdo, incluyendo el ápex cardíaco, en un esfuerzo por identificar hipocinesia o acinesia segmentaria, junto con aneurismas apicales. También es frecuente observar hiperecogenicidad y retracción de la pared, similar a la descrita en la cardiopatía isquémica; esto es un sustrato para el desarrollo de arritmias ventriculares reentrantes.
4. Se recomienda prestar especial atención a la búsqueda de contraste ecográfico espontáneo y a la existencia de trombos en las cámaras.
5. Evaluar específicamente la función diastólica y la función ventricular derecha en todos los pacientes con sospecha de cardiopatía de Chagas. La alteración de la función diastólica del ventrículo izquierdo se produce de forma temprana en la enfermedad de Chagas y su gravedad suele correlacionarse con el grado de disfunción sistólica.36,37
6. El examen transesofágico está indicado cuando la ventana transtorácica no permite evaluar las cámaras izquierdas.
La reducción de la fracción de eyección del ventrículo izquierdo, el aumento del diámetro telesistólico y un patrón de flujo mitral restrictivo son los mejores indicadores pronósticos obtenidos por ecocardiografía en pacientes con cardiopatía de Chagas.38,39
En estadios avanzados de la enfermedad, cuando hay insuficiencia cardíaca congestiva, el perfil ecocardiográfico predominante consiste en una hipocinesia biventricular difusa con agrandamiento de las 4 cámaras.
Otros exámenes cardiológicos en pacientes con sospecha de cardiopatía de Chagas
Además de los estudios básicos mencionados, otros exámenes complementarios pueden ser útiles en determinados pacientes o circunstancias:
Monitorización Holter de 24 horas
Se recomienda la monitorización Holter de 24 horas en pacientes con los siguientes síntomas:
Síntomas sugestivos de arritmia cardíaca (síncope, presíncope o palpitaciones)
La presencia de ciertas arritmias cardíacas en el ECG, como bradiarritmias sinusales (con una frecuencia cardíaca media inferior a 40 latidos por minuto y/o pausas sinusales prolongadas), bloqueos auriculoventriculares de segundo grado, y extrasístoles ventriculares frecuentes y/o repetitivas (ráfagas)
La monitorización Holter de 24 horas permitirá evaluar la posible asociación de los síntomas con una arritmia, identificar a los pacientes con riesgo de muerte súbita e identificar la disfunción autonómica.33,40 Se registran episodios de taquicardia ventricular no sostenida en aproximadamente el 90% de los pacientes con cardiopatía de Chagas y disfunción ventricular o insuficiencia cardíaca.41
La monitorización Holter debe realizarse con una técnica convencional, preferiblemente con un sistema de 3 canales. La sensibilidad del registro Holter es baja cuando los episodios de arritmia son poco frecuentes y en estos casos se pueden utilizar otras técnicas como el Holter implantable.
Estudio electrofisiológico
El objetivo de un estudio electrofisiológico en estos pacientes es identificar las anomalías de la conducción auriculoventricular e intraventricular y valorar la inducción de arritmias ventriculares malignas. Las indicaciones son las mismas que para la evaluación de otros trastornos con riesgo de muerte súbita:
Pacientes con síntomas sugestivos de arritmia (síncope o presíncope) no confirmados en estudios previos
Taquicardia ventricular sostenida, con o sin síntomas, independientemente del grado de función ventricular
Paciente reanimado de muerte súbita
Pacientes que presentan alteraciones en el ECG o en la monitorización Holter que se asocian a un mayor riesgo de muerte súbita: extrasístoles ventriculares repetidas o pareadas, episodios de taquicardia ventricular no sostenida y aumento de la extensión del intervalo QT asociado a la presencia de disfunción ventricular.42 En este subconjunto de pacientes, si no es posible realizar un estudio electrofisiológico, se puede administrar amiodarona de forma empírica siempre que no existan contraindicaciones.
Prueba de esfuerzo
La prueba de esfuerzo estaría indicada principalmente en los siguientes casos:
Evaluación de la capacidad funcional
Evaluación de la respuesta cronotrópica
En presencia de dolor torácico y cardiopatía de Chagas, la prueba de esfuerzo es poco útil para determinar la etiología del dolor; en esos casos debe realizarse una angiografía coronaria
La angiografía coronaria
Está indicada según los criterios de la Sociedad Española de Cardiología,43 teniendo en cuenta las consideraciones sobre la prueba de esfuerzo.
Biopsia miocárdica
La biopsia miocárdica no se considera actualmente una técnica diagnóstica en la cardiopatía de Chagas como consecuencia de su riesgo y limitada especificidad.
MANEJO DE PACIENTES CON INFECCIÓN POR T CRUZI
Pacientes asintomáticos con electrocardiograma y radiografía de tórax normales
El riesgo de cardiopatía chagásica es mayor durante la segunda y tercera décadas tras la infección.44 En los pacientes con evidencia de infección por T. cruzi y con un ECG normal o con anomalías mínimas no sugestivas de cardiopatía chagásica crónica, el riesgo anual de progresión a cardiopatía es de entre el 2% y el 5%.45,46 En consecuencia, se recomienda la realización de un ecocardiograma de referencia.
Pacientes asintomáticos con anomalías en el ECG
Se recomienda la realización de un ecocardiograma de referencia en pacientes asintomáticos con anomalías en el ECG. Los hallazgos son muy variables, y la disfunción ventricular izquierda (fracción de eyección inferior al 40%) se detecta en aproximadamente el 30% de los casos. La tabla 4 muestra la prevalencia de la disfunción ventricular izquierda según el patrón del ECG.47 En general, el pronóstico viene determinado por el grado de disfunción ventricular.48
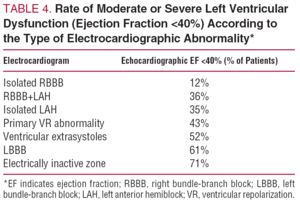
La frecuencia con la que se debe repetir la ecocardiografía dependerá del estado clínico del paciente. Aunque los estudios no están disponibles, la progresión de la enfermedad es lenta en pacientes asintomáticos con un ecocardiograma normal; en consecuencia, es suficiente repetir la evaluación dentro de los 5 años siguientes en este grupo, mientras no aparezcan síntomas. Cuando el estudio inicial revela anomalías debe repetirse en un periodo de 1 a 3 años, debido al mayor riesgo de progresión,49 especialmente si existe una disfunción ventricular significativa (fracción de eyección inferior al 40%). En cualquier paciente, la aparición de nuevos síntomas o anomalías en el ECG debe considerarse una indicación para realizar un nuevo ecocardiograma.
El objetivo del seguimiento ecocardiográfico es identificar a los pacientes con disfunción moderada o grave, que a menudo siguen siendo asintomáticos pero que podrían beneficiarse del suministro precoz de fármacos para el manejo de la cardiopatía.50
Pacientes sintomáticos
Los pacientes con cardiopatía de Chagas sintomática (tabla 1) deben considerarse con mayor riesgo de muerte súbita. Síntomas tan inespecíficos como la debilidad o el tambaleo tienen mucha más importancia en este contexto, ya que podrían ser predictivos de un episodio de síncope. Es importante recordar que la muerte súbita puede ser a menudo la primera manifestación de la cardiopatía de Chagas.51,52 La tabla 5 resume las principales indicaciones de las pruebas diagnósticas en la evaluación de la cardiopatía de Chagas.
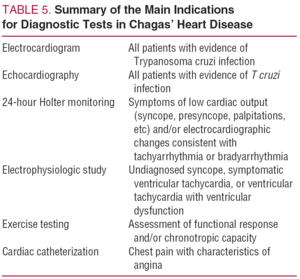
Tratamiento de los pacientes con cardiopatía de Chagas
Manejo de la disfunción ventricular y la insuficiencia cardíaca
En general, el manejo de estos pacientes tiene mucho en común con el de otras cardiopatías. También hay que tener en cuenta que a menudo se aplican medidas generales a la cardiopatía de Chagas que no están específicamente validadas para su uso en esta enfermedad. Los β-bloqueantes (con las precauciones que se mencionan en el párrafo siguiente) y los inhibidores de la enzima convertidora de angiotensina (IECA) son los fármacos recomendados para su uso en pacientes con disfunción ventricular moderada o grave (fracción de eyección 53
Existen peculiaridades en la cardiopatía chagásica que es importante tener en cuenta para el manejo terapéutico de estos pacientes:
La cardiopatía chagásica crónica se asocia a una elevada tasa de bradiarritmias (bloqueo auriculoventricular, disfunción del nodo sinusal, etc). En consecuencia, fármacos como los glucósidos digitálicos, los β-bloqueantes, algunos antagonistas de los canales del calcio y la amiodarona deben utilizarse con cuidado, iniciando el tratamiento a dosis bajas y vigilando cuidadosamente la posible aparición de complicaciones
Los pacientes con insuficiencia cardíaca refractaria pueden ser valorados como candidatos a trasplante cardíaco. A pesar de la descripción de algunos casos de reactivación de la enfermedad de Chagas las series de casos publicadas muestran resultados satisfactorios y una mejor supervivencia en estos pacientes en comparación con los pacientes con cardiopatía isquémica o miocardiopatía dilatada idiopática54
No hay indicación de cardiomioplastia ni de cirugía reconstructiva en esta enfermedad
La utilidad de la terapia de resincronización en estos pacientes está aún en discusión y los criterios ecocardiográficos y ECG para valorar su indicación
Se han obtenido algunos resultados preliminares no publicados sobre la mejora de la función miocárdica mediante el uso de células madre en pacientes con enfermedad de Chagas
Manejo y prevención del tromboembolismo
La alta tasa de eventos trombóticos y embólicos debe tenerse en cuenta en los pacientes con enfermedad de Chagas. La mayoría de estos eventos son accidentes isquémicos cerebrales y muchos pacientes presentan causas cardiovasculares que explican el fenómeno, aunque hay otros factores implicados.55,56
En un estudio realizado en Brasil, se identificaron 4 predictores de accidente cerebrovascular embólico en pacientes con cardiopatía de Chagas subyacente: edad superior a 48 años, anormalidad primaria en la repolarización ventricular, aneurisma apical y fracción de eyección del ventrículo izquierdo inferior al 50%.57 La presencia de estos 4 predictores se asoció con una incidencia anual de accidente cerebrovascular del 4%. A falta de pruebas más definitivas, la prevención de la tromboembolia en los pacientes con cardiopatía crónica de Chagas debe guiarse, no obstante, por las recomendaciones clínicas habituales: pacientes con fibrilación auricular, eventos embólicos previos y/o existencia de trombos murales. El papel de los fármacos antiplaquetarios en la prevención de eventos tromboembólicos está aún por determinar.
Manejo de las bradiarritmias
Las bradiarritmias sintomáticas son a veces candidatas a la implantación de un marcapasos. Las directrices internacionales sobre la implantación de marcapasos son útiles en los pacientes con cardiopatía de Chagas.
Manejo de las arritmias ventriculares
Los pacientes con cardiopatía de Chagas suelen presentar extrasístoles ventriculares y taquicardias, más comúnmente asociadas a un daño miocárdico que genera fenómenos de reentrada. La mayoría de las taquiarritmias ventriculares sostenidas en pacientes con cardiopatía de Chagas no surgen del aneurisma apical del ventrículo izquierdo, sino de la región inferolateral.58,59
Puesto que se trata de una anomalía progresiva con múltiples focos arritmogénicos, la ablación por radiofrecuencia no debe considerarse una técnica de primera elección.
En cambio, y a pesar de la ausencia de estudios específicos en la cardiopatía de Chagas crónica, se recomienda la implantación de un desfibrilador cardioversor implantable para reducir el riesgo de muerte súbita en las siguientes situaciones:
Taquicardia ventricular sostenida. Además, en estos pacientes se aconseja la administración empírica de amiodarona en un esfuerzo por reducir la tasa de descargas y disminuir la probabilidad de tormenta eléctrica. Si el paciente recibe demasiadas descargas a pesar de este tratamiento, debe considerarse la ablación por radiofrecuencia60,61
La taquicardia ventricular sostenida monomorfa durante el estudio electrofisiológico
La administración de amiodarona es una posibilidad en pacientes con taquicardia ventricular no sostenida y estudio electrofisiológico normal (no inducible).
Manejo del dolor anginoso
El dolor torácico constituye a veces una manifestación clínica de la cardiopatía chagásica e incluso de la enfermedad de Chagas esofágica. Se postula que el mecanismo fisiopatológico subyacente a este síntoma es la microvasculatura miocárdica anormal.
Si el dolor torácico es el síntoma principal o predominante de la cardiopatía chagásica, el diagnóstico diferencial debe incluir la evaluación de la cardiopatía isquémica asociada mediante cateterismo cardíaco. Puede utilizarse la evaluación de la perfusión miocárdica con técnicas que emplean isótopos radiactivos, aunque su utilidad para el diagnóstico diferencial del dolor anginoso está limitada por la presencia de áreas de fibrosis miocárdica en los pacientes con cardiopatía de Chagas. No se dispone de un tratamiento específico para estos casos.
Tratamiento etiológico en la enfermedad de Chagas crónica
Se sabe que en la fase crónica de la enfermedad, la tasa de curación en adultos oscila entre el 8% y el 25%.62 La reducción del título de anticuerpos séricos se utiliza como marcador de curación, pero la lentitud con la que se producen los cambios serológicos, las posibles infecciones de repetición en zonas endémicas y la falta de marcadores clínicos han dificultado la determinación clara de la eficacia del tratamiento. En consecuencia, y como resultado de los posibles efectos adversos de la medicación, no existe un consenso internacional sobre el tratamiento etiológico en esta fase de la enfermedad. Sin embargo, un estudio reciente mostró una reducción de la progresión de la enfermedad de Chagas en pacientes tratados con benznidazol.63 Según el documento de consenso de 200526 , los pacientes con pruebas parasitológicas positivas deben recibir tratamiento etiológico y debe considerarse para los demás; debe establecerse un acuerdo entre el médico y el paciente y proporcionarse información adecuada sobre los posibles efectos adversos del fármaco.
CONSIDERACIONES ADICIONALES
La enfermedad de Chagas debe sospecharse en todos los pacientes cuyos antecedentes sean compatibles con la epidemiología de la enfermedad y que presenten síntomas de afectación cardíaca. Las características diferenciales de la cardiopatía chagásica, la escasa información disponible sobre la enfermedad en España, y la elevada tasa de arritmias y muerte súbita como potenciales manifestaciones primarias de la enfermedad, hacen prioritaria la elaboración y difusión de protocolos de diagnóstico y tratamiento para la atención de estos pacientes, con el fin de mejorar el conocimiento de la enfermedad por parte de los profesionales sanitarios implicados en su detección y manejo.
En algunos entornos puede no disponerse de las técnicas necesarias para el correcto diagnóstico y tratamiento de los pacientes con sospecha de enfermedad de Chagas o cardiopatía chagásica. Si un paciente con antecedentes compatibles con la epidemiología de la enfermedad presenta signos y síntomas de cardiopatía, se recomienda remitirlo a un especialista en cardiología y a un hospital especializado en enfermedades importadas. En ambos casos, la derivación no debe implicar que el médico de atención primaria, responsable de la evaluación inicial del paciente, no obtenga una buena historia clínica y realice una evaluación clínica, un ECG convencional y una radiografía de tórax antes de derivar al paciente.
Claramente, el manejo de la cardiopatía chagásica crónica ha sido, y sigue siendo, un tema de discusión científica en los países endémicos. Para más información, se remite al lector a los informes de consenso de la Sociedad Argentina de Cardiología y de la Sociedad Brasileña de Cardiología64,65; estos documentos están disponibles en Internet.
El taller sobre la enfermedad de Chagas importada tuvo lugar los días 6 y 7 de marzo de 2006 y fue financiado por la Agència de Gestió d’Ajuts Universitaris i de Recerca (AGAUR; 2005/ARCS2/00040) de la Generalitat de Catalunya, el Ministerio de Educación y Ciencia (SAF-200524601-E) y la Red de Medicina Tropical del Fondo Español de Investigación Sanitaria (RICET). Varias personas implicadas en la elaboración del documento de consenso participan en la red RICET y en la Red Catalana de Vigilancia Epidemiológica de Enfermedades Tropicales e Importadas (RIVEMTI).
Correspondencia: Dr. J. Gascón.
Secció Medicina Tropical. Centre de Salut Internacional. Hospital Clínic.
Villarroel, 170. 08036 Barcelona. España.
Correo electrónico: [email protected]