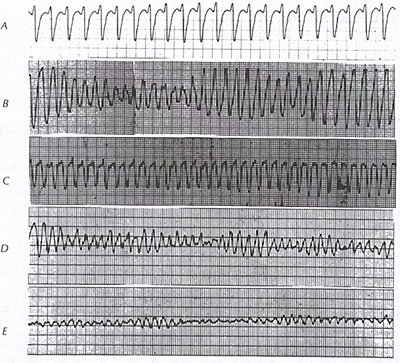
La fibrillazione ventricolare (vedi figura 9B) è un’aritmia terminale, che richiede uniformemente un rapido inizio delle misure di emergenza.
Il flutter ventricolare (vedi figura 9B) con perdita di coscienza e VT instabile rapido può essere clinicamente equivalente alla VF e viene trattato in modo identico quando è accompagnato dal quadro clinico dell’arresto cardiaco. La fibrillazione ventricolare si verifica comunemente nel contesto di eventi ischemici acuti (vedi figura 70) o imprevedibilmente nella cardiopatia ischemica cronica avanzata. Inoltre, è la modalità di morte nel 25-50% dei decessi tra i pazienti con cardiomiopatie (vedi figure 39A, 39B, 39C, 39D, 39E, 39F, 39G, 43B, 73, 74, 75, 76, 77A, 77B). Può anche svilupparsi durante l’ipossia, la fibrillazione atriale con risposte ventricolari rapide nella sindrome WPW (vedi figura 3A, 3B), pacing R-on-T o cardioversione, o messa a terra impropria di dispositivi elettrici o come effetti proaritmici (vedi figura 13) di farmaci antiaritmici. Un ambiente a rischio particolarmente elevato per la VF è l’infarto miocardico acuto con blocco di branca destro o sinistro.
La fibrillazione ventricolare può verificarsi de novo, ma tra i pazienti con arresto cardiaco extraospedaliero, la VT precede comunemente l’insorgenza della VF. L’arteria coronaria destra è un sito comune di spasmo coronarico isolato che porta all’arresto cardiaco dovuto alla fibrillazione ventricolare (figura 9d).
Il modello elettrocardiografico della VF è quello di una grossolana disorganizzazione senza forme d’onda o intervalli ripetitivi identificabili (vedi figura 9B). All’inizio, la VF può avere un andamento “grossolano”, ma col tempo, perde la sua ampiezza e diventa “fine” (
MALFUNZIONAMENTO DEI DEFIBRILLATORI CARDIOVERTORI INTERNI
Ci sono dispositivi attualmente disponibili, che incorporano sia il pacemaker (stimolazione VVI) che il defibrillatore cardioverter impiantabile per trattare quei pazienti con una storia di bradicardia sinusale cronica, malattia del sistema di conduzione A-V o gravi bradiaritmie postshock.
Il malfunzionamento dell’ICD può essere causato da frattura o migrazione dell’elettrocatetere, esaurimento prematuro della batteria e malfunzionamento del generatore.
Tutte le unità di solito sono modificate temporaneamente posizionando un magnete sopra il generatore di impulsi.
Le scariche appropriate e indesiderabili possono a volte essere difficili da distinguere dagli shock appropriati e desiderabili (la fibrillazione atriale con una rapida frequenza ventricolare che supera il cutoff della frequenza programmata può innescare una scarica appropriata (anche se indesiderabile) e può spiegare le scariche ripetitive sperimentate in stretta successione.
I dispositivi con caratteristiche di second look che richiedono la riconferma dell’aritmia immediatamente prima dell’erogazione dello shock hanno in gran parte eliminato il problema delle scariche indesiderate dovute a tachicardia ventricolare non sostenuta.
L’interruzione dell’elettrocatetere può essere diagnosticata sulla base dei risultati dei raggi x sovrapentrati, analizzando i toni udibili emessi in sincronia con gli eventi rilevati, o esaminando le registrazioni telemetrate degli elettrogrammi intracardiaci memorizzati o in tempo reale.La scarica durante il ritmo sinusale è fortemente evidente per il malfunzionamento del rilevamento.L’analisi degli elettrogrammi o degli intervalli di frequenza registrati dai dispositivi più recenti durante il ritmo sinusale e al momento della terapia ha permesso una migliore correlazione tra gli eventi aritmici e le risposte del dispositivo e ha notevolmente facilitato la diagnosi di malfunzionamento dell’elettrocatetere o del generatore di impulsi.
Nel sospetto di malfunzionamento del pacemaker nei casi con il pacer così come con l’ICD, devono essere prese lunghe strisce di diversi elettrocateteri ECG.L’ECG deve essere registrato nelle modalità base (sincrona) e magnete (asincrona).A causa dei ritmi competitivi quando si usa un magnete, la maggior parte dei produttori usa una frequenza del magnete tra 90 e 100 impulsi al minuto per annullare i ritmi spontanei.Con i sistemi di stimolazione a camera singola, l’ECG nelle modalità sincrona o asincrona dovrebbe confermare una stimolazione normale, l’artefatto di stimolo del sistema di elettrocateteri bipolare è spesso impossibile da vedere sull’ECG di superficie.Per la conferma del rilevamento del pacemaker in pazienti con pacing coerente, il paziente può essere esercitato per accelerare il tasso intrinseco o il tasso di pacing ridotto dalla programmazione fino a quando il tasso intrinseco emerge.
Il generatore di impulsi in fuga del pacemaker è un problema raro (riferendosi a un aumento del tasso di pacing oltre 150 impulsi/minuto con uscita sufficiente per catturare il cuore).