

ジョン・ダルトンの原子論は近代化学の基礎を築いた。
John Dalton’s Early Life and Education
John Daltonは1766年9月6日にイギリスのEaglesfieldで生まれた。
彼の両親は共にクエーカー教徒であった。 クエーカーはキリスト教徒であったが、既成の英国国教会からは異教徒とみなされた。
父親は織物商で、家とわずかな土地を所有していた。
ジョン・ドルトンは知的な子供で、周囲の世界に興味を持ち、何事もできる限り学ぼうとした。
11歳まで村の学校に通い、その後教師として手伝い始めた。
15歳のとき、兄ジョンが自宅から40マイル離れたケンダルの町でクエーカーの寄宿学校を経営するのを手伝い始めた。 その間、彼は独学で科学、数学、ラテン語、ギリシャ語、フランス語を学び続けた。
学校の生徒たちは、ダルトンに教わることを楽しんでいたようで、生徒の一人は次のように回想している:
「少年たちはみなジョン・ダルトンに教わることを喜んでいた、なぜなら彼はより優しい性格であり、しかも彼の心は数学でいっぱいで、彼らの欠点には気づいていなかった。「
Becoming a Scientist
1793年の前半、26歳のドルトンはマンチェスターのニューカレッジという反対派の大学で数学と自然哲学の教師の職を得た。
これは、色覚異常について論じた史上初の論文であった。 ダルトンは、自分や家族が色覚異常であったことから、この症状が遺伝性のものであることに気づいていた。 この後、熱伝導、熱による気体の膨張、光の性質、オーロラ、気象学など、物理学の研究論文を発表している。
1800年、ダルトンは財政難のニューカレッジを辞し、科学と数学の個人教師を始めた。
原子論
気体の挙動
1801年にマンチェスターで一連の講義を行い、1802年に内容が出版された。 この講義の中で、彼は気体や液体について行っていた研究を発表した。
まず、ダルトンは、温度が十分に低く、圧力が十分に高ければ、すべての気体が液化することを疑う余地がないことを正しく述べている。
そして彼は、容器の中で体積が一定に保たれているとき、気体の圧力はその温度に直接比例して変化すると述べた。
これは、1809年にそれを発表したジョセフ・ゲイ=リュサックにちなんで名付けられたゲイ=リュサックの法則として、最終的に知られるようになったものの最初の公式声明であった。
1803年には、ダルトンが「分圧の法則」を発表し、今でも大学の化学の学生なら誰でも使っている。これは、反応しない気体の混合物では、全ガス圧は個々の気体の分圧の和に等しいというものだ。
ダルトンの研究は、彼を第一級の科学者として際立たせ、ロンドンの王立研究所に招かれて講義を行った。
ダルトンと原子
気体の研究により、ダルトンはこれらの見えない物質は実際に何からできているかを考えるようになった。
原子という考えは、2000年以上前に古代ギリシャのデモクリトスによって初めて提案された。 デモクリトスは、すべてのものは原子という小さな粒子でできていて、この原子は小さな粒子に分裂することはないと考えていた。 果たしてデモクリトスは正しかったのだろうか? 誰も知らなかった!
ダルトンは今、この2000年前の謎を解こうとしていたのです。
彼は数え切れないほどの化学反応を行い、1808年に『A New System of Chemical Philosophy』という本の中で、現在我々が「ドルトンの法則」と呼ぶものを発表した:
もし2つの要素がそれらの間で複数の化合物を形成するなら、最初の要素の一定の質量と結合する2番目の要素の質量比は小さな整数の比となるだろう。
たとえば、ダルトンは、12グラムの炭素が16グラムの酸素と反応して、現在私たちが一酸化炭素と呼ぶ化合物を形成できることを見いだした。
この32:16という比率は、単純化して2:1となり、ドルトンは興味をそそられた。
収集したすべてのデータを分析し、ダルトンは物質が原子として存在するという信念を述べました。 彼はデモクリトスよりもさらに踏み込んで、異なる元素の原子は異なる質量を持つことを明言した。 例えば、
1. 原子が結合して分子を形成する方法
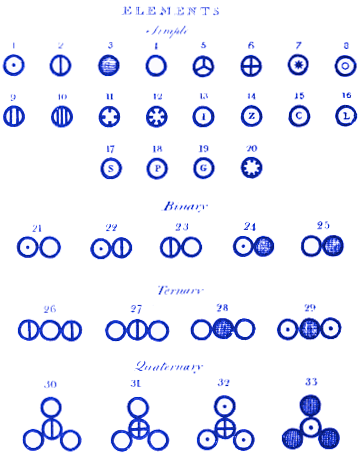

図の一番上で、ドルトンは原子1を水素、2窒素、3炭素、4酸素、5リンなどと割り当てています。 例えば、分子21は水(OH)、22はアンモニア(NH)、23は窒素酸化物(NO)である。 現代の読者は、ダルトンが分子21と22を間違えていることに気がつくだろう。 このことは、ダルトンの原子・分子体系が、現代の我々が表現しうるものとほとんど同じであることより重要ではない。 例えば、ドルトンの分子28は二酸化炭素である。
Amedeo AvogadroはすぐにDaltonの研究を基に、Daltonの誤りをいくつか訂正した研究を発表した。例えばAvogadroは水はH20と書くべきであると言った。
2 氷の中で水の分子はどう見えるか
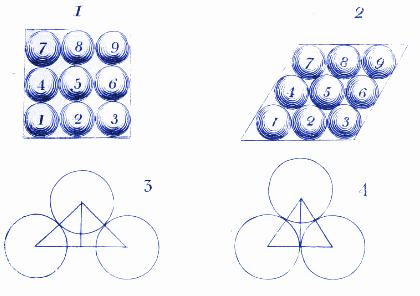

ここでドルトンは、水の分子が氷の中で凍ったときにどう配列するかを示している。 今日では、結晶の中で原子や分子がどのように配列するかを示すために、同様の図を使っています。 元素は原子からできており、原子は目に見えないほど小さな粒子である。
2. 特定の元素の原子はすべて同一である。
3. 異なる元素の原子は異なる性質を持つ。質量が異なり、化学反応も異なる。
4. 原子は生成、破壊、分割できない。
5. 化学反応において、原子は互いに結びついたり、離れたりする。
6. 原子は単純な整数比で結合して化合物を形成する。
同じ元素の原子が異なる質量を持ち(同位体)、核反応で分割できることを学んだが、ダルトンの原子論のほとんどは、彼がそれを記述してから200年以上たった今日も有効である。 8722>
 「ダルトン氏の永久的な名声は、化学の事実に普遍的に適用できる単純な原理を発見したこと、すなわち物体が結合する比率を確定し、将来の研究の基礎を築いたことにかかっているだろう…この点での彼の功績は天文学におけるケプラーの功績に似ている」。”
「ダルトン氏の永久的な名声は、化学の事実に普遍的に適用できる単純な原理を発見したこと、すなわち物体が結合する比率を確定し、将来の研究の基礎を築いたことにかかっているだろう…この点での彼の功績は天文学におけるケプラーの功績に似ている」。”
Honors
Daltonは結婚せず、子供もいなかった。 1810年、王立協会会員への招待を辞退。 1822年、本人が知らないうちに選出されていた。 1826年、「原子論」で王立協会からメダルを授与される。
1833年、フランス科学アカデミーが彼を8人の外国人会員の一人に選出。 1834年、アメリカ芸術科学アカデミーが彼を外国人会員に選出した。
The End
71歳のとき、ダルトンは小さな脳卒中、つまり当時でいう麻痺を起こした。 その1年後、さらに大きな脳卒中が起こり、かつてのようにはっきりと話すことができなくなった。 1844年、77歳のときにも脳卒中に襲われた。 1844年7月27日、77歳で死去。
彼の科学的評価は非常に高く、彼の遺体がマンチェスター・タウンホールに安置されると、4万人以上の人々が敬意を払って訪れた。 ジョン・ダルトンはマンチェスターのアードウィック墓地に葬られた。