化学元素コバルトは、移行金属として分類されています。 1735年にジョージ・ブラントによって発見されました。

Data Zone
| 分類されます。 | コバルトは遷移金属 |
| 色: | 青白い |
| 原子量: | 58.9332 |
| 状態: | 固体 |
| 融点: | 1495 oC, 1768 K |
| 沸点.沸点.沸点: | |
| 固体 | |
| 状態.融点: | |
| 2930 oC, 3203 K | |
| 電子: | 27 |
| プロトン: | 27 |
| 最も豊富な同位体の中性子: | 32 |
| 電子の殻。 | 2,8,15,2 |
| 電子配置: | 3d7 4s2 |
| 密度 @ 20oC: | 8.90 g/cm3 |
もっと表示する。 熱、エネルギー、酸化、反応、
化合物、半径、導電率
| 原子容積: | 6.7 cm3/mol | |
| 構造: | hcp: hexagonal close pkd | |
| 硬度: | 5.0 mohs | |
| 比熱 | ||
| 融解熱 | 16.190 kJ mol-1 | |
| 霧化熱 | ||
| 蒸発熱 | 熱膨張係数 | 熱分解熱 |
| 熱分解熱 | ||
| 第1イオン化エネルギー | 758.3 kJ mol-1 | |
| 第1イオン化エネルギー | 758.3 kJ mol-14 kJ mol-1 | |
| 第2イオン化エネルギー | 1646 kJ mol-1 | |
| 第3イオン化エネルギー | 3232.3 kJ mol-1 | |
| 第1イオン化エネルギー | 32.3 kJ mol-1 | |
| 電子親和力 | 63.8 kJ mol-1 | |
| 最小酸化数 | -1 | |
| 最小一般酸化数 | ||
| 電子親和力<1973> | 電子親和力-1 | 0 |
| 最大酸化数 | 5 | |
| 最大共通酸化数 | 3 | |
| 電気陰性度(ポーリングスケール) | 1.0 | 2.0 | 1.0 |
| 1.088 | ||
| 分極率体積 | 7.5Å3 | |
| 空気との反応 | 穏やか、w/ht ? Co3O4 | |
| 15M硝酸との反応 | 活発、 ? Co(NO3)2, NOx | |
| 6M塩酸との反応 | マイルド、? H2, CoCl2 | |
| 6MのNaOHとの反応 | – | |
| オキサイド(s) | CoO, Co3O4 | |
| 水素化物(単体) | なし | |
| 塩化物(単体) | CoCl2 | |
| 原子レベル 半径 | 135 pm | |
| イオン半径(1+イオン) | – | |
| イオン半径(2+イオン) | 83.0.8 pm | |
| イオン半径(3+イオン) | 71.8 pm | |
| イオン半径(1-イオン) | – | |
| イオン半径(2-イオン) | – | |
| イオン半径(3-イオン) | ||
| – | ||
| – | ||
| 熱伝導率 | 100 W m-1 K-1 | |
| 電気伝導率 | 17.9 x 106 S m-1 | |
| 凍結融点: | 1495 oC, 1768 K |
コバルトの発見
古くから、青ガラスやセラミックにコバルト化合物が使用されてきた。
この元素は1735年にスウェーデンの化学者ジョージ・ブラントによって初めて単離されました。 彼は、ガラスの青色を引き起こすのは、それまで考えられていたビスマスではなく、コバルトという元素の存在であることを示しました。
1741年頃、彼は「6種類の金属があるように、私は信頼できる実験によって…6種類のハーフメタルもあることを示した:水銀、ビスマス、亜鉛、アンチモンとヒ素のレグルスに加えて、新しいハーフメタル、すなわちコバルトレグルスだ」
コバルトという言葉はドイツ語でゴブリンや妖精という意味の「kobold」から来ています。


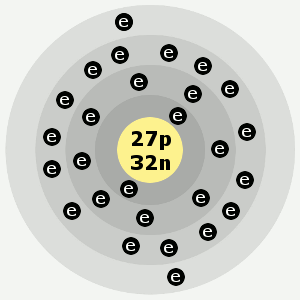
コバルトの電子殻
外観と性質
有害作用:
コバルトおよびその化合物は皮膚接触でわずかに、摂取で中程度の毒性があると考えられています。
特性:
コバルトは青白く光沢があり、硬くてもろい金属です。 強磁性です。
化学的に活性で、多くの化合物を形成します。
コバルトの用途
コバルトは航空機のエンジン部品の合金や、耐食性/耐摩耗性の用途の合金に使われます。
コバルトは電池や電気めっきに広く使用されています。
コバルト塩はガラスやセラミックに青や緑の色をつけるのに使われます。
放射性の60Coはがんの治療に使われます。
コバルトは多くの生物に不可欠で、ビタミンB12の成分です。
また、サマリウム-コバルト永久磁石に使用されます。
コバルトはサマリウム・コバルト永久磁石にも使われており、ギターのピックアップや高速モーターに使われています。
地殻の存在量:重量で25ppm、モルで8ppm
太陽系の存在量:重量で25ppm。 重量で100万分の4、モル数で100万分の0.7
コスト、純粋:100gあたり21ドル
コスト、バルク:100gあたり40ドル
源流。 コバルトは自然界に遊離元素として存在しません。 鉱石の中に含まれています。 コバルトの主な鉱石はコバルト酸塩(CoAsS)、エリスライト(コバルトの水和ヒ酸塩)、グラコド(Co,Fe)AsS、スクッテルダイト(Co,Ni)As3である。 コバルトは一般にニッケルや銅の採掘の副産物として産出されます。
同位体。 コバルトには半減期がわかっている同位体が22種類あり、質量数は50~72である。

- Edward Smedley, Hugh James Rose, Henry John Rose, Encyclopaedia Metropolitana; or Universal Dictionary of Knowledge…コバルトは、その安定同位体59コから構成されています。 1845, Volume 4, p693 William Clowes and Sons.
Cite this Page
Cite this Page
オンラインでのリンクは、以下のいずれかをコピー&ペーストしてください:
<a href="https://www.chemicool.com/elements/cobalt.html">Cobalt</a>
または
<a href="https://www.chemicool.com/elements/cobalt.html">Cobalt Element Facts</a>
学術文書でこのページを引用するには、以下のMLA準拠の引用文を使用してください:
"Cobalt." Chemicool Periodic Table. Chemicool.com. 16 Oct. 2012. Web. <https://www.chemicool.com/elements/cobalt.html>.