Zolang er substraat beschikbaar is om zich aan te binden, zal een toenemende enzymconcentratie de enzymatische reactie versnellen. Als al het substraat gebonden is, zal de reactie niet meer versnellen met de toenemende enzymconcentratie, omdat er dan niets meer is voor extra enzymen om zich aan te binden.
Hoe werken enzymen?
Enzymen zijn katalytische eiwitten die de chemische reactie kunnen versnellen zonder tijdens het reactieproces te worden veranderd. In het reactieproces wordt er geen binding gevormd tussen het enzym en het substraat, zodat het enzym zijn oorspronkelijke vorm weer aanneemt en opnieuw kan worden gebruikt. Het enzym bindt zich via de actieve site aan het substraat om een enzym-substraatcomplex te vormen. Het enzym is zeer specifiek in de reactie en ook voor het substraat waarmee het bindt. Wanneer de vorm van het substraat overeenkomt met de actieve site van het enzym, is de functie van het enzym juist. Ze maken de reactie gemakkelijker door de activeringsenergie te verlagen en meer moleculen te activeren, waardoor de katalysator wordt uitgevoerd.
Effect van enzymconcentratie
De concentratie van het enzym is belangrijk bij chemische reacties, omdat het nodig is om met het substraat te reageren. Vaak kan een kleine hoeveelheid enzym een grote hoeveelheid substraat verbruiken. Met de toename van de enzymconcentratie neemt echter ook de effectiviteit van de actieve sites toe, zodat deze actieve sites de substraatmoleculen in producten zullen omzetten. Dit betekent in feite dat als de concentratie van het enzym wordt verhoogd, er een overmaat aan substraat moet zijn, met andere woorden dat de reactie onafhankelijk moet zijn van de concentratie van het substraat.
Zero-Order Reaction
Om het effect van verhoging van de enzymconcentratie op de reactiesnelheid te bestuderen, moet het substraat in een overmaat aanwezig zijn; dat wil zeggen dat de reactie onafhankelijk moet zijn van de substraatconcentratie. Elke verandering in de hoeveelheid product die in een bepaalde tijdsperiode wordt gevormd, is afhankelijk van de hoeveelheid aanwezig enzym. Grafisch kan dit als volgt worden weergegeven:
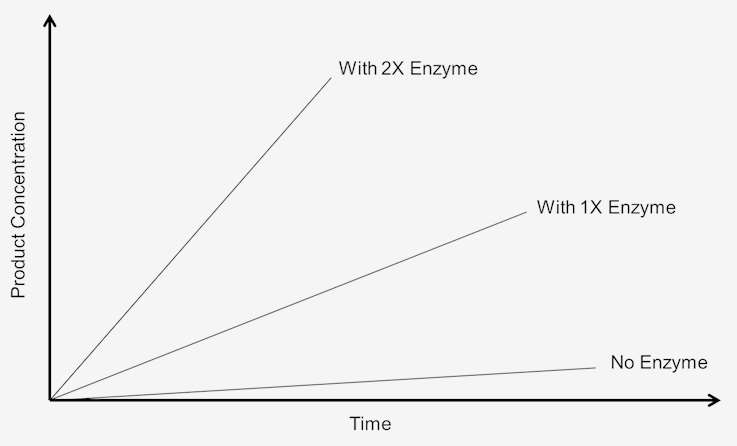 Figuur 1. Nul-orde reactiesnelheid is afhankelijk van substraatconcentratie.
Figuur 1. Nul-orde reactiesnelheid is afhankelijk van substraatconcentratie.
Deze reacties worden “nul-orde reacties” genoemd omdat de snelheden onafhankelijk zijn van de substraatconcentratie. De vorming van product verloopt met een snelheid die lineair is met de tijd. De toevoeging van meer substraat verhoogt de snelheid niet. Bij een nul-orde kinetiek resulteert een verdubbeling van de tijd in een verdubbeling van de hoeveelheid product.
De hoeveelheid enzym die in een reactie aanwezig is, wordt gemeten aan de hand van de activiteit die het katalyseert. De verhouding tussen activiteit en concentratie wordt door vele factoren beïnvloed, zoals temperatuur, pH, enz. Een enzymtest moet zo worden ontworpen dat de waargenomen activiteit evenredig is met de hoeveelheid aanwezig enzym, zodat de enzymconcentratie de enige beperkende factor is. Hieraan wordt alleen voldaan wanneer de reactie nul-orde is.
Gerelateerde diensten
Enzymkinetiek
Enzymologie Assays
Om meer details van de dienst te bespreken, kunt u contact met ons opnemen door te bellen naar 1-631-562-8517, of ons een e-mail te sturen naar [email protected].