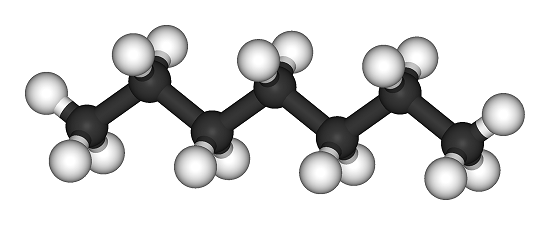
Heptan är en alkan med den kemiska formeln C7H16. Som kolväte kan det genomgå kolväteförbränning som avger värmeenergi Heptan är en flyktig, färglös vätska som är luktfri när den är ren.
Heptan är en viktig kolväte (eller organisk molekyl) eftersom den, tillsammans med rent oktan, fastställer de extrema ändarna på oktantalskalan. Heptan används för att fastställa standardens nollpunkt. Detta innebär att det som bränsle brinner på ett sätt som är olämpligt i en motor, närmare bestämt att det förbränns när det sätts under tryck. Därför är högre oktantal bättre för en motor. Heptan är ett fruktansvärt bränsleval för en bil eftersom det brinner explosivt och orsakar knackningar i motorn. Förutom att heptan är nollpunkten för oktantalet används det ofta som lösningsmedel i laboratorier på grund av sin låga reaktivitet med andra molekyler. Många ämnen som inte löser sig i vatten löser sig i heptan.
Egenskaper
Nedan följer en tabell med några av de grundläggande egenskaperna hos heptan.
| Kemisk formel | C7H16 |
| Molarmassa | 100.21 gram/mol |
| Smältpunkt | -91oC |
| Kokpunkt | 98oC |
Förbränningsreaktion
Heptan genomgår en förbränning av kolväten, där det förenas med syre till koldioxid. Den balanserade kemiska ekvationen för fullständig förbränning av heptan är:
Kolväteförbränningsreaktionen frigör värmeenergi och är ett exempel på en exoterm reaktion. Reaktionen har också ett negativt värde för entalpiändringen (ΔH).
För ytterligare läsning
- Kemisk energi
- Kemisk bindning
- Förbränning
- Primär. energi
- Energiomvandlingsteknik
- Och utforska en slumpmässig sida
- ”Heptan-3D-bollar”. Licensed under Public Domain via Wikimedia Commons – http://commons.wikimedia.org/wiki/File:Heptane-3D-balls.png#mediaviewer/File:Heptane-3D-balls.png
- National Center for Biotechnology Information. (2015). Egenskaper hos heptan . Tillgänglig: http://pubchem.ncbi.nlm.nih.gov/compound/heptane .
- Utbildningsportal. (2015). Heptan: Struktur, användning, & Formel . Tillgänglig: http://education-portal.com/academy/lesson/heptane-structure-uses-formula.html
- 4.0 4.1 Charles E. Ophardt. (2003). Virtual Chembook – Hydrocarbon Boiling Points . Tillgänglig: http://www.elmhurst.edu/~chm/vchembook/501hcboilingpts.html .