28. listopadu prohlásil He Jiankui před zaplněnou konferenční místností na druhém mezinárodním summitu o úpravě lidského genomu v Hongkongu, že upravil genom dvou dvojčat Lulu a Nany, která se narodila v Číně.
Vědci z Jižní univerzity vědy a technologie v čínském Kuang-tungu Heův výzkum odsoudili s tvrzením, že „vážně porušil akademickou etiku a kodexy chování“, a filozofové a bioetici se rychle ponořili do morku editace lidských genomů. Nebudu se tedy zabývat tímto územím. Chci se zabývat tím, co jsme se dozvěděli: jak stvořil tyto děti.
Jsem teoreticky penzionovaný profesor na katedře biomedicínských věd na Coloradské státní univerzitě. Více než 50 let jsem zkoumal četné aspekty asistované reprodukce včetně klonování a provádění genetických změn na savčích embryích, takže mě zajímá většina všech výzkumů týkajících se „designových dětí“ a zdravotních problémů, kterými mohou trpět.
První?
Na konferenci podal obecný přehled o vědě. Ačkoli by se takový výzkum obvykle prezentoval vědecké komunitě publikováním v recenzovaném časopise, což má podle svých slov v úmyslu, můžeme si udělat přibližnou představu o tom, jak tyto modifikované děti vytvořil. Jedná se o něco, co bylo úspěšně provedeno u jiných živočišných druhů a právě v loňském roce u lidských embryí – ta však nebyla implantována do ženy. Říká, že než přešel k práci na lidských embryích, strávil tři roky testováním tohoto postupu na myších a opicích.
Není pochyb o tom, že lze provádět přesné genetické úpravy lidských spermií, vajíček, embryí a dokonce i některých buněk dospělých lidí. Takové modifikace byly provedeny ad nauseum u myší, prasat a několika dalších savců. Vědcům, jako jsem já, je tedy zřejmé, že tytéž genetické modifikace mohou být a budou provedeny i u lidí. Nejjednodušší způsob, jak provádět genetické změny, začíná u embrya.
Sada nástrojů
Nejmodernější strategie pro modifikaci DNA v současnosti zahrnuje nástroj pro úpravu genů CRISPR/Cas-9, který dokáže provádět přesné genetické modifikace v živých buňkách. Ačkoli jsou již léta k dispozici i jiné nástroje, přístup CRISPR/Cas-9 je jednodušší, snazší, přesnější a levnější.
Způsob jeho fungování je v zásadě jednoduchý. Součást Cas-9 jsou molekulární nůžky, které stříhají DNA v místě určeném malým kouskem RNA, nazývaným „šablona CRISPR“. Jakmile je DNA přestřižena, může být v daném místě upraven gen. Řez je pak opraven enzymy, které jsou již v buňkách přítomny.
V tomto případě se zaměřil na gen, který produkuje protein na povrchu buněk zvaný CCR5. Virus HIV používá tento protein k tomu, aby se připojil k buňce a infikoval ji. Jeho záměrem bylo geneticky změnit CCR5 tak, aby virus HIV již nemohl infikovat buňky, čímž by se dívky staly vůči viru odolné.
V tuto chvíli neposkytl jasné vysvětlení, jak přesně CCR5 vyřadil a jaká byla povaha genetické modifikace. Tento druh „vyřazení“ se však ve výzkumu běžně používá.
Jak to udělal
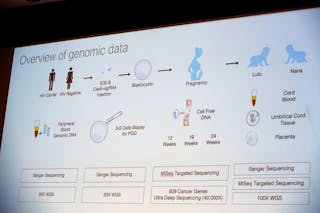
Z diagramu, který představil, vyplývá, že systém CRISPR/Cas-9 vpravil do vajíčka současně s vpravením spermie k jeho oplodnění. Poté se vajíčko rozdělilo a vytvořilo klubko desítek buněk – embryo. V této fázi odebral z každého embrya několik buněk, aby zjistil, zda došlo k požadované genetické změně. Podle mých zkušeností byla embrya v této fázi pravděpodobně zmražena. Když byla analýza dokončena, pravděpodobně rozmrazil upravená embrya a ta nejlepší přenesl zpět do dělohy matky k donošení. Embrya bez úprav nebo s nesprávnými úpravami by byla buď vyřazena, nebo použita pro výzkum.
Pro mnoho aplikací je ideální provádět jakékoli změny genů ve stadiu jedné buňky. Když pak embryo duplikuje svou DNA a rozdělí se na dvoubuněčné embryo, genetická úprava se také duplikuje. Takto se pokračuje, takže genetickou změnu má každá buňka výsledného dítěte.
Zdá se však, že genetická modifikace v tomto případě nastala až ve dvoubuněčném stadiu nebo později, protože některé buňky v dětech tuto modifikaci měly, zatímco jiné ne. Tato situace se nazývá mozaika, protože dítě je mozaikou normálních a upravených buněk.
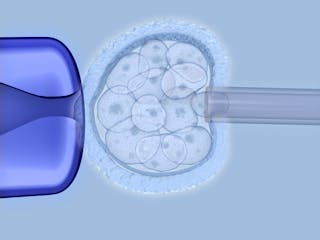
Nebezpečí editace embryí?“
Co se může pokazit u embrya upraveného genem? Spousta.
První závadou je, že nebyla provedena žádná úprava, což se stává často. Variantou je, že ke změně dojde v některých buňkách embrya, ale ne ve všech, jak se stalo u těchto dětí.
Nejčastější obavou jsou tzv. necílové účinky, kdy je genetická modifikace provedena, ale na jiných místech genomu dojde k další nechtěné úpravě (úpravám). Mít modifikaci na nesprávném místě může způsobit nejrůznější vývojové problémy, například abnormální vývoj orgánů, potraty a dokonce i rakovinu.
Z jeho slajdu vyplývá, že sekvenoval genomy – kompletní genetický plán každého dítěte – v několika fázích těhotenství, aby zjistil, zda nedošlo k nežádoucím modifikacím, i když ty není vždy snadné najít. Dokud však nezávislí vědci nebudou moci prozkoumat DNA těchto dvou holčiček, nebudeme znát výsledky. Z výsledků, o které se zatím podělil, také není jasné, zda se tato genetická změna může přenést na další generaci.
Dalším častým problémem, na který jsme již naráželi, je mozaika, k níž zřejmě došlo u jednoho z těchto dvojčat. Pokud jsou některé buňky editovány a některé ne, může se stát, že dítě bude mít například jaterní buňky obsahující editovaný gen a srdeční buňky s normální verzí. To může, ale nemusí vést k vážným problémům.

Dalším problémem je, že manipulace s embryi in vitro – mimo jejich normální prostředí v reprodukčním traktu – kde nemůžeme přesně kopírovat normální výživu, hladinu kyslíku, hormony a růstové faktory – by mohla vést k vývojovým abnormalitám včetně nadměrné velikosti plodu, metabolických problémů atd. K tomu někdy dochází při rutinních postupech, jako je oplodnění in vitro, kdy není snaha o genetické úpravy.
Naštěstí je příroda poměrně dobrá ve vyřazování abnormálních embryí prostřednictvím embryonální smrti a spontánních potratů. Dokonce i ve zdravé lidské populaci, která se normálně rozmnožuje, téměř polovina embryí zemře dříve, než se žena vůbec dozví, že byla těhotná.
Přestože jsem zdůraznil, co se může pokazit, věřím, že se věda bude vyvíjet tak, že geneticky modifikované děti budou zdravější než nemodifikované. A tato zlepšení se budou přenášet na další generace. Genetickou modifikací by mohly být z rodiny odstraněny těžce oslabující genetické abnormality, jako je například Tay-Sachsův syndrom.
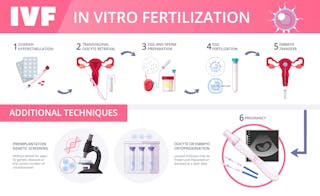
Pravděpodobně se již rodí designové děti pomocí techniky zvané preimplantační genetická diagnostika (PGD). Několik buněk z embryí je vyšetřeno na desítky a potenciálně stovky genetických abnormalit, jako je například Downův syndrom, cystická fibróza a Tay-Sachsův syndrom. Rodiče si také mohou vybrat embrya požadovaného pohlaví. Podle mého názoru je výběr embryí k implantaci jednoznačně vytvářením designových dětí.
Jdeme-li o krok dál, PGD se neomezuje pouze na odstraňování nemocí. Budoucí rodič si může vybrat i jiné znaky. Pokud je jeden z budoucích rodičů neplodný, existují katalogy, které poskytují údaje o rase, výšce a váze, a dokonce i o úrovni vzdělání dárce spermatu nebo vajíčka, u něhož je navíc zjištěno, že nemá závažné genetické vady a netrpí AIDS a jinými pohlavními chorobami.

Podle mého názoru, pokud budou postupy považovány za eticky a morálně přijatelné, bude většina genetických modifikací, které budou pravděpodobně provedeny úpravou embryí, jak tvrdí, zahrnovat spíše odstranění škodlivých než přidání žádoucích znaků. Protože změny budou cílené, budou přesnější a méně škodlivé než mutace, které se náhodně vyskytují v DNA v podstatě všech spermií a vajíček přirozenou cestou.
Ve všech těchto reprodukčních technologiích je tu ještě jeden aspekt: obrovské náklady na popsané postupy. Do jaké míry by měla společnost investovat vzácné lékařské zdroje do aplikace těchto technik, zvláště když případné výhody pravděpodobně získají především bohatší rodiny?
Tato hlediska je třeba mít na paměti při hodnocení potenciálních genetických manipulací s lidmi.