November 28-án He Jiankui a hongkongi Second International Summit on Human Genome Editing konferenciaterem zsúfolásig megtelt üléstermében azt állította, hogy ő szerkesztette a Kínában született két ikerlány, Lulu és Nana genomját.
A kínai Guangdongban található Déli Tudományos és Technológiai Egyetem tudósai elítélték He kutatását, azt állítva, hogy “súlyosan megsértette az akadémiai etikát és magatartási kódexet”, a filozófusok és bioetikusok pedig gyorsan belemerültek az emberi genomok szerkesztésének mocsarába. Szóval nem fogok erre a területre kitérni. Amivel foglalkozni akarok, az az, amit megtudtunk: hogyan készítette ezeket a babákat.
Elméletileg a Colorado Állami Egyetem Biomedicinális Tudományok Tanszékének nyugalmazott professzora vagyok. Több mint 50 éve kutatom az asszisztált reprodukciós technológia számos aspektusát, beleértve a klónozást és az emlősök embrióinak genetikai módosítását, ezért érdekel a legtöbb kutatás a “dizájner babákkal” és az általuk esetleg elszenvedett egészségügyi problémákkal kapcsolatban.
Egy első?
A konferencián általános áttekintést adott a tudományról. Bár az ehhez hasonló kutatásokat általában úgy mutatnák be a tudományos közösségnek, hogy egy lektorált folyóiratban publikálnának, amit állítása szerint szándékában áll megtenni, nagyjából képet kaphatunk arról, hogyan hozta létre ezeket a módosított babákat. Ez olyasmi, amit már sikeresen elvégeztek más fajokon, és éppen tavaly emberi embriókon – de ez utóbbiakat nem ültették be nőbe. Elmondása szerint három évig tesztelte az eljárást egereken és majmokon, mielőtt áttért az emberi embriókon végzett munkára.
Kétségtelen, hogy pontos genetikai módosításokat lehet végezni az emberi spermiumokon, petesejteken, embriókon, sőt még a felnőttek egyes sejtjein is. Ilyen módosításokat egereken, sertéseken és számos más emlősön is végeztek már a végtelenségig. Így a hozzám hasonló tudósok számára nyilvánvaló, hogy ugyanezeket a genetikai módosításokat embereken is el lehet végezni, és el is fogják végezni. A genetikai módosítások elvégzésének legegyszerűbb módja az embrióval kezdődik.
Az eszköztár
A DNS módosításának legtrendibb stratégiája manapság a CRISPR/Cas-9 génszerkesztő eszköz, amely képes pontos genetikai módosításokat végezni élő sejtekben. Bár más eszközök már évek óta rendelkezésre állnak, a CRISPR/Cas-9 megközelítés egyszerűbb, könnyebb, pontosabb és olcsóbb.
A működés módja egyszerű koncepció. A Cas-9 komponens egy molekuláris olló, amely a DNS-t egy kis RNS-darabka, az úgynevezett “CRISPR-templát” által meghatározott helyen vágja el. Miután a DNS-t elvágták, egy gén módosítható az adott helyen. A vágást ezután a sejtekben már jelen lévő enzimek javítják ki.
Ebben az esetben egy olyan gént vett célba, amely a sejtek felszínén egy CCR5 nevű fehérjét termel. A HIV-vírus ezt a fehérjét használja a sejthez való kapcsolódáshoz és a fertőzéshez. Az volt az ötlete, hogy genetikailag megváltoztatja a CCR5-öt, hogy a HIV többé ne tudja megfertőzni a sejteket, így a lányok ellenállóvá válnak a vírussal szemben.
Előre nem adott egyértelmű magyarázatot arra, hogy pontosan hogyan kapcsolta ki a CCR5-öt és milyen jellegű volt a genetikai módosítás. De ezt a fajta “kikapcsolást” rutinszerűen alkalmazzák a kutatásban.
Hogyan csinálta
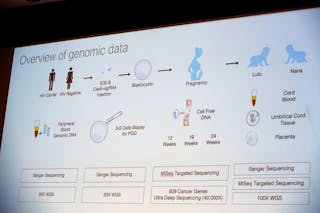
Az általa bemutatott ábrából úgy tűnik, hogy He a CRISPR/Cas-9 rendszert egy petesejtbe fecskendezte, ugyanakkor, amikor a spermiumot befecskendezte a megtermékenyítéshez. Ezt követően a petesejt osztódott, és egy tucatnyi sejtből álló gömböt – az embriót – alkotott. Ebben a szakaszban minden egyes embrióból eltávolított néhány sejtet, hogy megállapítsa, megtörtént-e a kívánt genetikai változás. Tapasztalataim alapján az embriókat valószínűleg ekkor fagyasztották le. Amikor az elemzés befejeződött, valószínűleg felolvasztotta a módosított embriókat, és a legjobbakat visszahelyezte az anya méhébe a terhesség végéig történő kihordásra. A szerkesztés nélküli vagy helytelenül szerkesztett embriókat vagy kidobták, vagy kutatásra használták fel.
Sok alkalmazás szempontjából ideális, ha a génmódosításokat az egysejtes stádiumban végezzük el. Ezután, amikor az embrió megkettőzi a DNS-ét és osztódik, hogy kétsejtű embriót hozzon létre, a genetikai módosítás is megkettőződik. Ez így folytatódik, így a létrejövő baba minden sejtje rendelkezik a genetikai változtatással.
Úgy tűnik azonban, hogy a genetikai módosítás ebben az esetben csak a kétsejtes stádiumban vagy később következett be, mert a babák egyes sejtjei rendelkeztek a módosítással, míg mások nem. Ezt a helyzetet mozaikizmusnak nevezik, mert a gyermek a normális és a módosított sejtek mozaikja.
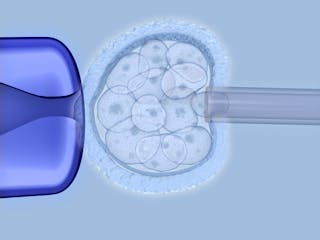
Az embriószerkesztés veszélyei?
Mi romolhat el egy génszerkesztett embrióban? Rengeteg.
Az első hiba az, hogy nem történt módosítás, ami gyakran előfordul. Egy variáció az, hogy a módosítás az embrió egyes sejtjeiben történik, de nem az összes sejtben, mint ahogyan az ezeknél a babáknál történt.
A leggyakoribb aggodalom az úgynevezett nem célzott hatások, amikor a genetikai módosítás megtörténik, de a genom más helyein más, nem szándékos szerkesztés(ek) következnek be. Ha egy módosítás rossz helyen történik, az mindenféle fejlődési problémát okozhat, például rendellenes szervfejlődést, vetélést és akár rákot is.
A diájából kiderül, hogy a terhesség több szakaszában szekvenálta a genomokat – az egyes gyermekek teljes genetikai tervrajzát -, hogy megállapítsa, voltak-e nem kívánt módosítások, bár ezeket nem mindig könnyű megtalálni. De amíg független tudósok nem vizsgálják meg a két kislány DNS-ét, addig nem tudjuk meg az eredményeket. Az általa eddig megosztott eredményekből az sem világos, hogy ez a genetikai változás átörökíthető-e a következő generációra.
A másik gyakori probléma, amire már utaltunk, a mozaikosság, ami a jelek szerint az egyik ikerpárnál történt. Ha néhány sejtet szerkesztettek, néhányat pedig nem, akkor a babának például lehetnek olyan májsejtjei, amelyek a szerkesztett gént tartalmazzák, és olyan szívsejtjei, amelyek a normál változatot. Ez vagy komoly problémákhoz vezethet, vagy nem.

Egy másik kérdés, hogy az embriók in vitro – a normál környezetükön kívül, a reproduktív traktusban – történő manipulálása, ahol nem tudjuk pontosan lemásolni a normális táplálkozást, oxigénszintet, hormonokat és növekedési faktorokat, fejlődési rendellenességekhez vezethet, beleértve a túlméretezett magzatokat, anyagcsereproblémákat és így tovább. Ez néha olyan rutineljárásoknál fordul elő, mint az in vitro megtermékenyítés, amikor nem próbálnak genetikai módosításokat végezni.
Szerencsére a természet elég jól kigyomlálja a rendellenes embriókat az embrióhalál és a spontán abortusz révén. Még az egészséges, normálisan szaporodó emberi populációkban is az embriók közel fele elpusztul, mielőtt a nő egyáltalán tudomást szerezne arról, hogy terhes.
Már most is tervezünk babákat – és vannak előnyei
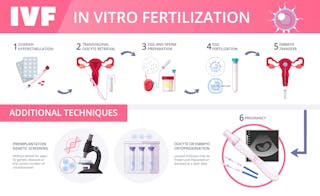
Míg hangsúlyoztam, hogy mi minden romolhat el, hiszem, hogy a tudomány úgy fog fejlődni, hogy a genetikailag módosított csecsemők egészségesebbek lesznek, mint a változatlanok. És ezek a fejlesztések továbbadódnak majd a következő generációknak. Súlyosan gyengítő genetikai rendellenességeket, mint például a Tay-Sachs-szindróma, genetikai módosítással ki lehetne küszöbölni egy családból.
Vitathatóan már most is születnek dizájnbabák a beültetés előtti genetikai diagnózisnak (PGD) nevezett technika segítségével. Az embriók néhány sejtjét több tucat, potenciálisan több száz genetikai rendellenességre vizsgálják, mint például a Down-szindróma, a cisztás fibrózis és a Tay-Sachs-szindróma, hogy csak néhányat említsünk. A szülők a kívánt nemű embriókat is kiválaszthatják. Véleményem szerint a beültetendő embriók kiválasztása egyértelműen dizájnbabák készítése.
Egy lépéssel továbbmenve, a PGD nem korlátozódik csupán a betegségek kiküszöbölésére. A leendő szülő más tulajdonságokat is választhat. Ha az egyik leendő szülő terméketlen, léteznek olyan katalógusok, amelyek megadják a spermium- vagy petesejtdonor faját, magasságát és súlyát, sőt még az iskolai végzettségét is, akiről azt is megállapítják, hogy mentes a főbb genetikai hibáktól, valamint az AIDS-től és más nemi betegségektől.

Véleményem szerint, ha az eljárásokat etikailag és erkölcsileg elfogadhatónak tartják, a legtöbb genetikai módosítás, amelyet valószínűleg az embriók szerkesztésével végeznek, ahogyan Ő mondja, inkább a káros tulajdonságok eltávolítását jelenti majd, mint a kívánatosak hozzáadását. Mivel a módosítások célzottan történnek, pontosabbak és kevésbé károsak lesznek, mint azok a mutációk, amelyek véletlenszerűen fordulnak elő lényegében minden spermium és petesejt DNS-ében a természetben.
Mindezzel a reprodukciós technológiával kapcsolatban van még egy szempont: a leírt eljárások hatalmas költségei. Milyen mértékben kellene a társadalomnak a szűkös orvosi erőforrásokat az ilyen technikák alkalmazásába fektetnie, különösen mivel az esetleges előnyök valószínűleg főként a tehetősebb családokat fogják érinteni?
Ezeket a szempontokat szem előtt kell tartani, amikor az embereken végzett lehetséges genetikai manipulációkat értékeljük.