Antibiotika udrydder patogene infektioner og redder liv – men samtidig forstyrrer de også integriteten af tarmens mikrobiom. Mens mange læger erkender behovet for at genoprette en patients mikrobielle balance efter et antibiotikaforløb, er der langt færre, der forstår, hvordan man gør dette effektivt.
Ved Amie Skilton, ND, er genoprettelse af tarmfloraen både kunst og videnskab. Hvis det gøres godt, kan det gøre en verden til forskel for patienterne. I nogle tilfælde kan det endda hjælpe patienterne med at overvinde de sygdomme, som antibiotika oprindeligt blev ordineret for.
Men det kræver mere end blot at anbefale et probiotikum fra hylden og håbe på det bedste.
Centers for Disease Control rapporterede sidste forår, at af de 154 millioner recepter på antibiotika, der hvert år udskrives i lægepraksis og på skadestuer, er 30 procent unødvendige. De fleste af de overflødige recepter, fandt CDC, blev uddelt for respiratoriske tilstande forårsaget af virus som almindelig forkølelse, viral halsbetændelse, bronkitis og bihule- og øreinfektioner, som ikke reagerer på antibiotika. Brugen af disse lægemidler “udsætter patienterne for unødig risiko for allergiske reaktioner eller den undertiden dødelige diarré, Clostridium difficile.”
Det komplicerer billedet yderligere, at antibiotika ikke kun spredes fra lægepraksis; de gives også i stor stil til husdyr og sprøjtes i stor stil på produkter, hvilket efterlader minimale, men biologisk aktive spor i de fødevarer, som mennesker så indtager.
Dosis, timing bestemmer virkningen
Da antibiotika dræber infektionsfremkaldende mikroorganismer, ødelægger de også ikke-selektivt samfund af gavnlige tarmbakterier, hvilket svækker stabiliteten af tarmmikrobiomet. Denne omfattende ødelæggelse kan være massiv; eksperimentelle data fra en undersøgelse ved hjælp af qPCR viser op til en 10-dobbelt reduktion af bakterieisolater umiddelbart efter behandling med antibiotika (Panda, S. et al. PLoS One. 2014; 9(4): e95476).
“Det er virkelig en decimerende effekt”, siger Dr. Skilton, naturmedicinsk læge og urteforsker ved Elysium Clinic of Natural Medicine i Sydney, NSW, Australien.
I et webinar sponsoreret af Holistic Primary Care and Bioceuticals skitserede hun de utallige virkninger af antibiotika på det menneskelige mikrobiom, idet hun bemærkede, at ikke alle antibiotika er lige ødelæggende for tarmbakterierne.
Den grad, i hvilken disse lægemidler skader tarmmikrobiotaen, afhænger af lægemiddeltype, behandlingsvarighed og hyppighed af brugen, sagde Skilton. Visse antibiotika udløser f.eks. en større frigivelse af endotoxiner og cytokiner end andre. Højere daglige doser har større virkning. Langvarig brug af antibiotika i høje doser kan forårsage ekstreme skader på mikrobiomet, som det kan tage flere år med genoprettende behandling at vende, hvis det overhovedet kan vendes.
Og i modsætning til den almindelige opfattelse kan intravenøs antibiotika have samme negative indvirkning på tarmfloraen som orale lægemidler. “I lang tid troede man, at intravenøse lægemidler ville gå uden om tarmen og ikke have den samme virkning. Vi ved nu, at det ikke er sandt.”
Tidspunktet for tilførsel af antibiotika gør også en forskel. Personer, der ofte bruger antibiotika tidligt i livet, er mere sårbare over for mange typer sygdomme, når de bliver ældre. I en artikel, der blev offentliggjort tidligere i år, påviste forskere en sammenhæng mellem antibiotikaforbrug i spædbarnsalderen og efterfølgende dårlige neurokognitive resultater, hvilket tyder på, at antibiotikaforbrug i en patients første leveår var forbundet med små, men statistisk signifikante forskelle i kognitive, adfærdsmæssige og humørmæssige foranstaltninger i barndommen (Slykerman, R. et al. Acta Paediatr. 2017; 106(1): 87-94).
Andre har knyttet føtal antibiotikaeksponering og antibiotikaeksponering i den tidlige barndom til den efterfølgende udvikling af astma senere i livet (Örtqvist, A. et al. Brit Med J. 2014; 349. doi: https://doi.org/10.1136/bmj.g6979). Antibiotika er også blevet sat i forbindelse med fedme og vægtøgning hos børn såvel som voksne (Million, M. et al. Clin Microbiol & Infec. 2013; 19(4): 305-313). Forskerne tilskriver disse ændringer den ændrede sammensætning af tarmens mikrobielle sammensætning.
Antibiotika kan udløse frigivelse af giftige lipopolysaccharider (LPS), store molekyler, der findes i de ydre membraner af patogene gramnegative bakterier. Nogle antyder, at antibiotika-induceret LPS-frigivelse kan bidrage til udviklingen af septisk chok hos patienter, der behandles for alvorlige infektioner forårsaget af Gram-negative bakterier. Andre har vist, at LPS udløser et immunrespons ved at frigive inflammatoriske cytokiner, et problem, der forværres efter antibiotikabehandling, bemærkede Skilton i sit webinar (Wu, T. et al. Toxicol Lett. 2009; 191(2-3): 195-202).
Fra et patogens synspunkt er produktion af LPS en overlevelsesstrategi. Disse molekyler interagerer på celleoverflader og danner en barriere, der forhindrer antibiotika og andre hydrofobiske forbindelser i at trænge ind og gør det muligt for gramnegative bakterier at leve selv i barske miljøer (Zhang, G. et al. Curr Opin Microbiol. 2013; 16(6): 779-785).
Hvordan man genopretter floraen
Probiotika er et aspekt i en omfattende strategi til at genoprette tarmfloraen efter antibiotika. I betragtning af den mikrobielle mangfoldighed i et sundt tarmøkosystem anbefaler Skilton at bruge produkter, der indeholder mange forskellige arter af gavnlige mikrober, i stedet for at “monokroppe” med en eller to enkelte stammer.
Som en generel regel anbefaler hun en måneds probiotisk behandling for hver uge, som en patient har været på antibiotika. De, der har været på langvarig kontinuerlig antibiotikabehandling, vil ligeledes have behov for langvarig genoprettelse. Hun understreger, at der for de fleste mennesker ikke er nogen sundhedsmæssige risici forbundet med længerevarende probiotisk tilskud.
Patienter, der modtager IV-antibiotika, bør også tage kommensale probiotika. Nogle klinikere, der er opmærksomme på dette problem, vil starte probiotika så tidligt som fire timer efter en dosis IV-antibiotika.
Opbygning af glykokalyxet
Personer, der har været på langvarig eller flere antibiotikakurser, viser typisk en alvorlig erosion af glykokalyxet, der normalt beklæder tarmens mikrovilli. Dette er normalt ledsaget af et tab af børstegrænser og en markant reduktion i den sekretoriske IgA-produktion.
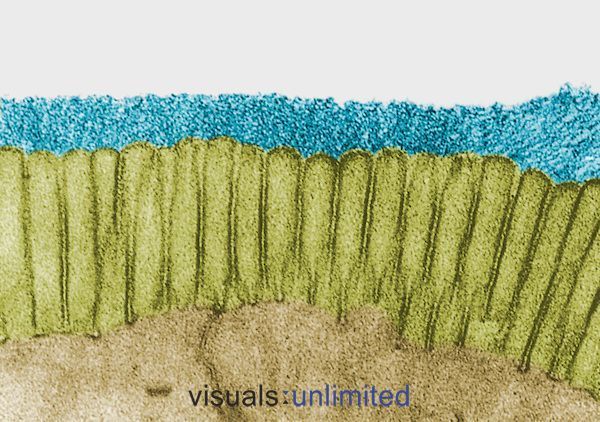 I nogle tilfælde er disse ændringer forårsaget af selve virkningerne af antibiotika. I andre tilfælde afspejler de virkningen af den infektion, for hvilken antibiotika blev ordineret. Uanset hvad er effekten den samme: etablering af et mikromiljø, der er gæstfrit for opportunistiske patogener som Candida, men stadig vanskeligere for normale kommensale bakterier.
I nogle tilfælde er disse ændringer forårsaget af selve virkningerne af antibiotika. I andre tilfælde afspejler de virkningen af den infektion, for hvilken antibiotika blev ordineret. Uanset hvad er effekten den samme: etablering af et mikromiljø, der er gæstfrit for opportunistiske patogener som Candida, men stadig vanskeligere for normale kommensale bakterier.
Svampeinfektioner ledsages næsten altid af utilstrækkelig IgA-produktion, da Candida forbruger både glycocalyx og sIgA som brændsel. Det bliver en ond cirkel: lavt IgA avler Candida, som yderligere udtømmer IgA. Kroniske urinvejsinfektioner og slimhindeinfektioner som f.eks. trøske er røde flag for lav sIgA-produktion, påpegede Skilton.
Suden et sundt glycocalyx har organismer som Lactobacilli og Bifidobacilli meget svært ved at etablere sig. I denne sammenhæng vil tilskud med almindelige probiotika normalt mislykkes.
“Selv om man anbefaler de bedste probiotika i verden, kan de ikke holde sig fast og kolonisere, hvis glycocalyxet er udhulet,” forklarede Dr. Skilton. “Du kan faktisk overdrive GI-symptomer ved at give probiotika, hvis der er tab af evnen til at producere glycocalyx.”
For at genoprette et sundere mikromiljø i disse tilfælde skal du udnytte de unikke egenskaber ved Saccharomyces boulardii, en antibiotikaresistent, probiotisk gær, der oprindeligt blev isoleret fra litchi-frugter i Indokina. Selv om S. boulardii ikke er en ægte kommensal organisme, er den en potent inducerer af glycocalyx-produktion og IgA-sekretion. Den stimulerer også enzymer ved børstensgrænsen og fremmer polyaminproduktionen, som nærer tarmens mikrovilli og kan være nyttig ved helbredelse af colitis ulcerosa, Crohns sygdom og irritabel tyktarm.
S. boulardii er i stand til at virke i forbindelse med højpatogene antibiotikaresistente bakterier som Clostridium difficile og er faktisk blevet anvendt som forebyggende behandling mod C. difficile-associeret diarré (Goldstein, E. et al. Clin Infect Dis. 2015; 60 (suppl_2): S148-S158). S. boulardii kan reducere nogle af de toksiske virkninger af enterotoxin A ved at hæmme toxin A-receptorbinding og forhindre dannelsen af enterotoxin B.
Men det mest bemærkelsesværdige er dens evne til hurtigt at kolonisere det beskadigede endotel og fortrænge patogene gærsvampe, samtidig med at den skaber et sundere mikromiljø for kommensale bakterier. “S. boulardii fremtvinger faktisk en fysisk evakuering af Candida,” siger Dr. Skilton og bemærker, at den er specifikt aktiv mod 7 ud af de 8 mest almindelige patogene Candida-arter. Den eneste undtagelse er C. tropicalis.
“Tænk på situationen som efterdønningerne af en orkan, der rammer en landsby. Antibiotika er orkanen. S. boulardii er som entreprenøren, der kommer ind og reparerer skaderne på landsbyen. Du kan derefter genbefolke landsbyen med kommensaler.”
BioCeuticals, et australsk nutraceutisk firma, der kun er rettet mod praktiserende læger, introducerede for nylig et produkt kaldet SB Floractiv, der indeholder 250 mg S. boulardii (også kaldet S. cereviciae) pr. kapsel.
For patienter, der har været på langtidsantibiotika, skal man begynde langsomt med en kapsel (250 mg) om dagen i 3-4 dage, derefter øge til to om dagen i yderligere 3-4 dage og derefter øge i et lignende trinvist mønster op til fire om dagen (1000 mg), som bør fortsættes i resten af en 4-ugers periode.
S. boulardii er meget sikker, og den eneste egentlige kontraindikation er hos patienter med ægte IgE-medierede reaktioner på gærsvampe, der manifesterer sig som anafylaksi eller 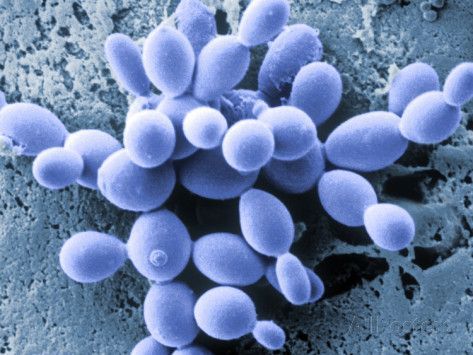 nældefeber. Når det er sagt, er det vigtigt at være opmærksom på, at nogle patienter i de første par dage efter indtagelse af S. boulardii kan opleve en mærkbar “tarmskylning”, da den probiotiske gær fortrænger Candida-arterne. Candidal die-off kan også få folk til at føle sig syge. Det er bedst at informere patienterne om disse muligheder på forhånd, så de ikke bliver overrasket, hvis de opstår.
nældefeber. Når det er sagt, er det vigtigt at være opmærksom på, at nogle patienter i de første par dage efter indtagelse af S. boulardii kan opleve en mærkbar “tarmskylning”, da den probiotiske gær fortrænger Candida-arterne. Candidal die-off kan også få folk til at føle sig syge. Det er bedst at informere patienterne om disse muligheder på forhånd, så de ikke bliver overrasket, hvis de opstår.
I henhold til Dr. Skelton er fire ugers intensivt tilskud af S. boulardii hos 9 ud af 10 patienter tilstrækkeligt til at genoprette et sundt glycocalyx-lag og inducere en tilstrækkelig IgA-sekretion. Dette lægger så op til en langt mere effektiv genoprettelsesrunde med et probiotikum med flere stammer.
Bioceuticals har udviklet et produkt specielt til brug efter antibiotika. Det hedder BioFloractiv 500 og indeholder 500 milliarder CFU’er, 12 arter og 14 stammer af gavnlige bakterier. Dr. Skilton anbefaler et maksimum på 14 dage, selv om en uges daglig behandling er tilstrækkelig for de fleste, ifølge Skilton.
Patienter med irritabel tyktarm eller Crohns sygdom kan dog have brug for længerevarende støtte for at genopbygge et sundt mikrobiom efter at have taget antibiotika.
En omfattende tilgang
Probiotika er kun en del af billedet. Og hvis en patient ikke kan tåle nogen form for probiotika, er det et rødt flag for, at patientens immunsystem ikke fungerer korrekt.
“Du skal først tage fat på alle aspekter af nervesystemet, især sympatisk dominans, der kan påvirke fordøjelseskanalen,” siger Dr. Skilton. Hun har fundet, at fiskeolie, zink, A-vitamin og colostrum har været af værdi i mange tilfælde. Sidstnævnte “er virkelig godt til at genoprette sIgA. Gør dette i en uge eller deromkring, før du overhovedet prøver probiotika.” Tilskud af slippery Elm og glutamin kan også være nyttige i nogle tilfælde.
Plantebaserede lægemidler som oreganoolie, tea tree oil eller pau d’arco-ekstrakt kan være nyttige til at befri GI-kanalen for patogene gærsvampe. Men Dr. Skilton understregede, at de ikke vil gøre noget for at stimulere sIgA-produktionen, og kroniske gærinfektioner er næsten altid forbundet med lavt IgA-niveau. Disse naturlige gær-busters bør aldrig bruges samtidig med S. boulardii; denne “venlige” gær er lige så sårbar over for ting som oregano og tea tree som de patogene gærsvampe.
En række probiotiske og præbiotiske fødevarer kan hjælpe processen med at genoprette tarmene. Tom O’Bryan, DC, grundlægger af Gluten Summit og uddannelsesprogrammet Certified Gluten Practitioner, anbefaler flere fødevarer, som man bør spise – og flere, som man bør undgå – når man genopbygger tarmen efter antibiotikabehandling.
“Når din tarm er blevet kompromitteret, ønsker du ikke at belaste din tarm,” siger O’Bryan. “Belastende” fødevarer omfatter hvede, mejeriprodukter, sukker, usunde fedtstoffer og stegte varer. Disse fødevarer, bemærker han, “smider benzin på ilden” i et tarmsystem, der er i bedring.
På den anden side bør man spise masser af fødevarer, der fremmer væksten af sunde kommensale organismer. O’Bryan anbefaler økologiske stuvede æbler, kogt til de er bløde og skimlede, som en god mulighed. Ved at koge æbler, forklarer han, frigøres pektin – en opløselig fiber, der giver brændstof til gavnlige bakterier.
Pektinen i stuvede æbler kan også hjælpe med at helbrede en beskadiget tarmslimhinde og forsegle revnerne i en utæt tarm, så store fødevaremolekyler ikke slipper igennem.
På samme måde hjælper kollagen med at forsegle en utæt tarm. O’Bryan opfordrer også patienter, der er ved at komme sig efter antibiotikabehandling, til at spise kyllingebenbuljong, som er en god kilde til kollagen, der også fungerer som et naturligt præbiotikum, der fodrer de sunde bakterier i tarmen.
Butyrat – et naturligt stof fremstillet i tarmen – er en anden vigtig aktør i genoprettelsen af tarmbakterier. O’Bryan forklarer, at cellerne, der beklæder tarmens inderside, reproducerer sig hurtigt, og at butyrat giver brændstof til genopbygningen af nye celler. Utilstrækkelig butyratproduktion og en langsom omsætning af tarmceller gør kroppen mere sårbar over for udvikling af kræftceller, hvilket resulterer i en højere risiko for tyktarmskræft.
En række præbiotiske frugter og grøntsager, herunder fødevarer bananer, søde kartofler og andre knolde, hjælper med at genopbygge tarmmikrobiomet, idet de leverer uopløselige fibre, der giver næring til gode – men ikke skadelige – bakterier.
Fermenterede, upasteuriserede grøntsager som surkål, kimchi og fermenterede rødbeder er en anden fremragende kilde til naturlige probiotika. Hver grøntsag producerer forskellige familier af gavnlige bakterier under fermenteringen, bemærker O’Bryan og opfordrer patienterne til at spise en gaffelfuld fermenterede grøntsager to gange om dagen. “Nøglen til sundhed i din tarm er mangfoldigheden af dit mikrobiom”, argumenterer han og påpeger, at tusindvis af forskellige bakteriefamilier lever og spiller sammen i tarmen med vidt forskellige virkninger på vores helbred.
END