Sappisuolat ja sappihapot ovat polaarisia kolesterolijohdannaisia, ja ne edustavat tärkeintä reittiä steroidin poistumisessa elimistöstä.
Ne ovat molekyylejä, joilla on samankaltainen, mutta ei täysin identtinen rakenne, ja joilla on moninaiset fysikaaliset ja biologiset ominaisuudet.
Ne syntetisoituvat maksassa, varastoituvat sappirakkoon, erittyvät pohjukaissuoleen ja lopulta suurimmaksi osaksi imeytyvät takaisin ileumiin.
Koska fysiologisessa pH:ssa nämä molekyylit esiintyvät anioneina, termejä sappihappo ja sappisuolat käytetään tässä yhteydessä synonyymeinä.
YHTEENVETO
- Sappisuolojen kemiallinen rakenne
- Primäär, konjugoidut ja sekundaariset sappisuolat
- Sappihappojen toiminta
- Sappisuolojen enterohepaattinen verenkierto
- Sappihappojen aineenvaihdunta suolistossa
- Liukoiset kuidut ja takaisinimeytyminen sappisuolojen
- Primaaristen sappihappojen synteesi
- Klassinen eli neutraali reitti
- Vaihtoehtoinen eli hapan reitti
- Pienemmät reitit
- Sappisuolat:
- Sappisuolojen kemiallinen rakenne
- Primääriset, konjugoidut ja sekundääriset sappisuolat
- Sappihappojen toiminta
- Sappisuolojen enterohepaattinen kierto
- Sappihappojen suolistoaineenvaihdunta
- Liukoiset kuidut ja sappisuolojen takaisinimeytyminen
- Primääristen sappihappojen synteesi
- Klassinen tai neutraali reitti
- Vaihtoehtoinen tai hapan reitti
- Pienemmät reitit
- Sappisuolat: synteesin säätely
Sappisuolojen kemiallinen rakenne
Sappisuoloilla on yhtäläisyyksiä ja eroja kolesterolimolekyylin kanssa.
Steroidin tavoin niillä on ydin, joka koostuu neljästä fuusioituneesta renkaasta: kolmesta sykloheksaanirenkaasta, jotka on merkitty A:lla, B:llä ja C:llä, ja syklopentaanirenkaasta, joka on merkitty D:llä. Tämä rakenne on perhydrosyklopentaanifenantreeni, joka tunnetaan yleisemmin steroidien ytimenä.
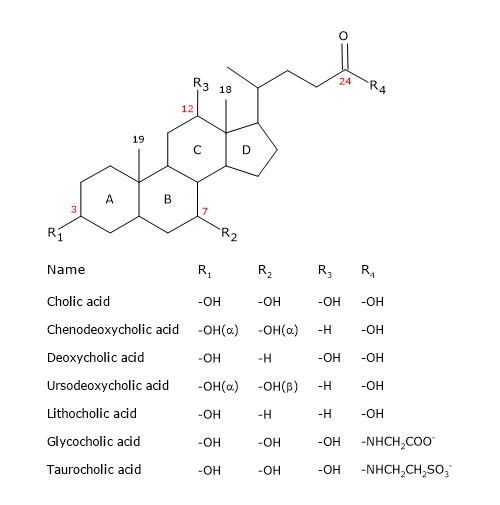
Korkeammilla selkärankaisilla niillä on 24 hiiliatomia, koska sivuketju on kolme hiiltä lyhyempi kuin alkuperäinen. Alemmilla selkärankaisilla sappihapoilla on 25, 26 tai 27 hiiliatomia. Sivuketju päättyy karboksyyliryhmään, joka ionisoituu pH 7:ssä ja joka voi liittyä aminohappo glysiiniin tai tauriiniin (ks. jäljempänä).
Positiossa 3 olevan hydroksyyliryhmän lisäksi niillä on hydroksyyliryhmiä positioissa 7 ja/tai 12.
Kaiken tämän vuoksi ne ovat paljon polaarisempia kuin kolesteroli.
Koska A- ja B-renkaat ovat fuusioituneet cis-konfiguraatiossa, steroidiytimen tasorakenne on kaareva, ja on mahdollista tunnistaa:
- kovera puoli, joka on hydrofiilinen, koska sivuketjun hydroksyyliryhmät ja karboksyyliryhmä, johon on tai ei ole sidoksissa aminohappoa, ovat suuntautuneet sitä kohti;
- kupera puoli, joka on hydrofobinen, koska asemissa 18 ja 19 esiintyvät metyyliryhmät ovat suuntautuneet sitä kohti.
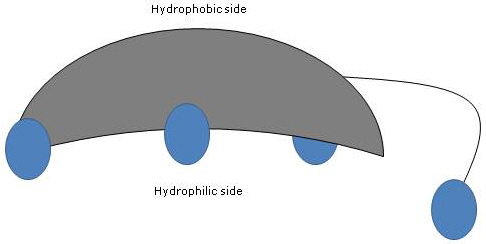
Sillä on siis sekä polaarisia että poolittomia ryhmiä, joten ne ovat amfifiilisiä molekyylejä ja erinomaisia pinta-aktiivisia aineita. Kemiallisen rakenteensa vuoksi ne eroavat kuitenkin monista muista pinta-aktiivisista aineista, sillä ne koostuvat usein poolisesta pääalueesta ja poolittomasta hännästä.
Primääriset, konjugoidut ja sekundääriset sappisuolat
Primääriset sappihapot ovat niitä, jotka syntetisoituvat suoraan kolesterolista hepatosyyteissä. Ihmisellä tärkeimmät ovat kolihappo ja ksenodeoksikolihappo, jotka muodostavat 80 % kaikista sappihapoista. Ennen kuin ne erittyvät sappiteihin, ne konjugoituvat lähes kokonaan, jopa 98-prosenttisesti, glysiinin tai tauriinin kanssa muodostaen vastaavasti glykokonjugaatteja ja taurokonjugaatteja. Erityisesti noin 75 prosenttia koliinihaposta ja kenodeoksikoliinihaposta konjugoituu glysiinin kanssa glykoliinihapoksi ja glykochenodeoksikoliinihapoksi ja loput 25 prosenttia tauriinin kanssa taurokoliinihapoksi ja taurochenodeoksikoliinihapoksi.
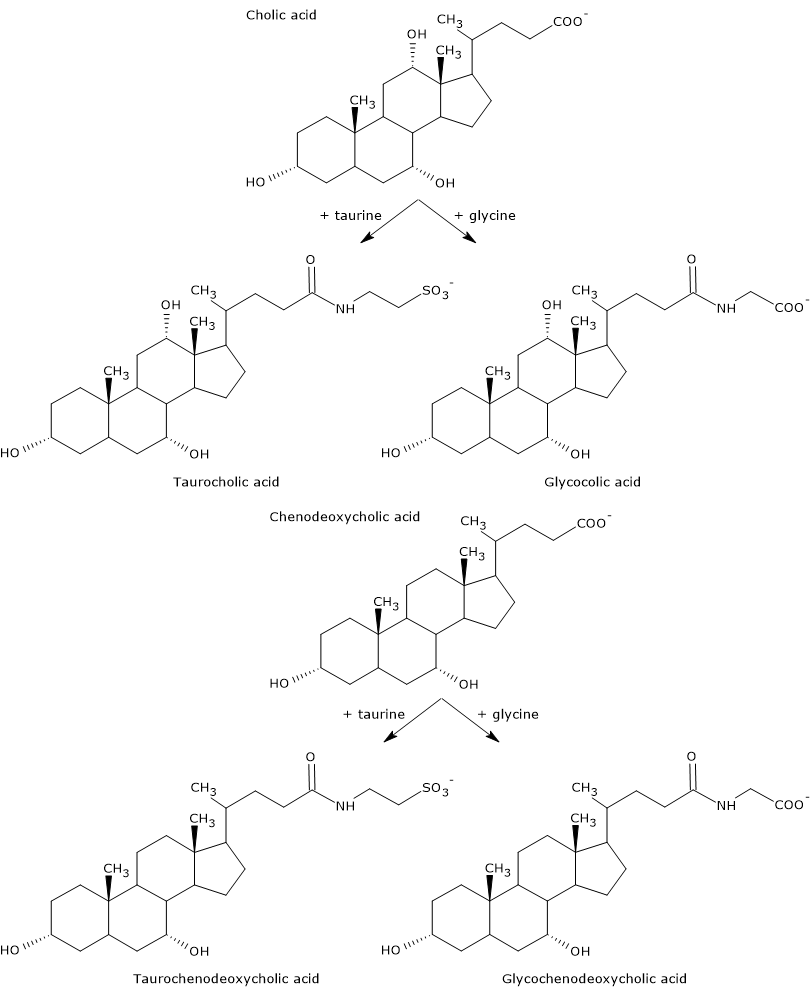
Konjugoidut sappihapot ovat molekyylejä, joissa on enemmän hydrofiilisiä ryhmiä kuin konjugoimattomissa sappihapoissa, minkä vuoksi niiden emulgointikyky on suurempi. Itse asiassa konjugointi laskee sappihappojen pKa:ta noin 6:sta, joka on tyypillinen arvo konjugoimattomille molekyyleille, noin 4:ään glykolihapolle ja noin 2:een taurokolihapolle. Tämä tekee siitä, että konjugoidut sappihapot ionisoituvat laajemmalla pH-alueella muodostaen vastaavia suoloja.
Yleisten happojen ja sappisuolojen hydrofiilisyys vähenee seuraavassa järjestyksessä: glysiinikonjugoitu < tauriinikonjugoitu < litokoliinihappo < deoksikoliinihappo < ksenodeoksikoliinihappo < koliinihappo <ursodeoksikoliinihappo.
Lopuksi konjugointi vähentää myös primaaristen sappihappojen sytotoksisuutta.
Sekundaariset sappihapot muodostuvat primaarisista sappihapoista, jotka eivät ole imeytyneet takaisin ohutsuolesta. Paksusuolessa ne voivat suolistomikrobiston toimesta käydä läpi useita modifikaatioita muodostaen sekundaarisia sappihappoja (ks. jäljempänä). Ne muodostavat loput 20 % elimistön sappihappovarastosta.
Toinen tapa luokitella sappisuolat perustuu niiden konjugoitumiseen glysiinin ja tauriinin kanssa sekä niiden hydroksylaatioasteeseen. Tämän perusteella tunnistetaan kolme luokkaa.
- Trihydroksikonjugaatit, kuten taurokolihappo ja glykolihappo.
- Dihydroksikonjugaatit, kuten glykodeoksikolihappo, glykokeenidodeoksikolihappo, taurokenidodeoksikolihappo ja taurodeoksikolihappo. Niiden osuus sapen sisältämistä sappisuoloista on noin 60 %.
- Konjugoimattomat muodot, kuten koliinihappo, deoksikoliinihappo, kenodeoksikoliinihappo ja litokoliinihappo.
Sappihappojen toiminta
Kaikki niiden fysiologiset toiminnot suoritetaan konjugoituneessa muodossa.
- Sappihapot ovat tärkein reitti kolesterolin poistumisessa ihmiskehosta.
Ihmisellä ei nimittäin ole entsyymejä, jotka pystyisivät hajottamaan steroidin ytimen sykloheksaanirenkaita tai syklopentaanirenkaita eikä hapettamaan kolesterolia CO2:ksi ja vedeksi.
Toinen mekanismi, jolla steroidi poistuu elimistöstä, on kolesteroli sinänsä sapessa. - Sappisuolat ovat vahvoja pinta-aktiivisia aineita. Ja erityisesti di- ja trihydroksikonjugaatit ovat sappihapoista parhaita pinta-aktiivisia aineita, paljon tehokkaampia kuin konjugoimattomat vastineet, koska niissä on enemmän polaarisia ryhmiä.
Kosketuksessa apolaaristen lipidien kanssa ohutsuolen luumenissa kupera apolaarinen pinta on vuorovaikutuksessa apolaaristen lipidien, kuten triglyseridien, kolesteroliestereiden ja rasvaliukoisten vitamiinien esterin kanssa, kun taas kovera polaarinen pinta on vuorovaikutuksessa ympäröivän vesipitoisen väliaineen kanssa. Tämä lisää apolaaristen lipidien dispersiota vesiliuoksessa, koska se mahdollistaa pienten lipidipisaroiden muodostumisen, mikä lisää pinta-alaa:
lipaasiaktiivisuudelle, pääasiassa haiman lipaasille, (sappisuoloilla on myös suora rooli tämän entsyymin aktivoinnissa);
suoliston esteraasiaktiivisuudelle.
Seuraavasti ne helpottavat lipidien pilkkoutumistuotteiden sekä rasvaliukoisten vitamiinien imeytymistä suolen limakalvolla sekamikellien muodostumisen ansiosta.
Sappihapoilla on samanlainen tehtävä sappirakossa, jossa ne muodostamalla sekamikellejä fosfolipidien kanssa estävät kolesterolin saostumista.
Huomautus: Polaaristen ja ei-polaaristen ryhmien järjestelyn seurauksena sappihapot muodostavat vesiliuoksessa mikkeleitä, jotka koostuvat yleensä alle 10 monomeeristä, kunhan niiden konsentraatio on yli niin sanotun kriittisen mikkelikonsentraation eli CMC:n.
- Suoliston tasolla ne moduloivat haimaentsyymien ja kolekystokiniinin eritystä.
- Hieno- ja paksusuolessa niillä, lähinnä deoksikolihapolla, on voimakas antimikrobinen aktiivisuus erityisesti grampositiivisia bakteereja vastaan. Tämä aktiivisuus voi johtua oksidatiivisesta DNA-vauriosta ja/tai solukalvon vaurioitumisesta. Siksi niillä on tärkeä rooli bakteerien liikakasvun ehkäisyssä, mutta myös suoliston mikrobiston koostumuksen säätelyssä.
- Viime vuosina on käynyt ilmeiseksi niiden säätelyrooli energia-aineenvaihdunnan ja erityisesti maksan glukoosinkäsittelyn säätelyssä.
Sappisuolojen enterohepaattinen kierto
Rasvan saannin jälkeen pohjukaissuolen enteroendokriiniset solut erittävät kolekystokiniinia verenkiertoon. Hormoni sitoutuu sappirakon sileiden lihassolujen reseptoreihin ja edistää niiden supistumista; hormoni aiheuttaa myös Oddin sulkijalihaksen rentoutumista. Kaikki tämä johtaa sapen ja siten sappihappojen erittymiseen pohjukaissuoleen.
Fysiologisissa olosuhteissa ihmisen sappisuolavarasto on vakio, ja se on noin 3-5 g. Tämä on mahdollista kahden prosessin ansiosta:
- suolen takaisinimeytyminen;
- de novo -synteesi (ks. jäljempänä).
Jopa 95 % erittyvistä sappisuoloista imeytyy takaisin suolistosta, ei yhdessä lipidien pilkkoutumistuotteiden kanssa, vaan enterohepaattiseksi verenkierroksi kutsutun prosessin kautta.
Se on erittäin tehokas kierrätysjärjestelmä, joka näyttää tapahtuvan vähintään kaksi kertaa jokaista ateriaa kohti, ja se käsittää maksan, sappipuun, ohutsuolen, paksusuolen ja portaaliverenkierron, jonka kautta uudelleen imeytyneet molekyylit palaavat maksaan. Tällainen kierrätys on välttämätöntä, koska maksan kyky syntetisoida sappihappoja on rajallinen ja riittämätön tyydyttämään suoliston tarpeet, jos sappisuoloja erittyisi ulosteeseen suuria määriä.
Suurin osa sappisuoloista imeytyy takaisin distaaliseen ileumiin, ohutsuolen alaosaan, enterosyyttien harjasrajan sisällä olevan natriumrieriippuvaisen kuljettajan eli natriumriippuvaisen sappihappokuljettajan (natrium-dependent bile acid transporter eli ASBT) avulla, joka suorittaa yhden sappihappomolekyylin ja kahden natriumionin yhteiskuljetuksen.
Enterosyytin sisällä sappihappojen uskotaan kulkeutuvan sytosolin läpi basolateraaliselle kalvolle ileaalisen sappihappoa sitovan proteiinin eli IBABP:n avulla. Ne ylittävät basolateraalisen kalvon orgaanisen liuenneen aineen kuljettajan alfa-beetan eli OSTα/OSTβ:n avulla, kulkeutuvat portaaliverenkiertoon ja saavuttavat albumiiniin sitoutuneina maksan.
On huomattava, että pieni osa sappihapoista pääsee maksaan maksavaltimon kautta.
Maksatasolla niiden uuttaminen on hyvin tehokasta, ja ensimmäisen ohituksen uuttamisosuus on 50-90 %:n luokkaa, ja tämä prosenttiosuus riippuu sappihapon rakenteesta. Konjugoitujen sappihappojen ottoa välittää pääasiassa Na+-riippuvainen aktiivinen kuljetusjärjestelmä eli natriumriippuvainen taurokolaatti-kotransportoiva polypeptidi eli NTCP. Voi kuitenkin tapahtua myös natriumista riippumatonta imeytymistä, jota toteuttavat orgaanisia anioneja kuljettavien polypeptidien eli OATP:n perheeseen kuuluvat proteiinit, pääasiassa OATP1B1 ja OATP1B3.
Nopeutta rajoittava vaihe enterohepaattisessa verenkierrossa on niiden kanavaperäinen erittyminen, jota pitkälti välittää ATP-riippuvainen ATP:stä riippuvainen sapensuolojen vientipumppu eli BSEP. Tämä pumppu kuljettaa monoanionisia sappisuoloja, joita on eniten. Glukuronihapon tai sulfaatin kanssa konjugoituneita sappihappoja, jotka ovat dianionisia, kuljettavat erilaiset kuljettajat, kuten MRP2 ja BCRP.
Huomautus: Seerumin sappihappopitoisuudet vaihtelevat sappihappojen takaisinimeytymisnopeuden perusteella, ja siksi ne ovat korkeammat aterioiden aikana, jolloin enterohepaattinen verenkierto on aktiivisempi.
Sappihappojen suolistoaineenvaihdunta
Sappihapot, jotka välttyvät ileaaliselta imeytymiseltä, kulkeutuvat paksusuoleen, jossa ne käyvät osittain läpi suoliston mikrobiston suorittamia modifikaatioita ja muuntuvat sekundaarisiksi sappihapoiksi.
Tärkeimmät reaktiot on lueteltu alla.
- Dekonjugaatio
Sivuketjussa voi tapahtua C24 N-asyyliamidisidoksen hydrolyysi, jolloin vapautuu konjugoimattomia sappihappoja ja glysiiniä tai tauriinia. Tätä reaktiota katalysoivat bakteerihydrolaasit, joita esiintyy sekä ohutsuolessa että paksusuolessa. - 7α-dehydroksylaatio
Kvantitatiivisesti se on tärkein reaktio, jonka suorittavat paksusuolen bakteeridehydraasit, jotka poistavat hydroksyyliryhmän 7-asemassa muodostaen 7-deoksisappihappoja. Erityisesti deoksikolihappoa muodostuu kolihaposta ja litokolihappoa, myrkyllistä sekundaarista sappihappoa, ksenodeoksikolihaposta.
On huomattava, että 7α-dehydroksylaatio, toisin kuin hapettuminen ja epimerisaatio (ks. jäljempänä), voi tapahtua vain konjugoimattomille sappihapoille, joten dekonjugoituminen on olennainen edellytys. - Hapettuminen ja epimerisaatio
Ne ovat reaktioita, joissa ovat osallisina hydroksyyliryhmät paikoissa 3, 7 ja 12 ja joita katalysoivat bakteerien hydroksisteroididehydrogenaasit. Esimerkiksi ursodeoksikolihappo syntyy ksenodeoksikolihapon epimerisaatiosta.
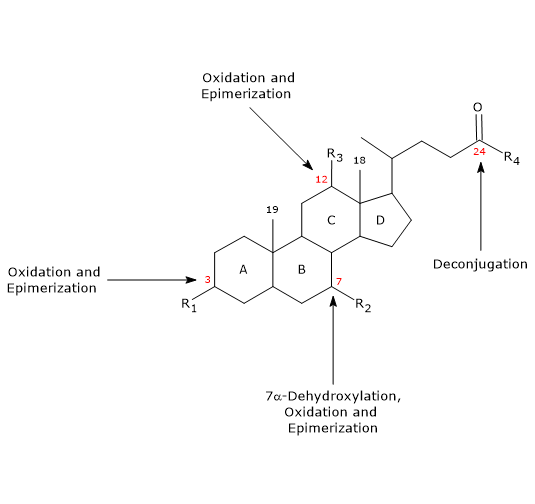
Osa sekundaarisista sappihapoista imeytyy sitten takaisin paksusuolesta ja palaa maksaan. Hepatosyyteissä ne konjugoidaan tarvittaessa uudelleen ja erittyvät uudelleen. Ne, joita ei imeydy takaisin, erittyvät ulosteeseen.
Jos hapetuksesta ja dekonjugoinnista huolehtii laaja kirjo anaerobisia bakteereja, 7α-dehydroksylaatioista huolehtii rajallinen määrä paksusuolen anaerobeja.
7α-dehydroksylaatiot ja dekonjugaatiot lisäävät sappihappojen pKa:ta ja siten niiden hydrofobisuutta, mikä mahdollistaa tietynasteisen passiivisen imeytymisen paksusuolen seinämän läpi.
Hydrofobisuuden lisääntymiseen liittyy myös näiden molekyylien lisääntynyt toksisuus. Ja sekundaaristen sappihappojen suuri pitoisuus sapessa, veressä ja ulosteessa on yhdistetty paksusuolasyövän patogeneesiin.
Liukoiset kuidut ja sappisuolojen takaisinimeytyminen
Sappisuolojen takaisinimeytymistä voidaan vähentää liukoisten kuitujen, kuten tuoreissa hedelmissä, palkokasveissa, kaurassa ja kauraleseissä esiintyvien kuitujen kelatoivalla vaikutuksella, sillä ne sitovat niitä ja vähentävät niiden imeytymistä. Tämä puolestaan lisää sappihappojen de novo -synteesiä, mikä säätelee 7α-hydroksylaasin ja steroli 12α-hydroksylaasin (ks. jäljempänä) ilmentymistä ylöspäin, ja siten pienentää hepatosyyttien kolesterolipitoisuutta.
Hepaattisen kolesterolin ehtyminen lisää LDL-reseptorin ilmentymistä ja siten pienentää LDL-kolesterolin pitoisuutta plasmassa. Toisaalta se myös stimuloi HMG-CoA-reduktaasin, kolesterolin biosynteesin avainentsyymin, synteesiä.
Huomautus: Jotkin kolesterolilääkkeet vaikuttavat sitomalla sappihappoja suolistossa ja estämällä siten niiden takaisinimeytymisen.
Primääristen sappihappojen synteesi
Kvantitatiivisesti tarkasteltuna sappihapot ovat kolesterolimetabolian päätuote.
Kuten aiemmin sanottiin, enterohepaattinen kierto ja niiden de novo -synteesi ylläpitävät sappihappopoolin kokoa vakiona. Erityisesti de novo -synteesi mahdollistaa kasvojen kautta erittyvien sappisuolojen korvaamisen, noin 5-10 % elimistön sappivarastosta, eli ~ 0,5 g/vrk.
Alhaalla kuvataan kolihapon ja ksenodeoksikolihapon synteesiä ja niiden konjugointia aminohappojen tauriinin ja glysiinin kanssa.
Sappihappojen synteesissä on kaksi pääreittiä: klassinen ja vaihtoehtoinen reitti. Lisäksi kuvataan joitakin muita pienempiä reittejä.
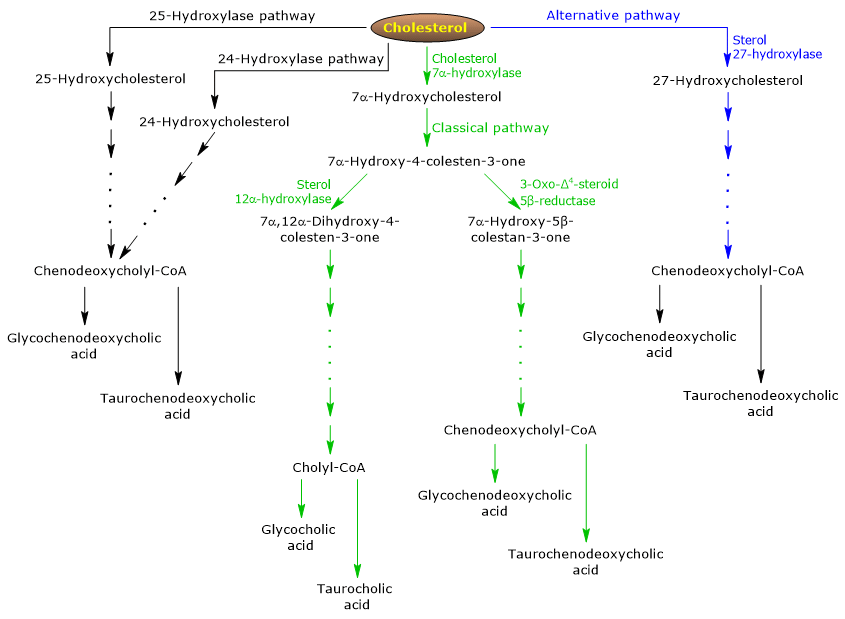
Klassinen tai neutraali reitti
Ihmisillä jopa 90 % sappisuoloista tuotetaan klassisen reitin (ks. kuvio 5) kautta, jota kutsutaan myös neutraaliksi reitiksi, koska välituotteet ovat neutraaleja molekyylejä.
Se on vain maksassa esiintyvä aineenvaihduntareitti, joka koostuu reaktioista, joita katalysoivat sytosoliin, endoplasmiseen retikulumiin, peroksisomeihin ja mitokondrioihin lokalisoituneet entsyymit, ja jonka lopputuotteet ovat kolihapon ja ksenodeoksikolihapon konjugaatit.
- Ensimmäinen reaktio on hydroksylaatio 7-alkuisen aseman kohdalla, jolloin muodostuu 7α-hydroksikolesterolia. Reaktiota katalysoi kolesterolin 7α-hydroksylaasi eli CYP7A1 (E.C. 1.14.14.23). Se on endoplasmisessa retikulumissa sijaitseva entsyymi, joka katalysoi reitin nopeutta rajoittavan vaiheen.
Kolesteroli + NADPH + H+ + O2 → 7α-hydroksikolesteroli + NADP+ + H2O
- 7α-hydroksikolesteroli hapettuu 3β-hydroksyyliryhmän hapettumisessa ja kaksoissidoksen siirtymisessä 5,6-asennosta 4,5-asentoon muodostaen 7α-hydroksi-4-kolesten-3-onin. Reaktiota katalysoi 3β-hydroksi-Δ5-C27-steroidioksidoreduktaasi eli HSD3B7 (E.C. 1.1.1.181), joka on endoplasmisessa retikulumissa sijaitseva entsyymi.
- 7α-hydroksi-4-kolesten-3-oni voi kulkea kahta reittiä:
pääsy polulle, joka johtaa kolihapon synteesiin, reaktion kautta, jota katalysoi 7α-hydroksi-4-kolesten-3-onin 12α-monooksygenaasi tai sterolin 12α-hydroksylaasi eli CYP8B1 (E.C. 1.14.18.8), joka on endoplasmiseen retikulumiin lokalisoitunut entsyymi;
pääsemään reittiin, joka johtaa ksenodeoksikolihapon synteesiin 3-okso-Δ4-steroidi 5β-reduktaasin eli AKR1D1:n katalysoiman reaktion kautta (E.C. 1.3.2.1.3), joka on sytosolinen entsyymi.
On korostettava, että steroli 12α-hydroksylaasin aktiivisuus määrittää kolihapon ja kenodeoksikolihapon välisen suhteen ja viime kädessä sappihappopoolin detergenttikapasiteetin. Ja itse asiassa steroli 12α-hydroksylaasigeenin transkription säätely on yksi klassisen reitin tärkeimmistä säätelyvaiheista.
Jos siis 7α-hydroksi-4-kolesten-3-oni etenee steroli 12α-hydroksylaasin katalysoiman reaktion kautta, tapahtuvat seuraavat reaktiot.
- 7α-Hydroksi-4-kolesten-3-oni hydroksyloidaan steroli 12α-hydroksylaasin toimesta 12-asemassa muodostaen 7α,12α-dihydroksi-4-kolesten-3-onia.
- 7α,12α-Dihydroksi-4-kolesten-3-oni pelkistyy 4,5-aseman kaksoissidoksessa 3-okso-Δ4-steroidi 5β-reduktaasin katalysoimassa reaktiossa muodostaen 5β-kolestan-7α,12α-diol-3-onia.
- 5β-kolestan-7α,12α-diol-3-oni pelkistyy 4-asennossa olevan hydroksyyliryhmän pelkistyksessä 3α-hydroksisteroididehydrogenaasin eli AKR1C4:n (EC 1.1.1.1.213), joka on sytosolinen entsyymi, muodostaen 5β-kolestan-3α,7α,12α-triolia.
- 5β-kolestan-3α,7α,12α,12α-trioli käy läpi sivuketjun hapettumisen kolmessa reaktiossa, joita katalysoi steroli-27-hydroksylaasi eli CYP27A1 (EC 1.14.15.15). Kyseessä on mitokondriaalinen entsyymi, jota esiintyy myös ekstrahepaattisissa kudoksissa ja makrofageissa, ja se tuo hydroksyyliryhmän asemaan 27. Hydroksyyliryhmä hapettuu aldehydiksi ja sitten karboksyylihapoksi muodostaen 3α,7α,12α-trihydroksi-5β-kolestanohappoa.
- 3α,7α,12α-trihydroksi-5β-kolestanohappo aktivoituu sen koentsyymi A -esteriksi, 3α,7α,12α-trihydroksi-5β-kolestanoyyli-CoA:ksi, reaktiossa, jota katalysoi joko hyvin pitkäketjuinen asyyli-CoA-syntetaasi eli VLCS (EC 6.2.1.1.-) tai sappihappo-CoA-syntetaasi eli BACS (EC 6.2.1.7), jotka molemmat sijaitsevat endoplasmisessa retikulumissa.
- 3α,7α,12α-trihydroksi-5β-kolestanoyyli-CoA kuljetetaan peroksisomeihin, joissa se käy läpi viisi peräkkäistä reaktiota, joista kutakin katalysoi eri entsyymi. Kahdessa viimeisessä reaktiossa sivuketju lyhenee neljään hiiliatomiin, ja lopulta muodostuu kolyyliCoA.
- Viimeisessä vaiheessa tapahtuu sivuketjun karboksyylihapporyhmän konjugoituminen amidisidoksen kautta aminohappo glysiinin tai tauriinin kanssa. Reaktiota katalysoi sappihappo-CoA:aminohappo N-asyltransferaasi eli BAAT (EC 2.3.1.65), joka on lokalisoitunut pääasiassa peroksisomeihin.
Reaktiotuotteet ovat siis konjugoituneita sappihappoja: glykolihappoa ja taurokolihappoa.
Jos 7α-hydroksi-4-kolesten-3-oni ei etene steroli 12α-hydroksylaasin katalysoiman reaktion kautta, se siirtyy reittiin, joka johtaa ksenodeoksikolihappokonjugaattien synteesiin jäljempänä kuvattujen reaktioiden kautta.
- 7α-Hydroksi-4-kolesten-3-oni muuttuu 3-okso-Δ4-steroidi 5β-reduktaasin katalysoimassa reaktiossa 7α-hydroksi-5β-kolestan-3-ooniksi.
- 7α-Hydroksi-5β-kolestan-3-oni muuttuu 3α-hydroksisteroididehydrogenaasin katalysoimassa reaktiossa 5β-kolestan-3α,7α-dioliksi.
Sitten konjugoituneet sappihapot glykokeenidodeoksikolihappo ja taurokenidodeoksikolihappo muodostuvat samanlaisilla modifikaatioilla kuin kolihapon konjugaatiossa, ja niitä katalysoivat enimmäkseen samat entsyymit.
Huomautus: Suolistossa muodostuvien konjugoimattomien sappihappojen on päästävä maksaan uudelleen konjugoitumaan.
Vaihtoehtoinen tai hapan reitti
Se on yleinen sikiöillä ja vastasyntyneillä, kun taas aikuisilla se johtaa alle 10 %:n osuuden sappisuolojen synteesiin.
Tämä reitti (ks. kuv. 5) eroaa klassisesta reitistä siinä, että:
- välituotteet ovat happamia molekyylejä, mistä vaihtoehtoinen nimi ”hapan reitti”;
- sivuketjun hapettumista seuraa steroidin ytimen modifikaatio eikä päinvastoin;
- lopputuotteet ovat ksenodeoksikolihapon konjugaatteja.
Ensimmäisessä vaiheessa kolesteroli muuttuu 27-hydroksikolesteroliksi reaktiossa, jota katalysoi steroli-27-hydroksylaasi.
27-hydroksikolesteroli voi kulkea kahta reittiä.
Reitti A
- 27-hydroksikolesteroli muuttuu 3β-hydroksi-5-kolesteenihapoksi reaktiossa, jota katalysoi steroli-27-hydroksylaasi.
- 3β-hydroksi-5-kolesteenihappo hydroksyloidaan 7-asemassa reaktiossa, jota katalysoi endoplasmiseen retikulumiin lokalisoitunut entsyymi oksysteroli-7α-hydroksylaasi eli CYP7B1 (EC 1.14.13.100), muodostaen 3β-7α-dihydroksi-5-kolesteenihappoa.
- 3β-7α-dihydroksi-5-kolesteenihappo muuttuu 3-okso-7α-hydroksi-4-kolesteenihapoksi reaktiossa, jota katalysoi 3β-hydroksi-Δ5-C27-steroidioksidoreduktaasi.
- 3-Okso-7α-hydroksi-4-kolesteenihappo muodostaa sivuketjumodifikaatioiden seurauksena ksenodeoksikoliinihappoa ja sen jälkeen sen konjugaatit.
Reitti B
- 27-Hydroksikolesteroli muuttuu 7α,27-dihydroksikolesteroliksi reaktiossa, jota katalysoivat oksysteroli-7α-hydroksylaasi ja kolesteroli-7α-hydroksylaasi.
- 7α,27-dihydroksikolesteroli muuttuu 7α,26-dihydroksi-4-kolesten-3-ooniksi 3β-hydroksi-Δ5-C27-steroidioksidoreduktaasin katalysoimassa reaktiossa;
7α,26-Dihydroksi-4-kolesten-3-oni voidaan muuntaa suoraan kenodeoksikolihapon konjugaateiksi tai se voidaan muuntaa 3-okso-7α-hydroksi-4-kolesteenihapoksi, minkä jälkeen se käy läpi sivuketjumodifikaatioita ja muita reaktioita, jotka johtavat kenodeoksikolihapon konjugaattien synteesiin.
Pienemmät reitit
On myös pienempiä reittejä (ks. kuva 5), jotka osallistuvat sappisuolojen synteesiin, vaikkakin vähäisemmässä määrin kuin klassiset ja vaihtoehtoiset reitit.
Esimerkiksi:
- Kolesteroli-25-hydroksylaasi (EC 1.14.99.38) ilmentyy maksassa.
- Kolesterolin 24-hydroksylaasi eli CYP46A1 (EC 1.14.14.25) ilmentyy aivoissa, ja näin ollen, vaikka elimistö ei voi viedä kolesterolia, se vie oksysteroleja.
- Epäspesifinen 7α-hydroksylaasi on myös löydetty. Se ilmentyy kaikissa kudoksissa, ja se näyttää osallistuvan oksysterolien tuottamiseen, jotka voidaan kuljettaa hepatosyytteihin muunnettavaksi ksenodeoksikolihapoksi.
Lisäksi steroli-27-hydroksylaasi ilmentyy eri kudoksissa, ja siksi sen reaktiotuotteet on kuljetettava maksaan muunnettavaksi sappisuoloiksi.
Sappisuolat: synteesin säätely
Sappihapposynteesin säätely tapahtuu negatiivisen takaisinkytkentämekanismin kautta erityisesti kolesteroli-7α-hydroksylaasin ja steroli-12α-hydroksylaasin ilmentymiseen.
Kun sappihappoja, sekä vapaita että konjugoituja, on liikaa, nämä molekyylit sitoutuvat ydinreseptoriin farnesoidi X-reseptoriin eli FRX:ään ja aktivoivat sen: tehokkain sappihappo on ksenodeoksikolihappo, kun taas muut, kuten ursodeoksikolihappo, eivät aktivoi sitä.
FRX indusoi transkriptionaalisen repressorin small heterodimer partner eli SHP:n ilmentymistä, joka puolestaan on vuorovaikutuksessa muiden transkriptiotekijöiden, kuten maksareseptorihomolog-1:n eli LRH-1:n ja hepatosyyttien ydintekijä-4α:n eli HNF-4α:n kanssa. Nämä transkriptiotekijät sitoutuvat 7α-hydroksylaasi- ja 12α-hydroksylaasigeenien promoottorialueella olevaan sekvenssiin, aluetta kutsutaan sappihappovaste-elementiksi eli BARE:ksi, ja estävät niiden transkriptiota.
Yksi syy siihen, miksi sappisuolojen synteesiä säädellään tiukasti, on se, että monet niiden aineenvaihduntatuotteista ovat myrkyllisiä.
Chiang J. Y. L. Bile acids: regulation of synthesis. J Lipid Res 2009;50(10):1955-66. doi:10.1194/jlr.R900010-JLR200
Gropper S.S., Smith J.L. Advanced nutrition and human metabolism. 6h painos. Cengage Learning, 2012
Moghimipour E., Ameri A. ja Handali S. Sappisuolojen imeytymistä tehostavat vaikutukset. Molecules 2015;20(8); 14451-73. doi:10.3390/molecules200814451
Monte M.J., Marin J.J.G., Antelo A., Vazquez-Tato J. Bile acids: Chemistry, physiology, and pathophysiology. World J Gastroenterol 2009;15(7):804-16. doi:10.3748/wjg.15.804
Rawn J.D. Biochimica. Mc Graw-Hill, Neil Patterson Publishers, 1990
Rosenthal M.D., Glew R.H. Medical biochemistry – Human metabolism in health and disease. John Wiley J. & Sons, Inc. julkaisu, 2009
Sundaram S.S., Bove K.E., Lovell M.A. ja Sokol R.J. Mechanisms of Disease: Inborn errors of bile acid synthesis. Nat Clin Pract Gastroenterol Hepatol 2008;5(8):456-68. doi:10.1038/ncpgasthep1179