Gallsalter och gallsyror är polära kolesterolderivat och utgör den viktigaste vägen för eliminering av steroiden från kroppen.
De är molekyler med liknande men inte identiska strukturer och olika fysiska och biologiska egenskaper.
De syntetiseras i levern, lagras i gallblåsan, utsöndras i tolvfingertarmen och slutligen, till största delen, återabsorberas de i ileum.
Eftersom dessa molekyler vid fysiologiskt pH föreligger som anjoner används termerna gallsyra och gallsalter här som synonymer.
INNEHÄLLEN
- Kemisk struktur hos gallsalter
- Primär, konjugerade och sekundära gallsalter
- Gallsyrornas funktion
- Enterohepatisk cirkulation av gallsalter
- Intestinal metabolism av gallsyror
- Lösliga fibrer och reabsorption. av gallsalter
- Syntes av primära gallsyror
- Den klassiska eller neutrala vägen
- Den alternativa eller sura vägen
- Mindre vägar
- Gallsalter: Reglering av syntesen
- Gallesalts kemiska struktur
- Primära, konjugerade och sekundära gallsalter
- Gallsyrornas funktion
- Enterohepatisk cirkulation av gallsalter
- Intestinal metabolism av gallsyror
- Lösliga fibrer och reabsorption av gallsalter
- Syntes av primära gallsyror
- Den klassiska eller neutrala vägen
- Den alternativa eller sura vägen
- Mindre vägar
- Gallsalter: reglering av syntesen
Gallesalts kemiska struktur
Gallesalter har likheter och skillnader med kolesterolmolekylen.
Likt steroid har de en kärna som består av fyra fusionerade ringar: tre cyklohexanringar, märkta A, B och C, och en cyklopentanring, märkt D. Denna struktur är perhydrocyklopentanofenanthren, mer allmänt känd som steroidkärna.
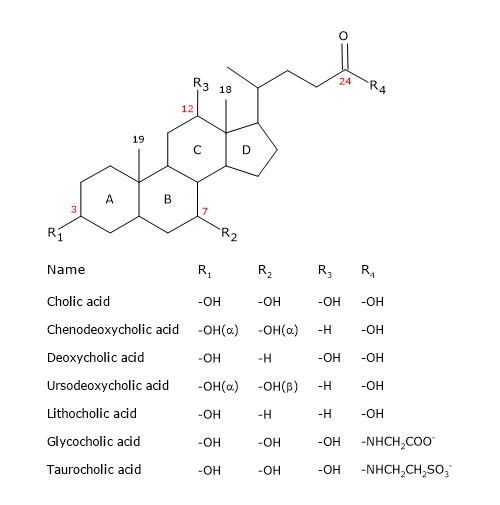
I högre ryggradsdjur har de 24 kolatomer, eftersom sidokedjan är tre kolatomer kortare än den ursprungliga. Hos lägre ryggradsdjur har gallsyrorna 25, 26 eller 27 kolatomer. Sidokedjan avslutas med en karboxylgrupp, joniserad vid pH 7, som kan kopplas till aminosyran glycin eller taurin (se nedan).
Inom hydroxylgruppen i position 3 har de hydroxylgrupper i positionerna 7 och/eller 12.
Allt detta gör dem mycket mer polära än kolesterol.
Då A- och B-ringarna är fusionerade i cis-konfiguration är steroidkärnans plana struktur krökt, och det är möjligt att identifiera:
- en konkav sida, som är hydrofil eftersom hydroxylgrupperna och karboxylgruppen i sidokedjan, med eller utan den länkade aminosyran, är orienterade mot den;
- en konvex sida, som är hydrofob eftersom metylgrupperna som finns i position 18 och 19 är orienterade mot den.
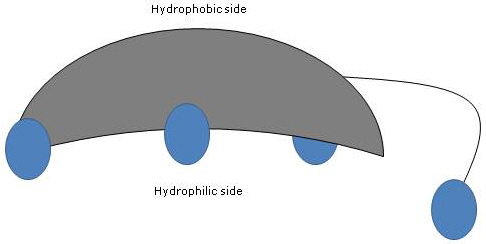
Därmed har de både polära och opolära grupper och är amfifila molekyler och utmärkta ytaktiva ämnen. Deras kemiska struktur gör dock att de skiljer sig från många andra ytaktiva ämnen, som ofta består av ett polärt huvudområde och en opolär svans.
Primära, konjugerade och sekundära gallsalter
Primära gallsyror är de som syntetiseras direkt från kolesterol i hepatocyterna. Hos människor är de viktigaste kolsyra och chenodeoxikolsyra, som utgör 80 % av alla gallsyror. Innan de utsöndras i gallträdet konjugeras de nästan helt, upp till 98 %, med glycin eller taurin för att bilda glykokonjugat respektive taurokonjugat. I synnerhet konjugeras cirka 75 % av kolsyra och chenodeoxikolsyra med glycin för att bilda glykokolsyra och glykochenodeoxikolsyra, medan de återstående 25 % konjugeras med taurin för att bilda taurokolsyra och taurochenodeoxikolsyra.
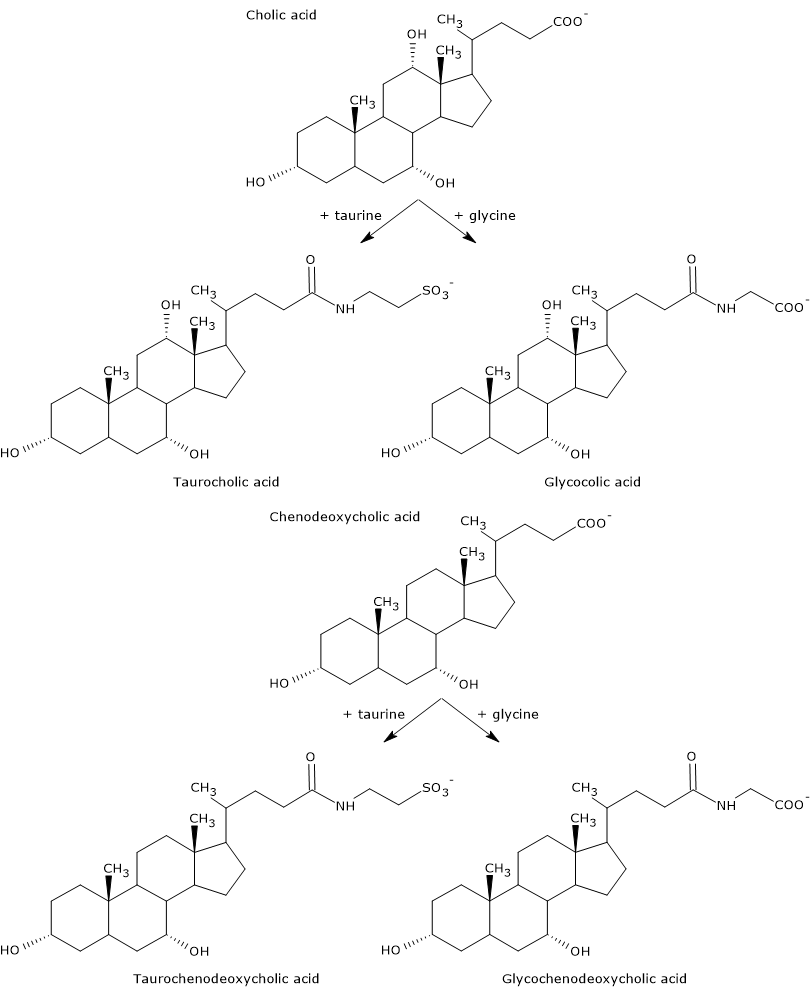
Konjugerade gallsyror är molekyler med fler hydrofila grupper än okonjugerade gallsyror och har därför en ökad emulgeringsförmåga. Konjugering minskar faktiskt gallsyrornas pKa från cirka 6, ett värde som är typiskt för okonjugerade molekyler, till cirka 4 för glykokolsyra och cirka 2 för taurokolsyra. Detta gör att konjugerade gallsyror joniseras i ett bredare pH-område för att bilda motsvarande salter.
Hydrofiliteten hos de vanliga syra- och gallsalterna minskar i följande ordning: glycinkonjugerad < taurinkonjugerad < lithokolsyra < deoxokolsyra < chenodeoxokolsyra < choksyra <ursodeoxokolsyra.
För det sista minskar konjugeringen också cytotoxiciteten hos primära gallsyror.
Sekundära gallsyror bildas av primära gallsyror som inte har återabsorberats från tunntarmen. När de väl når tjocktarmen kan de genomgå flera modifieringar av tarmmikrobiota för att bilda sekundära gallsyror (se nedan). De utgör de resterande 20 % av kroppens gallsyrepool.
Ett annat sätt att kategorisera gallsalter är baserat på deras konjugering med glycin och taurin och deras grad av hydroxylering. På denna grund identifieras tre kategorier.
- Trihydroxykonjugat, t.ex. taurokolsyra och glykokolsyra.
- Dihydroxykonjugat, t.ex. glykodexokolsyra, glykochenodeoxokolsyra, taurochenodeoxokolsyra och taurodeoxokolsyra. De utgör cirka 60 % av de gallsalter som finns i gallan.
- Okonjugerade former, t.ex. kolsyra, deoxikolsyra, chenodeoxikolsyra och litokolsyra.
Gallsyrornas funktion
Alla deras fysiologiska funktioner utförs i den konjugerade formen.
- De är den viktigaste vägen för eliminering av kolesterol från människokroppen.
Människan har nämligen inte de enzymer som kan bryta upp cyklohexanringarna eller cyklopentanringen i steroidkärnan och inte heller oxidera kolesterol till CO2 och vatten.
Den andra mekanismen för att eliminera steroiden från kroppen är som kolesterol i sig självt i gallan. - Gallesalter är starka ytaktiva ämnen. Och i synnerhet är di- och trihydroxykonjugater de bästa tensiderna bland gallsyrorna, mycket effektivare än okonjugerade motsvarigheter, eftersom de har fler polära grupper.
När de väl kommer i kontakt med apolära lipider i tunntarmens lumen interagerar den konvexa apolära ytan med de apolära lipiderna, t.ex. triglycerider, kolesterolestrar och estrar av fettlösliga vitaminer, medan den konkava polära ytan interagerar med det omgivande vattenhaltiga mediet. Detta ökar spridningen av apolära lipider i det vattenhaltiga mediet, eftersom det möjliggör bildandet av små lipiddroppar, vilket ökar ytan för:
lipasaktivitet, främst pankreaslipas, (gallsalter spelar också en direkt roll i aktiveringen av detta enzym);
intestinal esterasaktivitet.
Följaktligen underlättar de absorptionen av lipidsmältningsprodukter samt av fettlösliga vitaminer av tarmslemhinnan tack vare bildandet av blandade miceller.
Gallsyror fyller en liknande funktion i gallblåsan där de, genom att bilda blandade miceller med fosfolipider, förhindrar utfällning av kolesterol.
Anmärkning: Till följd av arrangemanget av polära och opolära grupper bildar gallsyror miceller i vattenlösning, som vanligen består av mindre än 10 monomerer, så länge deras koncentration ligger över den så kallade kritiska micellära koncentrationen eller CMC.
- På tarmnivå modulerar de sekretionen av pankreasenzymer och cholecystokinin.
- I tunn- och tjocktarmen har de en potent antimikrobiell aktivitet, främst deoxycholsyra, särskilt mot grampositiva bakterier. Denna aktivitet kan bero på oxidativ DNA-skada och/eller skada på cellmembranet. Därför spelar de en viktig roll i förebyggande av bakteriell överväxt, men också i regleringen av sammansättningen av tarmmikrobiota.
- Under de senaste åren har det blivit uppenbart att de har en reglerande roll i kontrollen av energimetabolismen, och i synnerhet för den hepatiska glukoshanteringen.
Enterohepatisk cirkulation av gallsalter
Efter fettintag utsöndrar enteroendokrina celler i duodenum cholecystokinin i blodet. Hormonet som binder till receptorer på glatta muskelceller i gallblåsan främjar deras sammandragning; hormonet orsakar också en avslappning av Oddis sfinkter. Allt detta resulterar i utsöndring av gallan och därmed av gallsyror i duodenum.
Under fysiologiska förhållanden är människans gallsaltsreservoar konstant och motsvarar cirka 3-5 g. Detta möjliggörs av två processer:
- deras tarmreabsorption;
- deras de novo-syntes (se nedan).
Upp till 95 % av de utsöndrade gallsalterna återabsorberas från tarmen, inte tillsammans med produkterna från fettspjälkningen, utan genom en process som kallas enterohepatisk cirkulation.
Det är ett extremt effektivt återvinningssystem som tycks inträffa minst två gånger för varje måltid och som omfattar levern, gallträdet, tunntarmen, tjocktarmen och portalcirkulationen, genom vilken de återabsorberade molekylerna återgår till levern. En sådan recirkulation är nödvändig eftersom leverns kapacitet att syntetisera gallsyror är begränsad och otillräcklig för att tillgodose tarmens behov om gallsalterna skulle utsöndras i stora mängder i avföringen.
De flesta gallsalter återabsorberas till distala ileum, tunntarmens nedre del, av en natriumberoende transportör i borstkanten av enterocyterna, kallad natriumberoende gallsyretransportör (sodium-dependent bile acid transporter eller ASBT), som utför kotransporten av en molekyl gallsyra och två natriumjoner.
Inom enterocyten tror man att gallsyror transporteras över cytosolen till det basolaterala membranet av det ileala gallsyrabindande proteinet eller IBABP. De korsar det basolaterala membranet genom den organiska lösningstransportören alfa-beta eller OSTα/OSTβ, passerar in i portalcirkulationen och når, bundna till albumin, levern.
Det bör noteras att en liten procentandel av gallsyrorna når levern via leverartären.
En levernivå är deras extraktion mycket effektiv, med en första passage-extraktionsfraktion som ligger mellan 50 och 90 %, en procentsats som beror på gallsyrans struktur. Upptaget av konjugerade gallsyror förmedlas huvudsakligen av ett Na+ -beroende aktivt transportsystem, det vill säga den natriumberoende taurokolatkotransporterande polypeptiden eller NTCP. Ett natriumoberoende upptag kan dock också förekomma, vilket utförs av proteiner ur familjen organiska anjontransporterande polypeptider eller OATP, främst OATP1B1 och OATP1B3.
Det hastighetsbegränsande steget i den enterohepatiska cirkulationen är deras kanalikulära sekretion, som till stor del förmedlas av gallsaltsexportpumpen eller BSEP, i en ATP-beroende process. Denna pump transporterar monoanjoniska gallsalter, som är de mest rikliga. Gallsyror som är konjugerade med glukuronsyra eller sulfat, som är dianjoniska, transporteras av olika transportörer, t.ex. MRP2 och BCRP.
Anmärkning: Serumnivåerna av gallsyror varierar på grundval av hastigheten för deras reabsorption och är därför högre under måltider, när den enterohepatiska cirkulationen är mer aktiv.
Intestinal metabolism av gallsyror
Gallsyror som undgår ileal absorption passerar in i tjocktarmen där de delvis genomgår modifieringar av tarmmikrobiota och omvandlas till sekundära gallsyror.
De viktigaste reaktionerna anges nedan.
- Dekonjugering
På sidokedjan kan hydrolys av C24 N-acylamidbindningen ske, med frisättning av okonjugerade gallsyror och glycin eller taurin. Denna reaktion katalyseras av bakteriella hydrolaser som finns både i tunntarmen och i tjocktarmen. - 7α-Dehydroxylering
Kvantitativt sett är det den viktigaste reaktionen, som utförs av bakteriella dehydrataser i tjocktarmen som avlägsnar hydroxylgruppen i position 7 för att bilda 7-deoxy gallsyror. I synnerhet bildas deoxikolsyra från kolsyra och litokolsyra, en giftig sekundär gallsyra, från chenodeoxikolsyra.
Det bör noteras att 7α-dehydroxylering, till skillnad från oxidation och epimerisering (se nedan), endast kan ske på okonjugerade gallsyror, och därför är dekonjugering en viktig förutsättning. - Oxidation och epimerisering
Dessa är reaktioner som involverar hydroxylgrupperna i positionerna 3, 7 och 12 och som katalyseras av bakteriella hydroxysteroiddehydrogenaser. Till exempel härrör ursodeoxykolsyra från epimerisering av chenodeoxykolsyra.
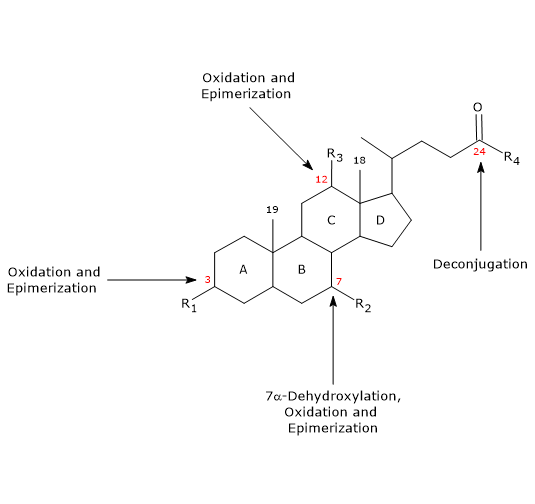
En del av de sekundära gallsyrorna reabsorberas sedan från tjocktarmen och återvänder till levern. I hepatocyterna omkonjugeras de vid behov och utsöndras på nytt. De som inte återabsorberas utsöndras i avföringen.
Och medan oxidationer och dekonjugationer utförs av ett brett spektrum av anaeroba bakterier, utförs 7α-dehydroxyleringar av ett begränsat antal anaeroba bakterier i kolon.
7α-dehydroxyleringar och dekonjugeringar ökar gallsyrornas pKa och därmed deras hydrofobicitet, vilket möjliggör en viss grad av passiv absorption genom kolonväggen.
Ökningen av hydrofobiciteten är också förknippad med en ökad toxicitet hos dessa molekyler. Och en hög koncentration av sekundära gallsyror i galla, blod och avföring har förknippats med patogenesen för tjocktarmscancer.
Lösliga fibrer och reabsorption av gallsalter
Reabsorptionen av gallsalter kan minskas genom kelatbildande verkan av lösliga fibrer, som de som finns i färska frukter, baljväxter, havre och havrekli, som binder dem, vilket minskar deras upptag. Detta ökar i sin tur gallsyra de novo-syntesen genom att uppreglera uttrycket av 7α-hydroxylas och sterol 12α-hydroxylas (se nedan) och minskar därmed hepatocytkolesterolkoncentrationen.
Den utarmning av hepatiskt kolesterol ökar uttrycket av LDL-receptorn och minskar därmed plasmakoncentrationen av LDL-kolesterol. Å andra sidan stimulerar det också syntesen av HMG-CoA-reduktas, nyckelenzym i kolesterolbiosyntesen.
Notera: Vissa antikolesterolläkemedel verkar genom att binda gallsyror i tarmen och därmed förhindra deras reabsorption.
Syntes av primära gallsyror
Kvantitativt sett är gallsyror den viktigaste produkten av kolesterolmetabolismen.
Som tidigare nämnts upprätthåller den enterohepatiska cirkulationen och deras de novo-syntes en konstant gallsyrepoolstorlek. I synnerhet gör de novo-syntesen det möjligt att ersätta de gallsalter som utsöndras i ansiktena, cirka 5-10 % av kroppspoolen, nämligen ~ 0,5 g/dag.
Nedan beskrivs syntesen av kolsyra och chenodeoxikolsyra och deras konjugering med aminosyrorna taurin och glycin.
Det finns två huvudsakliga vägar för gallsyrasyntesen: den klassiska vägen och den alternativa vägen. Dessutom kommer några andra mindre viktiga vägar att beskrivas.
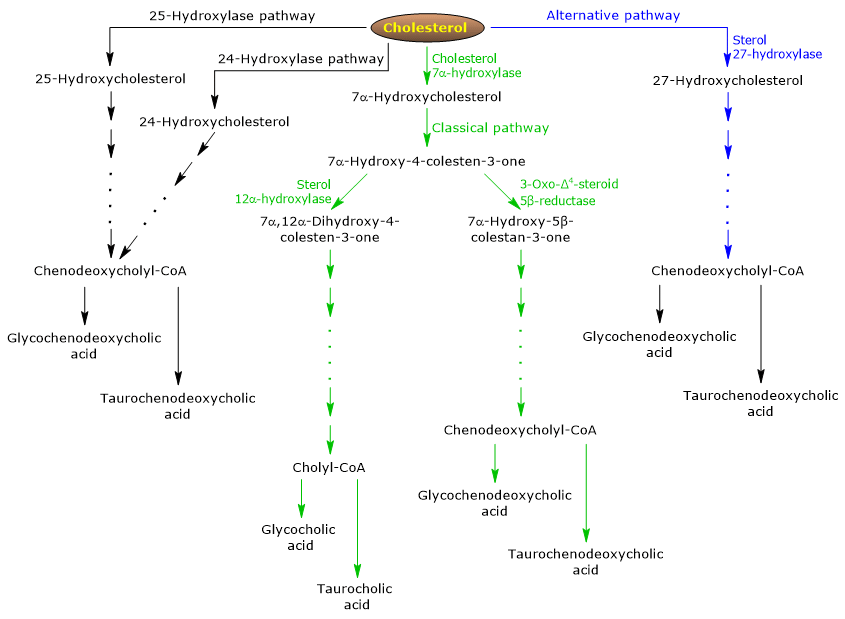
Den klassiska eller neutrala vägen
I människor produceras upp till 90 % av gallsalterna via den klassiska vägen (se fig. 5), som också kallas ”neutral” väg eftersom intermediärerna är neutrala molekyler.
Det är en metabolisk väg som endast finns i levern och som består av reaktioner som katalyseras av enzymer lokaliserade i cytosol, endoplasmatiskt retikulum, peroxisomer och mitokondrier, och vars slutprodukter är konjugat av kolsyra och chenodeoxikolsyra.
- Den första reaktionen är hydroxylering i kolesterolets position 7, för att bilda 7α-hydroxykolesterol. Reaktionen katalyseras av kolesterol 7α-hydroxylas eller CYP7A1 (E.C. 1.14.14.23). Det är ett enzym som är lokaliserat i det endoplasmatiska retikulumet och katalyserar det hastighetsbegränsande steget i vägen.
Colesterol + NADPH + H+ + O2 → 7α-Hydroxykolesterol + NADP+ + H2O
- 7α-Hydroxykolesterol genomgår oxidation av 3β-hydroxylgruppen och förskjutning av dubbelbindningen från positionen 5,6 till positionen 4,5, för att bilda 7α-hydroxi-4-kolesten-3-on. Reaktionen katalyseras av 3β-hydroxy-Δ5-C27-steroidoxidoreduktas eller HSD3B7 (E.C. 1.1.1.1.181), ett enzym lokaliserat i det endoplasmatiska retikulumet.
- 7α-hydroxi-4-kolesten-3-on kan följa två vägar:
att gå in i den väg som leder till syntesen av kolsyra, genom den reaktion som katalyseras av 7α-hydroxi-4-kolesten-3-on 12α-monooxygenas eller sterol 12α-hydroxylas eller CYP8B1 (E.C. 1.14.18.8), ett enzym lokaliserat i det endoplasmatiska retikulumet;
att gå in i den väg som leder till syntesen av chenodeoxycholsyra, genom den reaktion som katalyseras av 3-oxo-Δ4-steroid 5β-reduktas eller AKR1D1 (E.C. 1.3.1.3), ett cytosoliskt enzym.
Det bör understrykas att aktiviteten hos sterol 12α-hydroxylas bestämmer förhållandet mellan kolsyra och chenodeoxikolsyra, och i slutändan gallsyrapoolens detergentkapacitet. Och i själva verket är regleringen av sterol 12α-hydroxylasets gentranskription ett av de viktigaste reglerande stegen i den klassiska vägen.
Om 7α-hydroxi-4-kolesten-3-on går via den reaktion som katalyseras av sterol 12α-hydroxylas kommer därför följande reaktioner att inträffa.
- 7α-hydroxi-4-kolesten-3-on hydroxyleras i position 12 av sterol 12α-hydroxylas för att bilda 7α,12α-dihydroxi-4-kolesten-3-on.
- 7α,12α-dihydroxi-4-kolesten-3-on genomgår reduktion av dubbelbindningen i position 4,5, i den reaktion som katalyseras av 3-oxo-Δ4-steroid 5β-reduktas, för att bilda 5β-kolestan-7α,12α-diol-3-on.
- 5β-kolestan-7α,12α-diol-3-on genomgår reduktion av hydroxylgruppen i position 4, i den reaktion som katalyseras av 3α-hydroxysteroiddehydrogenas eller AKR1C4 (EC 1.1.1.213), ett cytosoliskt enzym, för att bilda 5β-kolestan-3α,7α,12α-triol.
- 5β-kolestan-3α,7α,12α-triol genomgår oxidation av sidokedjan via tre reaktioner som katalyseras av sterol 27-hydroxylas eller CYP27A1 (EC 1.14.15.15). Det är ett mitokondriellt enzym som också finns i extrahepatiska vävnader och makrofager och som introducerar en hydroxylgrupp i position 27. Hydroxylgruppen oxideras till aldehyd och sedan till karboxylsyra för att bilda 3α,7α,12α-trihydroxy-5β-kolestansyra.
- 3α,7α,12α-trihydroxi-5β-kolestansyra aktiveras till sin koenzym A ester, 3α,7α,12α-trihydroxi-5β-kolestanoyl-CoA, i den reaktion som katalyseras av antingen mycket långkedjigt acyl-CoA-syntetas eller VLCS (EC 6.2.1.-), eller gallsyra-CoA-syntetas eller BACS (EC 6.2.1.7), båda lokaliserade i det endoplasmatiska retikulumet.
- 3α,7α,12α-trihydroxy-5β-kolestanoyl-CoA transporteras till peroxisomerna där det genomgår fem på varandra följande reaktioner, var och en katalyserad av ett annat enzym. I de två sista reaktionerna förkortas sidokedjan till fyra kolatomer och slutligen bildas cholylCoA.
- I det sista steget sker konjugering, via amidbindning, av sidokedjans karboxylsyregrupp med aminosyran glycin eller taurin. Reaktionen katalyseras av gallsyra-CoA:aminosyra N-acyltransferas eller BAAT (EC 2.3.1.65), som huvudsakligen är lokaliserad i peroxisomer.
Reaktionsprodukterna är således de konjugerade gallsyrorna: glykokolsyra och taurokolsyra.
Om 7α-hydroxi-4-kolesten-3-on inte fortsätter via den reaktion som katalyseras av sterol 12α-hydroxylas, går det in i den väg som leder till syntesen av konjugerade chenodeoxikolsyrakonjugat, genom de reaktioner som beskrivs nedan.
- 7α-hydroxi-4-kolesten-3-on omvandlas till 7α-hydroxi-5β-kolestan-3-on i den reaktion som katalyseras av 3-oxo-Δ4-steroid 5β-reduktas.
- 7α-hydroxi-5β-kolestan-3-on omvandlas till 5β-kolestan-3α,7α-diol i den reaktion som katalyseras av 3α-hydroxysteroiddehydrogenas.
Därefter bildas de konjugerade gallsyrorna glycochenodeoxycholsyra och taurochenodeoxycholsyra genom modifieringar som liknar dem som ses för konjugering av kolsyra, och katalyseras huvudsakligen av samma enzymer.
Notera: Okonjugerade gallsyror som bildas i tarmen måste nå levern för att återkonjugeras.
Den alternativa eller sura vägen
Den är vanlig hos foster och nyfödda, medan den hos vuxna leder till syntesen av mindre än 10 % av gallsalterna.
Denna väg (se fig. 5) skiljer sig från den klassiska vägen genom att:
- mellanprodukterna är sura molekyler, varifrån det alternativa namnet ”acidic pathway”;
- oxidationen av sidokedjan följs av modifieringar av steroidkärnan, och inte tvärtom;
- slutprodukterna är konjugater av chenodeoxycholsyra.
Det första steget innebär omvandling av kolesterol till 27-hydroxykolesterol i den reaktion som katalyseras av sterol 27-hydroxylas.
27-hydroxykolesterol kan följa två vägar.
Rutt A
- 27-hydroxikolesterol omvandlas till 3β-hydroxi-5-kolestenoisk syra i en reaktion som katalyseras av sterol 27-hydroxylas.
- 3β-hydroxi-5-kolestenosyra hydroxyleras i position 7 i den reaktion som katalyseras av oxysterol 7α-hydroxylas eller CYP7B1 (EC 1.14.13.100), ett enzym lokaliserat i det endoplasmatiska retikulumet, för att bilda 3β-7α-dihydroxi-5-kolestenosyra.
- 3β-7α-dihydroxi-5-kolestenosyra omvandlas till 3-oxo-7α-hydroxi-4-kolestenosyra, i den reaktion som katalyseras av 3β-hydroxiΔ5-C27-steroidoxidoreduktas.
- 3-Oxo-7α-hydroxi-4-kolestenosyra bildar, som ett resultat av modifieringar i sidokedjan, chenodeoxycholsyra, och därefter dess konjugater.
Rutt B
- 27-Hydroxykolesterol omvandlas till 7α,27-dihydroxykolesterol i den reaktion som katalyseras av oxysterol 7α-hydroxylas och kolesterol 7α-hydroxylas.
- 7α,27-dihydroxykolesterol omvandlas till 7α,26-dihydroxy-4-kolesten-3-on i den reaktion som katalyseras av 3β-hydroxy-Δ5-C27-steroidoxidoreduktas;
7α, 26-dihydroxi-4-kolesten-3-on kan omvandlas direkt till konjugater av chenodeoxykolsyra eller omvandlas till 3-oxo-7α-hydroxi-4-kolestensyra och sedan genomgå modifieringar av sidokedjan och andra reaktioner som leder till syntesen av konjugater av chenodeoxykolsyra.
Mindre vägar
Det finns också mindre vägar (se fig. 5) som bidrar till gallsaltssyntesen, om än i mindre utsträckning än de klassiska och alternativa vägarna.
Till exempel:
- Ett kolesterol 25-hydroxylas (EC 1.14.99.38) uttrycks i levern.
- Ett kolesterol 24-hydroxylas eller CYP46A1 (EC 1.14.14.25) uttrycks i hjärnan, och därför exporterar organet oxysteroler även om det inte kan exportera kolesterol.
- Ett ospecifikt 7α-hydroxylas har också upptäckts. Det uttrycks i alla vävnader och verkar vara inblandat i genereringen av oxysteroler, som kan transporteras till hepatocyter för att omvandlas till chenodeoxycholsyra.
Det uttrycks dessutom sterol 27-hydroxylas i olika vävnader, och därför måste dess reaktionsprodukter transporteras till levern för att omvandlas till gallsalter.
Gallsalter: reglering av syntesen
Regleringen av gallsyrasyntesen sker via en negativ återkopplingsmekanism, särskilt på uttrycket av kolesterol 7α-hydroxylas och sterol 12α-hydroxylas.
När ett överskott av gallsyror, både fria och konjugerade, uppstår binder dessa molekyler till kärnreceptorn farnesoid X-receptorn eller FRX och aktiverar den: den mest effektiva gallsyran är chenodeoxycholsyra, medan andra, som ursodeoxycholsyra, inte aktiverar den.
FRX inducerar uttrycket av transkriptionsrepressorn small heterodimer partner eller SHP, som i sin tur interagerar med andra transkriptionsfaktorer, t.ex. leverreceptor homolog-1 eller LRH-1 och hepatocyte nuclear factor-4α eller HNF-4α. Dessa transkriptionsfaktorer binder till en sekvens i promotorregionen för 7α-hydroxylas- och 12α-hydroxylasgener, region som kallas bile acid response elements eller BAREs, och hämmar deras transkription.
En av anledningarna till att gallsaltssyntesen är hårt reglerad är att många av deras metaboliter är giftiga.
Chiang J.Y.L. Bile acids: regulation of synthesis. J Lipid Res 2009;50(10):1955-66. doi:10.1194/jlr.R900010-JLR200
Gropper S.S., Smith J.L. Advanced nutrition and human metabolism. 6h Edition. Cengage Learning, 2012
Moghimipour E., Ameri A., and Handali S. Absorptionshöjande effekter av gallsalter. Molecules 2015;20(8); 14451-73. doi:10.3390/molecules200814451
Monte M.J., Marin J.J.G., Antelo A., Vazquez-Tato J. Gallsyror: Kemi, fysiologi och patofysiologi. World J Gastroenterol 2009;15(7):804-16. doi:10.3748/wjg.15.804
Rawn J.D. Biochimica. Mc Graw-Hill, Neil Patterson Publishers, 1990
Rosenthal M.D., Glew R.H. Medical biochemistry – Human metabolism in health and disease. John Wiley J. & Sons, Inc., Publication, 2009
Sundaram S.S., Bove K.E., Lovell M.A. och Sokol R.J. Mechanisms of Disease: inborn errors of bile acid synthesis. Nat Clin Pract Gastroenterol Hepatol 2008;5(8):456-68. doi:10.1038/ncpgasthep1179