Kobieta w wieku 40 lat przedstawiona z licznymi „atakami” w ciągu ostatniego tygodnia, o rosnącej częstotliwości. Czuje się oszołomiona, a następnie nie reaguje. Trwa to zwykle około jednej minuty, po czym ustępuje. Nie odczuwała bólu w klatce piersiowej. W dzieciństwie miała napady drgawkowe, ale w czasie tych napadów nie ma aktywności drgawkowej.
Monitor pokazuje co następuje:

Tachykardia komorowa, częstość około 220 uderzeń na minutę
Podczas tego rytmu pacjentka była przytomna, chroniła swoje drogi oddechowe, była blada, miała obfite pocenie się i chłodne kończyny. Puls był obecny. Nie stwierdzono zaburzeń oddychania.
Zarejestrowano 12-odprowadzeniowe EKG:
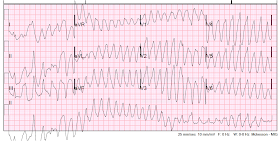
VT, i jest to „polimorficzny” VT, ponieważ zespoły mają wiele morfologii. Częstość ponownie około 220. Polimorficzny częstoskurcz komorowy jest albo torsade (związany z długim odstępem QT), albo nie torsade (QT nie jest długi, często z powodu niedokrwienia)
Na monitorze nastąpiła spontaniczna konwersja do innego rytmu i uzyskano kolejny zapis 12-odprowadzeniowy:

Występuje bigeminia. Wąskie zespoły poprzedzone są załamkami P. Zespoły QRS związane z pobudzeniami zatokowymi mają charakter bloku prawej odnogi pęczka Hisa (RBBB) i nie wydają się mieć bardzo długiego odstępu QT (obliczyłem 400ms QT podzielone przez pierwiastek kwadratowy z poprzedzającego odstępu R-R = 460ms). Interweniujące zespoły komorowe (PVC) wyglądają bardzo dziwacznie z długim QT. PVCs mają duże uniesienie ST (II, III, aVF) z wzajemnym obniżeniem ST (aVL, precordial), co sugeruje inferoposterior STEMI, ale jest to wyraźnie mimika, ponieważ zespoły zatokowe nie mają uniesienia ST.
Powróciła do tachykardii:
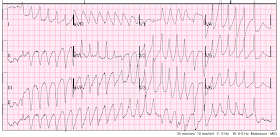
Polimorficzny VT ponownie.
Co robić?
Po pierwsze, jaki to jest rodzaj VT? Polimorficzny VT. PMVT definiuje się jako szeroki złożony rytm komorowy o częstości powyżej 100 z szybko zmieniającą się osią QRS i/lub morfologią.
Polimorficzny VT
Etiologia
Polimorficzny VT to albo torsades de pointe (związane z długim QT w wyjściowym 12-odprowadzeniowym EKG), albo nietorsades (zwykle związane z niedokrwieniem lub inną organiczną chorobą serca). Obecność wydłużenia odstępu QT w podstawowym 12-odprowadzeniowym EKG nie zawsze jest oczywista. Torsade de pointes oznacza „skręcanie punktów” i odnosi się do zmiany osi wokół linii izoelektrycznej.
1. Nabyte: spowodowane zwykle przez leki. Lista jest długa. Również z powodu zaburzeń elektrolitowych, zwłaszcza hipokryzji i hipomegalii. Skorygowany odstęp QT (korekcja Bazetta = QT podzielone przez pierwiastek kwadratowy z poprzedzającego odstępu R-R w milisekundach) jest zwykle większy niż 600 ms. Torsade w nabytym długim QT jest znacznie bardziej prawdopodobne w bradykardii, ponieważ odstęp QT po długiej pauzie jest jeszcze dłuższy. Dlatego torsade w nabytym długim QT nazywa się „zależnymi od pauzy”: jeśli po długiej pauzie występuje pobudzenie zatokowe (co powoduje wydłużenie odstępu QT), to wczesne PVC („wczesna afterdepolaryzacja”, EAD) jest znacznie bardziej prawdopodobne, że wystąpi podczas repolaryzacji i zapoczątkuje torsade. Zwykle sekwencja jest następująca: pobudzenie zatokowe, następnie wczesne PVC, potem długa pauza, ponieważ PVC było wczesne, co powoduje szczególnie długi QT, następnie kolejne PVC z „R na T”, które inicjuje torsade.
2. Wrodzony, szczególnie wrodzony zespół długiego QT. Niestabilny PMVT spowodowany wrodzonym zespołem długiego QT jest znacznie rzadszy. (W ciągu 26 lat EM i 125 000 pacjentów nigdy nie widziałem przypadku torsade PMVT z powodu wrodzonego długiego QT). Do wrodzonych przyczyn torsade PMVT zalicza się również „katecholaminergiczny PMVT”, w którym nie obserwuje się widocznego wydłużenia QT w zapisie 12-odprowadzeniowym, ale uważa się, że ma on podobną etiologię. Profilaktyka wrodzonego długiego QT obejmuje stosowanie beta-blokerów (tak samo jak w przypadku katecholaminergicznego PMVT, ponieważ w obu przypadkach stymulacja beta prowokuje torsade); odróżnia się to od nabytego długiego QT, który może być leczony stymulacją beta (izopreterenol).
Nie znalazłem żadnych zaleceń dotyczących stosowania beta-blokerów w ostrym leczeniu torsade w tej grupie, ale prawie niemożliwe jest stwierdzenie, czy izoproterenol pogorszy lub polepszy sytuację u danego pacjenta z wrodzonym długim QT (patrz komentarz naszego elektrofizjologa na końcu). Wydaje się, że większość objawowych pacjentów z wrodzonym długim QT pojawia się po omdleniu lub po reanimacji v fib, a rzadko z utrzymującymi się torsade lub niestabilnością. Postępowanie u tych chorych polega więc przede wszystkim na rozpoznawaniu i zapobieganiu przyszłym omdleniom i nagłym zgonom sercowym, zwykle z zastosowaniem wszczepialnego debribrylatora jako uzupełnienia beta-blokerów. Torsade z wrodzonego długiego QT może być wywołany przez stosowanie leków wydłużających QT.
Non-Torsade Etiologie PMVT
Najczęściej z powodu niedokrwienia. Prawie zawsze będą to jawne, ciężkie epizody niedokrwienia, z bólem w klatce piersiowej i/lub jednoznacznymi niedokrwiennymi nieprawidłowościami w EKG. Również z powodu wcześniej istniejącej kardiomiopatii.
Zarządzanie polimorficznym VT
Większość torsade jest samoograniczająca się. Jeśli nie nawraca spontanicznie, wymaga defibrylacji, jeśli pacjent jest niestabilny. Jeśli dojdzie do nawrotu, istnieje prawdopodobieństwo nawrotu, a terapia ma na celu zapobieganie nawrotom.
Leczenie ostrych epizodów torsade:
1. Kardiowersja lub defibrylacja, jeśli jest aktywna, zwłaszcza jeśli jest niestabilna
2. Usunięcie czynnika wywołującego w nabytym długim QT
3. Korekta hipoK, nawet do poziomu nieznacznie przekraczającego normę
4. Podanie 2-4 g MgSO4, nawet jeśli poziom Mg jest prawidłowy (przydatna może być kroplówka w dawce 3-10 mg na minutę)
5. Tylko jeśli jest to nabyty długi QT: stymulacja beta-adrenergiczna z izoproterenolem
6. Jeśli te metody nie przyniosą efektu, prawie zawsze zadziała stymulacja overdrive, zwykle z częstością około 100, aby zapobiec pauzom (stymulacja przezskórna jest dobra dla tymczasowej ulgi, jako pomost do stymulacji przezżylnej).
7. Lidokaina może również przynieść korzyść, ponieważ może tłumić PVCs (wczesne afterdepolaryzacje), które inicjują torsade, jeśli występują na załamku T.
8. Amiodaron przynosi wątpliwą korzyść i może zaszkodzić. Sam w sobie wydłuża odstęp QT, jednak bez znacznego zwiększenia ryzyka torsade
9. Nie należy podawać beta-blokerów, jeśli u pacjenta nie rozpoznano wrodzonego długiego QT. Odwrotnie: izoproterenol.
10. Jeśli jest to wrodzone, to ostra beta-blokada może być wskazana. Najpierw spróbowałabym esmololu, bo można go wyłączyć. Nie ma on jednak blokady beta-2 i jest dla mnie niejasne, czy jest to ważne i/lub konieczne. Jeśli esmolol nie zadziała, to należy podać IV propranolol. Propranolol i nadolol są najlepszymi długoterminowymi beta-blokerami dla wrodzonego długiego QT, a beta 1 selektywny metoprolol nie jest bardzo skuteczny. Czy jest to spowodowane selektywnością beta nie jest dla mnie jasne.
Here jest fascynujący przypadek wrodzonego długiego QT z Torsade. Jest tam świetna dyskusja na temat roli i funkcji beta-blokady we wrodzonym długim QT.
Terapia ostrego nietorsade PMVT: podobna do monomorficznego VT
1. Kardiowersja lub defibrylacja, jeśli jest aktywna
2. Korekta zaburzeń elektrolitowych, zwłaszcza hipokliny lub hipomegalii
3. Zapobieganie kolejnym epizodom za pomocą lidokainy lub amiodaronu, ewentualnie beta-blokera, takiego jak esmolol (którego należy unikać w przypadku nabytych torsade’ów z długim QT).
4. Leczenie przeciwniedokrwienne, aż do rewaskularyzacji włącznie
5. Implantowany kardiowerter-defibrylator może być konieczny nawet przy udanej rewaskularyzacji
Powrót do naszego przypadku
Kardiowersja jest wskazana tylko wtedy, gdy pacjent jest w torsade, i będzie działać tylko tymczasowo, ponieważ pacjent wchodzi i wychodzi z rytmu. Istotne jest zapobieganie kolejnym epizodom.
W tym przypadku widzimy długi QT tylko w PVCs, ale nie w natywnych pobudzeniach RBBB. Często torsade są „zależne od pauzy” i można je zaobserwować tylko w kompleksie, który następuje po długiej pauzie. Nie występuje ból w klatce piersiowej, a w zespołach zatokowych EKG nie stwierdza się cech niedokrwienia. Aby polimorficzny częstoskurcz komorowy był spowodowany niedokrwieniem, w EKG zwykle stwierdza się jednoznaczne oznaki niedokrwienia. Wszystko to więc sugeruje torsade, ale nie jest diagnostyczne. Pacjentka nie przyjmowała żadnych znanych leków, które wydłużają odstęp QT. Ma tylko historię choroby Gravesa i donosi, że odstawiła wszystkie leki.
Gdy nie ma częstoskurczu komorowego, jej ciśnienie tętnicze jest podwyższone do 190/80 z wyczuwalnym pulsem 90 i saturacją 99.
Wstępne K wróciło do normy. Poziom Mg nie był znany w tym momencie.
W chwili t = 12 podano 2 gramy magnezu dożylnie.
W chwili t = 13 minut podano 150 mg amiodaronu
W chwili t = 15 minut podano 100 mg lidokainy
W chwili t = 30 minut nie było poprawy i podano esmolol w bolusie i kroplówce. Należy podać izoproterenol.
Pracownia cewnikowania została uruchomiona. Podano kolejne 2 gramy magnezu dożylnie.
t = 64 minuty: K powraca na poziomie 2,4 mEq/L (wartość początkowa była błędna). To jeszcze mocniej sugeruje torsade. Podano KCl do linii centralnej. Rozpoczęto podawanie kroplówki z Amiodaronu. Podano aspirynę doodbytniczo.
t = 79 minut: Podano prokainamid 1500 mg w ciągu 2 minut. (Prokainamid może być przydatny w nietorsade PMVT, ale prawdopodobnie wydłuży QT i sprawi, że torsade będą bardziej niestabilne. Jest również silnym ujemnym inotropem i może być niebezpieczny przy słabej funkcji LV.)
t = 97 minut: pacjent zabrany do pracowni cewnikowania:
Pacjenta zabrano do pracowni cewnikowania i założono stymulator. Rytm został wychwycony za pomocą stymulacji overdrive, a następnie zwolniony. Stwierdzono rozsianą chorobę wieńcową, ale bez zmiany sprawczej (brak ostrego zespołu wieńcowego). Troponina była ujemna.
Okazało się, że pacjent był na metadonie i był toksyczny dla metadonu. Jest to jeden z wielu leków, który powoduje długi QT. To był Torsade de Pointes z powodu długiego QT z powodu metadonu i hipokaliemii.
Tutaj 12-odprowadzeniowy zapis podczas stymulacji:
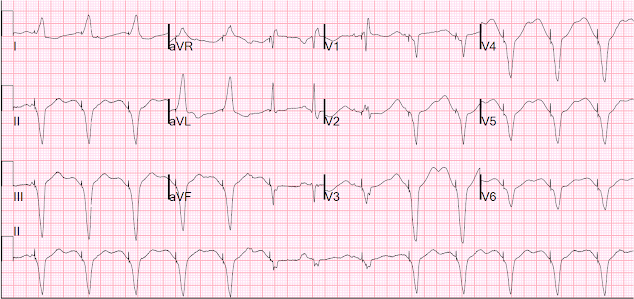
Podczas stymulacji
Tutaj kolejny z wyłączonym stymulatorem, następnego dnia:
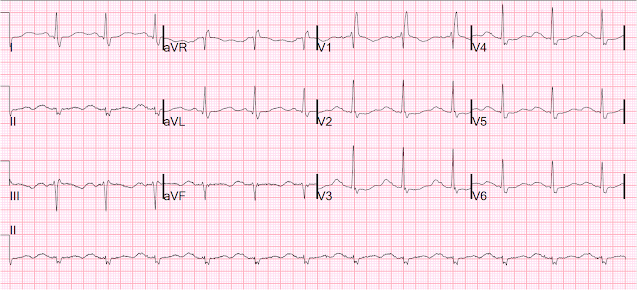
Sinus z RBBB i bardzo długim QT
I jeszcze czwartego dnia:
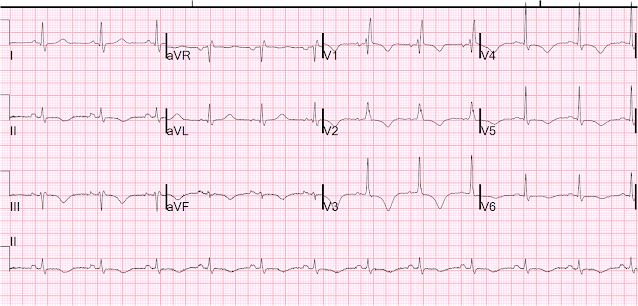
Inwersje załamka T, QT nadal długi
Z powodu wyjątkowo długiego okresu półtrwania metadonu potrzeba było wielu dni, aby QT się skrócił. Ostatecznie pacjent poradził sobie dobrze.
Komentarz dotyczący stosowania izoproterenolu we wrodzonym długim QT:
Zadałem naszemu elektrofizjologowi (Rehan Karim) następujące pytanie:
„Chcę być pewien, że mam to proste:
W przypadku wrodzonego długiego QT beta-blokada jest wskazana przewlekle, a pacjentowi z nawracającym częstoskurczem komorowym, który przebywa w szpitalu, NIE NALEŻY podawać izoproterenolu.
Tylko nabyta długa QT jest „zależna od pauzy” i poprawia się przy szybszej pracy serca, a blokada beta NIE jest wskazana. Wskazany jest raczej izoproterenol (i stymulacja typu overdrive).
Czy może mnie Pan poprawić w tej kwestii?”
Innymi słowy:
Oto jego odpowiedź:
„Chciałbym, żeby sprawy były na tyle jasne, żeby można było wszystko ująć w formie algorytmu… ale niestety tak nie jest.”
To naprawdę zależy, z jakim typem wrodzonego długiego QT masz do czynienia, a nawet jeśli wiesz – sprawy nie są tak proste.
Oto przykład:
Wrodzone długie QT typu 3 to mutacja kanału sodowego (SCN5A) – który jest tym samym genem co zespół Brugadów.
Długie QT typu 3 mają Torsade zależne od pauzy. Jednak w tej sytuacji nadal stosuje się beta-blokery (oczywiście po wprowadzeniu stymulacji przedsionków, aby zapobiec bradykardii) – głównie ze względu na wpływ beta-blokerów na zmniejszenie dyspersji QT.
Jeszcze bardziej skomplikowane… bloker kanału sodowego klasy I-B (meksyletyna) jest czasami stosowany w LQT-3.
Zgodnie z moją wiedzą beta-blokery nie są prawdopodobnie tak skuteczne w LQT-3 jak w innych formach – ale nadal są stosowane.
W związku z tym, nie sądzę, że możliwe jest wymyślenie odpowiedzi Tak/Nie z wiedzą, którą mamy w tej chwili – rzeczy muszą być brane w perspektywie klinicznej.
to jeden z mylących tematów – w rzeczywistości większość genetycznych arytmii / chanellopatii jest dość trudna do opanowania klinicznie. Jesteśmy tak bardzo przyzwyczajeni do oglądania danych od tysięcy pacjentów w badaniach kardiologicznych – a potem dostajemy się do takich sytuacji, w których obciążenie chorobą nie jest wystarczająco duże, aby dać nam dane inne niż rejestry z dużych ośrodków klinicznych.