Nelikymppinen nainen sai viimeisen viikon aikana useita ”jaksoja”, joiden taajuus oli lisääntynyt. Häntä huimaa, minkä jälkeen hän ei enää reagoi. Kohtaus kestää yleensä noin minuutin ja häviää sitten. Hänellä ei ole ollut rintakipua. Hänellä on ollut lapsena kouristuskohtauksia, mutta näiden kohtausten aikana ei esiinny kouristustoimintaa.
Monitori näyttää seuraavaa:

Ventrikulaarinen takykardia, lyöntitiheys noin 220 lyöntiä minuutissa
Tämän rytmin aikana hän oli hereillä, hän suojasi hengitysteitään, ja hänellä oli kalpeus, diaforeesi ja viileät raajat. Pulssit olivat läsnä. Hengitysvaikeuksia ei ollut.
Kirjattiin 12-kytkentäinen EKG:
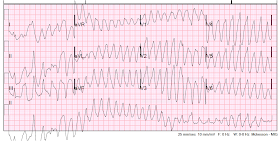
VT, ja se on ”polymorfinen” VT, koska komplekseilla on useita morfologioita. Syke taas noin 220. Polymorfinen VT on joko torsade (liittyy pitkään QT-väliin) tai ei-torsade (QT ei ole pitkä, johtuu usein iskemiasta)
Monitorissa hän siirtyi spontaanisti eri rytmiin, ja saatiin toinen 12-kytkentäinen:

On bigeminia. Kapeita komplekseja edeltävät P-aallot. Sinuslyönteihin liittyvässä QRS:ssä on oikean sidehaaran esto (RBBB), eikä niillä näytä olevan kovin pitkiä QT-välejä (laskin 400 ms QT:n jaettuna edeltävän R-R-välin neliöjuurella = 460 ms). Välissä olevat kammiokompleksit (PVC:t) näyttävät hyvin oudoilta ja niillä on pitkä QT-aika. PVC:ssä on suuri ST-nousu (II, III, aVF) ja vastavuoroinen ST-laskeuma (aVL, prekordiaalinen), mikä viittaa inferoposterioriseen STEMI:iin, mutta tämä on selvästi jäljitelmä, koska väliin jäävissä sinuskomplekseissa ei ole ST-nousua.
Hänellä alkoi taas takykardia:
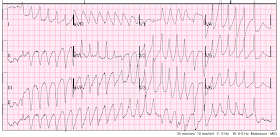
Polymorfinen VT taas.
Mitä pitäisi tehdä?
Ensin, millainen VT on kyseessä? Polymorfinen VT. PMVT määritellään laajakompleksiseksi kammiorytmiksi taajuudella yli 100, jossa QRS-akseli ja/tai morfologia muuttuu nopeasti.
Polymorfinen VT
Etiologia
Polymorfinen VT on joko torsades de pointe (johon liittyy pitkä QT-aika 12-kytkentäisessä EKG:ssä lähtötilanteessa) tai ei-torsades (liittyy yleensä iskemiaan tai muuhun orgaaniseen sydänsairauteen). QT-ajan pidentyminen 12-kytkentäisessä EKG:ssä ei ole aina ilmeistä. Torsade de pointes tarkoittaa ”pisteiden kiertymistä” ja viittaa akselin muuttumiseen isoelektrisen linjan ympäri.
PMVT:n morfologia (eli pisteiden kiertymisen esiintyminen) ei yksinään pysty erottamaan pitkästä QT:stä johtuvaa PMVT:tä (torsade) muista etiologioista johtuvasta PMVT:stä (ei-torsade). Pulssitonta PMVT:tä on käytännössä mahdotonta erottaa kammiovärinästä, ja tutkimukset ovat osoittaneet, että suurin osa pulssittomista rytmeistä, jotka näyttävät olevan torsadeja (ja joissa on ”pisteiden kiertymistä”), ovat todellisuudessa kammiovärinää. Tällä erottelulla ei ole merkitystä välittömän hoidon (defibrillointi) kannalta, mutta sillä on tärkeitä vaikutuksia uusien rytmihäiriöiden ehkäisyyn.
Torsadit PMVT:n etiologiat
1. Hankittu: johtuu yleensä lääkkeistä. Luettelo on pitkä. Johtuu myös elektrolyyttipoikkeavuuksista, erityisesti hypoK ja hypoMg. Korjattu QT-väli (Bazett-korjaus = QT jaettuna edeltävän R-R-välin neliöjuurella millisekunteina) on yleensä suurempi kuin 600 ms. Torsadit hankitun pitkän QT:n yhteydessä ovat paljon todennäköisempiä bradykardiassa, koska pitkän tauon jälkeinen QT-väli on vielä pidempi. Näin ollen torsadeja hankitun pitkän QT:n yhteydessä kutsutaan ”tauko-riippuvaisiksi”: jos pitkän tauon jälkeen on sinuslyönti (joka luo pidemmän QT-intervallin), varhainen PVC (”varhainen jälkidepolarisaatio”, EAD) tapahtuu paljon todennäköisemmin repolarisaation aikana ja käynnistää torsadit. Tavallinen järjestys on: sinuslyönti, sitten varhainen PVC, sitten pitkä tauko, koska PVC oli varhainen, mikä sitten johtaa erityisen pitkään QT-aikaan, sitten toinen PVC, jossa on ”R on T”, joka käynnistää torsadit.
2. Synnynnäinen, erityisesti synnynnäinen pitkän QT:n oireyhtymä. Synnynnäisestä pitkästä QT:stä johtuva epästabiili PMVT on paljon harvinaisempi. (26 vuoden EM-toiminnan ja 125 000 potilaan aikana en ole koskaan nähnyt synnynnäisestä pitkästä QT:stä johtuvaa torsade PMVT:tä). Synnynnäisiä syitä torsadeen ovat muun muassa ”katekolaminerginen PMVT”, jossa QT-ajan pidentyminen ei näy 12-kytkentäisessä EKG:ssä, mutta sillä uskotaan olevan samanlainen etiologia. Synnynnäisen pitkän QT:n ennaltaehkäisevään hoitoon kuuluu beetasalpaajien käyttö (sama kuin katekolaminergisen PMVT:n kohdalla, sillä molemmissa beetastimulaatio aiheuttaa torsadekohtauksen); tämä eroaa hankitusta pitkästä QT:stä, jota voidaan hoitaa beetastimulaatiolla (isopreterenoli).
En ole löytänyt suosituksia beetasalpaajien käytöstä torsadin akuutissa hoidossa tässä ryhmässä, mutta on lähes mahdotonta sanoa, pahentaako vai parantaako isoproterenoli tilannetta kenelläkään tietyllä potilaalla, jolla on synnynnäinen pitkä QT (ks. elektrofysiologimme kommentti lopussa). Näyttää siltä, että useimmat oireilevat potilaat, joilla on synnynnäinen pitkä QT-aika, tulevat synkopeen tai elvytetyn v fib:n jälkeen, ja harvoin heillä esiintyy jatkuvaa torsadia tai epävakautta. Näin ollen näiden potilaiden hoito on ensisijaisesti synkopeen ja sydänperäisen äkkikuoleman tunnistamista ja ehkäisemistä tulevaisuudessa, yleensä implantoitavalla debribrillaattorilla beetasalpaajien lisäksi. Synnynnäisestä pitkästä QT:stä johtuvat torsadit voidaan saada aikaan QT-aikaa pidentävien lääkkeiden käytöllä.
PMVT:n ei-torsadiset etiologiat
Yleisimmin johtuvat iskemiasta. Nämä ovat lähes aina avoimia, vaikeita iskemian jaksoja, joihin liittyy rintakipua ja/tai yksiselitteisiä iskeemisiä EKG-poikkeavuuksia. Johtuvat myös jo olemassa olevasta kardiomyopatiasta.
Polymorfisen VT:n hoito
Useimmiten torsade on itsestään rajoittuva. Jos se ei muutu spontaanisti, se on defibrilloitava, jos potilas on epävakaa. Jos se muuttuu, se todennäköisesti uusiutuu, ja hoidolla pyritään estämään uusiutuminen.
Akuuttien torsadejaksojen hoito:
1. Kardioversio tai defibrillaatio, jos se on aktiivinen, erityisesti jos se on epävakaa
2. Aiheuttavan aineen poisto hankitussa pitkässä QT:ssä
3. HypoK:n korjaus, jopa lievästi supranormaalille tasolle
4. 2-4 g MgSO4:n anto, vaikka Mg-taso olisi normaali (tippa 3-10 mg minuutissa voi olla hyödyllinen)
5. MgSO4:n anto. Vain jos kyse on hankitusta pitkästä QT:stä: beeta-adrenerginen stimulaatio isoproterenolilla
6. Jos nämä eivät auta, ylikierroksilla tapahtuva tahdistus, tavallisesti noin 100:n tahdilla taukojen estämiseksi, toimii melkein aina (transkutaaninen tahdistus sopii hyvin tilapäiseen helpotukseen siltana transvenooseen tahdistukseen siirtymiseksi)
7. Lidokaiinista voi olla myös hyötyä, koska se voi tukahduttaa PVC:t (varhaiset jälkidepolarisaatiot), jotka aloittavat torsadekohtauksen (torsadekohtauksen), jos ne tapahtuvat T-aallokossa.
8. Amiodaronista on kyseenalaista hyötyä ja mahdollisesti haittaa. Itsessään se pidentää QT-väliä, vaikkei se suuresti lisää torsadien riskiä
9. Älä anna beetasalpaajia, ellei potilaalla ole synnynnäisen pitkän QT-ajan diagnoosia. Juuri päinvastoin: isoproterenoli.
10. Jos kyseessä on synnynnäinen , akuutti beetasalpaus voi olla aiheellinen. Kokeilisin esmololia ensin, koska se voidaan kytkeä pois päältä. Siinä ei kuitenkaan ole beeta-2-salpausta ja minulle on epäselvää, onko se tärkeää ja/tai tarpeellista. Jos esmololi ei tehoa, olisi annettava suonensisäistä propranololia. Propranololi ja nadololi ovat parhaita pitkäaikaisia beetasalpaajia synnynnäisen pitkän QT-ajan hoitoon, eikä beeta 1 -selektiivinen metoprololi ole kovin tehokas. Johtuuko tämä beetaselektiivisyydestä, ei ole minulle selvää.
Tässä on kiehtova tapaus synnynnäisestä pitkästä QT:stä, johon liittyy Torsade. Siellä on hyvä keskustelu beetasalpauksen roolista ja tehtävästä synnynnäisessä pitkässä QT:ssä.
Akuutin ei-torsadisen PMVT:n hoito: samanlainen kuin monomorfinen VT
1. Kardioversio tai defibrillaatio, jos aktiivinen
2. Elektrolyyttihäiriöiden, erityisesti hypoK:n tai hypoMg:n, korjaaminen
3. Uusien episodien ehkäisy lidokaiinilla tai amiodaronilla, mahdollisesti beetasalpaajalla, kuten esmololilla (jota vältettäisiin kaikissa hankituissa pitkän QT:n Torsadeissa)
4. Anti-iskeemiset hoitomuodot, revaskularisaatio mukaan luettuna
5. Hoidot. Implantoitava kardioverteri-defibrillaattori voi olla tarpeen, vaikka revaskularisaatio onnistuisikin
Takaisin tapaukseemme
Kardioversio on indikoitu vain silloin, kun potilas on torsadissa, ja se toimii vain tilapäisesti, kun potilas menee rytmiin ja poistuu siitä. Uusien jaksojen ehkäisy on olennaista.
Tässä tapauksessa näemme pitkän QT:n vain PVC:ssä, mutta ei natiivissa RBBB-lyönneissä. Usein torsadit ovat ”tauko-riippuvaisia” ja näkyvät vain kompleksissa, joka seuraa pitkää taukoa. Rintakipua ei ole, eikä sinus EKG-komplekseissa ole todisteita iskemiasta. Jotta polymorfinen VT johtuisi iskemiasta, on yleensä olemassa jokin yksiselitteinen EKG-löydös iskemiasta. Kaikki tämä viittaa siis torsadesiin, mutta ei ole diagnostista. Potilaalla ei ollut mitään tunnettua QT-väliä pidentävää lääkitystä. Hänellä on ollut vain Gravesin tauti, ja hän ilmoittaa olleensa ilman kaikkia lääkkeitä.
Kun hänellä ei ole VT:tä, hänen verenpaineensa on koholla 190/80, tunnusteltava pulssi on 90 ja happisaturaatio 99.
Alku-K palautui normaaliksi. Mg-taso ei ollut tässä vaiheessa tiedossa.
Klo t = 12 annettiin 2 grammaa magnesiumia suonensisäisesti.
Klo t = 13 minuuttia annettiin 150 mg amiodaronia
Klo t = 15 minuuttia annettiin 100 mg lidokaiinia
Klo t = 30 minuuttia ei tapahtunut parannusta ja annettiin esmololibolus ja -tippa. Isoproterenolia olisi annettava.
Katetrilaboratorio aktivoitiin. Annettiin vielä 2 grammaa magnesiumia suonensisäisesti.
t = 64 minuuttia: K palautuu 2,4 mEq/L (alkuperäinen arvo oli virheellinen). Tämä viittaa entistä vahvemmin Torsadeen. KCl annetaan keskuslaskimoon. Amiodaronitiputus aloitettiin. Annetaan aspiriinia rektaalisesti.
t = 79 minuuttia: Prokaiiniamidia annetaan 1500 mg 2 minuutin aikana. (Prokaiiniamidi voi olla hyödyllinen ei-torsaadisessa PMVT:ssä, mutta se todennäköisesti pidentää QT-aikaa ja tekee torsadeista epävakaampia. Se on myös voimakas negatiivinen inotrooppi ja voi olla vaarallinen, jos LV:n toiminta on huono.)
t = 97 minuuttia: Potilas vietiin katetrilaboratorioon:
Potilas vietiin katetrilaboratorioon ja hänelle asetettiin tahdistin. Rytmi saatiin kiinni ylitahdistuksella ja sitten hidastettiin. Potilaalla oli diffuusi sepelvaltimotauti, mutta ei culprit-leesiota (ei akuuttia sepelvaltimo-oireyhtymää). Troponiini oli negatiivinen.
Havaittiin, että potilas käytti metadonia ja oli metadonitoksinen. Se on yksi monista lääkkeistä, jotka aiheuttavat pitkän QT-ajan. Kyseessä oli Torsade de Pointes, joka johtui metadonin ja hypokalemian aiheuttamasta pitkästä QT:stä.
Tässä on 12-kytkentäinen tahdistuksen aikana:
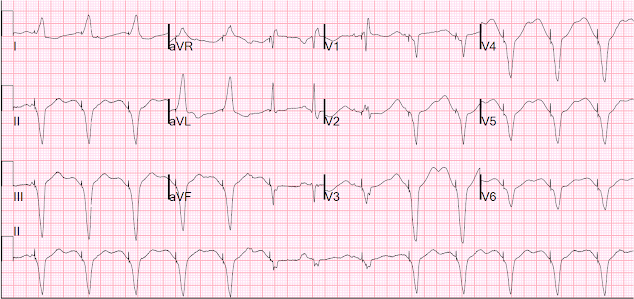
Tahdistuksen aikana
Tässä on toinen tahdistin pois päältä, seuraavana päivänä:
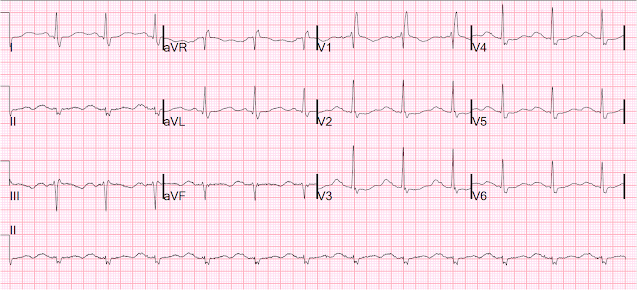
Sinus, jossa on RBBBB ja erittäin pitkä QT
Ja sitten neljäntenä päivänä:
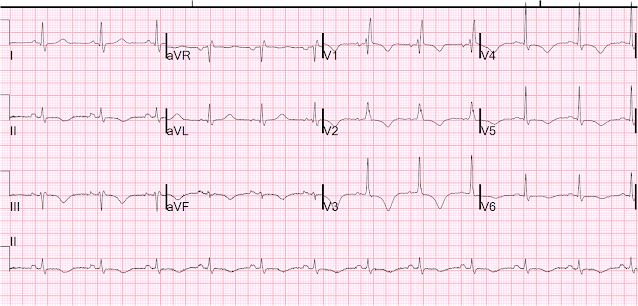
T-aaltoinversiot, QT edelleen pitkä
Metadonin poikkeuksellisen pitkän puoliintumisajan vuoksi QT:n lyheneminen kesti päiviä. Lopulta potilas pärjäsi hyvin.
Kommentti isoproterenolin käytöstä synnynnäisen pitkän QT:n hoidossa:
Kysyin elektrofysiologiltamme (Rehan Karim) seuraavaa:
”Haluan olla varma, että olen ymmärtänyt asian oikein:
Synnynnäisen pitkän QT:n hoidossa beetasalpaajahoito on indikoitua kroonisesti, ja potilaalle, jolla on sairaalahoidossa oleva toistuva VT, EI anneta isoproterenolia.
Vain hankittu pitkä QT on ”tauko-riippuvainen” ja paranee nopeammalla sykkeellä, ja beetasalpaus EI ole indikoitu. Pikemminkin isoproterenoli on indikoitu (ja ylitahdistus).”
Voitteko oikaista minua tästä?”
Muilla sanoilla:
Tässä on hänen vastauksensa:
”Toivon, että asiat olisivat tarpeeksi selkeitä, jotta voisin laittaa kaiken algoritmiseen muotoon… mutta valitettavasti näin ei ole.”
Se todella riippuu siitä, minkä tyyppisestä synnynnäisestä pitkästä QT:stä on kyse, ja vaikka tietäisitkin – asiat eivät ole yhtä suoraviivaisia.
Tässä on esimerkki:
Synnynnäinen pitkä QT-tyyppi 3 on natriumkanavan mutaatio (SCN5A) – joka on sama geeni kuin Brugadan oireyhtymä.
Pitkä QT-tyyppi 3:lla on tauko-riippuvainen Torsades. Beetasalpaajia käytetään kuitenkin edelleen tässä tilanteessa (tietenkin sen jälkeen, kun eteisten tahdistus on aloitettu bradykardian estämiseksi) – tämä johtuu ensisijaisesti beetasalpaajien vaikutuksesta QT-dispersiota pienentävästi.
Se on vielä monimutkaisempaa… I-B-luokan natriumkanavan salpaajaa (Mexiletine) käytetään joskus LQT-3:n hoidossa.
Tietääkseni beetasalpaajat eivät ole luultavasti yhtä tehokkaita LQT-3:n hoidossa kuin muiden muotojen hoidossa – mutta niitä käytetään edelleen.
Sen vuoksi en usko, että tämänhetkisellä tietämyksellämme on mahdollista antaa kyllä/ei-vastausta – asiat on otettava kliinisestä näkökulmasta.
Jos jollakulla on selvästi tauko-riippuvaisia torsadeja, eikä häntä tahdisteta – en käytä beetasalpaajaa, vaan yritän pikemminkin nostaa sykettä isoproterenolin avulla.
Tohtori Karim lisäsi:
Tämä on yksi hämmentävistä aiheista – itse asiassa useimmat geneettiset rytmihäiriöt / chanellopatiat ovat melko haastavia hallita kliinisesti. Olemme niin paljon tottuneet näkemään tietoja tuhansista potilaista kardiologisissa tutkimuksissa – ja sitten joudumme sellaisiin tilanteisiin, joissa tautitaakka ei ole tarpeeksi suuri, jotta saisimme muita tietoja kuin suurten kliinisten keskusten rekistereistä.