La fluorescencia es una de las herramientas más importantes y útiles de la caja de herramientas de un biólogo. En biología, casi todos los campos, desde la fisiología hasta la inmunología, utilizan moléculas fluorescentes (también conocidas como fluoróforos) para detectar proteínas. Sin embargo, la ciencia específica que subyace al funcionamiento de la fluorescencia puede resultar confusa o pasarse por alto.
¡No tema! En este artículo, desglosamos los puntos clave de la fluorescencia para que pueda ser el experto que siempre quiso ser.
¿Qué es exactamente la fluorescencia?
Por definición, la fluorescencia es un tipo de fotoluminiscencia, que es lo que ocurre cuando una molécula es excitada por fotones de luz ultravioleta o visible. Más concretamente, la fluorescencia es el resultado de que una molécula absorba luz a una longitud de onda específica y emita luz a una longitud de onda más larga.
Detalles, por favor
Afortunadamente, el Dr. Aleksander Jablonski dedicó su vida a este tema. Finalmente desarrolló el diagrama de Jablonski para describir la absorción y emisión de la luz. En resumen, los 3 pasos de la fluorescencia son la absorción (o excitación), la transición no radiativa (o el tiempo de vida del estado excitado) y la emisión de fluorescencia.1
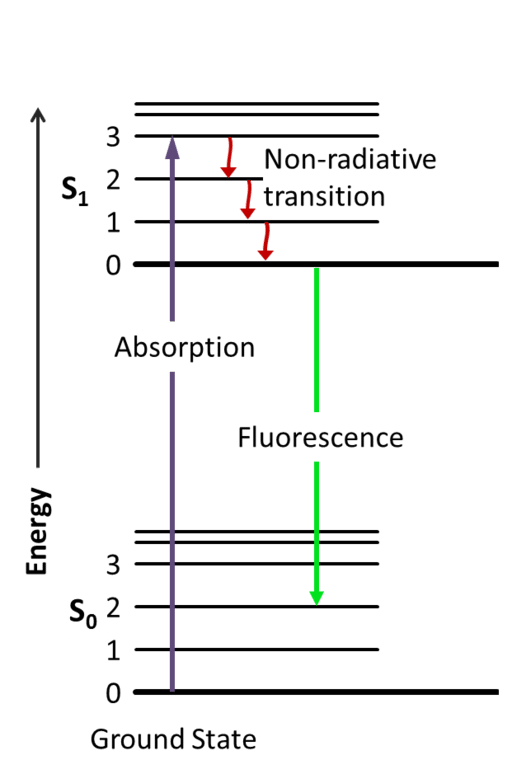
Figura 1. Diagrama de Jablonski. S0 y S1 representan diferentes estados electrónicos. Los otros números (aquí 0-3) representan estados vibracionales. Cortesía de Jacobkhed.
Paso 1: Excitación
Regreso a la Química General: la luz visible existe como partículas elementales llamadas fotones. Estas partículas son paquetes esenciales de energía que, al ser absorbidos, impulsarán o «excitarán» a la molécula que absorbe la luz hacia un nivel de energía superior. En el caso de la fluorescencia, los fluoróforos absorben la luz visible, normalmente proporcionada por una lámpara incandescente o un láser, lo que conduce a un estado electrónico singlete (S1) excitado de la molécula.
Paso 2: Tiempo de vida del estado excitado
Como todos sabemos, el objetivo de un átomo es estar en el estado de energía más bajo posible. Así que cuando un fluoróforo se excita a un estado electrónico superior, inmediatamente quiere empezar a liberar energía; por lo tanto, este estado excitado, conocido como el tiempo de vida del estado excitado, no dura mucho tiempo (normalmente entre 1 y 10 nanosegundos). Aun así, este paso en el proceso es increíblemente importante, ya que es durante este tiempo que la energía de S1 comienza a decaer hacia un estado excitado singlete «relajado» desde el que se origina la emisión de fluorescencia.
Paso 3: Emisión
Y finalmente, ¡estamos listos para la fluorescencia! Comenzando en el estado excitado «relajado», el fotón de alta energía decae rápidamente hacia el estado básico y emite este exceso de energía como un fotón de luz. Esta transición de energía es lo que conocemos como fluorescencia. Curiosamente, debido a que parte de esa energía ya fue liberada durante el tiempo de vida del estado excitado, la energía del fotón ahora fluorescente es menor que la energía del fotón de excitación. Por lo tanto, la energía liberada durante la fluorescencia siempre será de una longitud de onda más larga que la necesaria para la excitación.
¿Cómo aprovecha la citometría de flujo las moléculas fluorescentes?
Hemos tratado el concepto y los fundamentos de la citometría de flujo en artículos anteriores y en un seminario web, así que vuelva a repasar el tema si lo necesita.
¿Listo? Vamos!
Cuando se trata de moléculas fluorescentes, debemos prestar especial atención a la diferencia entre las longitudes de onda o energía de excitación y emisión, también conocida como desplazamiento de Stokes. La importancia del desplazamiento de Stokes radica en su simplicidad: nos permite determinar si la longitud de onda de la luz emitida y la longitud de onda de la luz de excitación son lo suficientemente grandes como para distinguirlas de forma fiable. Dado que la lectura de la citometría de flujo se basa únicamente en la fluorescencia, es esencial tener en cuenta este parámetro, o se corre el riesgo de generar datos poco fiables, tipo emoji de caca.
Además, es extremadamente importante hacer un seguimiento del espectro de absorción y del espectro de emisión de cada fluoróforo, y de cómo varios láseres pueden interactuar con el fluoróforo en cuestión. Por ejemplo, en una máquina de citometría de flujo el láser de iones de argón emite 488 nm de luz, que excita el fluoróforo, isotiocianato de fluoresceína (FITC). Como los 488 nm están muy cerca del máximo de absorción del FITC, la excitación da lugar a una alta emisión de FITC. Sin embargo, si el FITC es excitado por otra longitud de onda de un láser diferente dentro de su espectro de absorción, emite luz en el mismo espectro, pero no es de la misma intensidad.
Y ahí lo tiene: una rápida introducción/recuerdo de la fluorescencia y cómo se relaciona con las moléculas fluorescentes utilizadas en la citometría de flujo. ¿Preguntas? ¿Comentarios? Háganoslo saber!