Een vrouw van in de 40 heeft de afgelopen week meerdere “aanvallen” gehad, die steeds vaker voorkwamen. Ze voelt zich licht in het hoofd en reageert dan niet meer. Het duurt meestal ongeveer een minuut en lost dan op. Ze heeft geen pijn op de borst gehad. Ze heeft als kind aanvallen gehad, maar tijdens deze aanvallen is er geen aanvalsactiviteit.
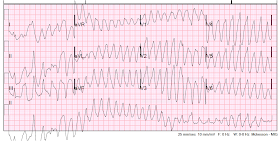
Op de monitor ziet u het volgende:

Ventriculaire tachycardie, snelheid ongeveer 220 slagen per minuut
Tijdens dit ritme was ze wakker, beschermde ze haar luchtwegen, had ze bleekheid, diaphorese en koele ledematen. Polsslag was aanwezig. Er was geen ademnood.
Een ECG met 12 afleidingen werd opgenomen:
VT, en het is “polymorfe” VT omdat de complexen meerdere morfologieën hebben. Koers weer ongeveer 220. Polymorfe VT is ofwel torsade (geassocieerd met een lang QT-interval) of geen torsade (QT niet lang, vaak als gevolg van ischemie)
Op de monitor ging ze spontaan over op een ander ritme, en er werd nog een 12-lead verkregen:

Er is sprake van bigeminy. Smalle complexen worden voorafgegaan door P-golven. Het QRS geassocieerd met de sinusbeats heeft rechterbundeltakblok (RBBB), en lijken geen erg lange QT-intervallen te hebben (ik berekende 400ms QT gedeeld door de vierkantswortel van het voorafgaande R-R-interval = 460ms). De tussenliggende ventriculaire complexen (PVC’s) zien er zeer bizar uit met een lange QT. De PVC’s hebben een grote ST-elevatie (II, III, aVF) met wederzijdse ST-depressie (aVL, precordiaal), wat een inferoposterior STEMI suggereert, maar dit is duidelijk een nabootsing omdat de tussenliggende sinuscomplexen geen ST-elevatie hebben.
Ze ging terug in tachycardie:
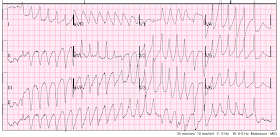
Polymorfe VT opnieuw.
Wat moet er worden gedaan?
Eerst, wat voor soort VT is dit? Polymorfe VT. PMVT wordt gedefinieerd als een breed complex ventriculair ritme met een snelheid van meer dan 100 en een snel veranderende QRS-as en/of morfologie.
Polymorfe VT
Etiologie
Polymorfe VT is ofwel torsades de pointe (geassocieerd met een lange QT op het baseline 12-lead ECG) of niet-torsades (meestal geassocieerd met ischemie of andere organische hartziekte). De aanwezigheid van QT-verlenging op het 12-afleidingen-ECG is niet altijd duidelijk. Torsade de pointes betekent “verdraaiing van de punten” en verwijst naar de veranderende as rond een iso-elektrische lijn.
Morfologie van de PMVT (d.w.z. aanwezigheid van verdraaiing van de punten) alleen kan geen onderscheid maken tussen PMVT ten gevolge van lange QT (torsades) en die ten gevolge van andere etiologieën (niet-torsades). Het is vrijwel onmogelijk pulseloze PMVT te onderscheiden van ventrikelfibrilleren, en studies hebben aangetoond dat de meerderheid van de pulseloze ritmen die torsade lijken te zijn (met “verdraaiing van de punten”) in werkelijkheid ventrikelfibrilleren zijn. Dit onderscheid heeft geen gevolgen voor de onmiddellijke behandeling (defibrillatie), maar wel belangrijke gevolgen voor het voorkomen van verdere hartritmestoornissen.
Torsades Etiologieën van PMVT
1. Verworven: meestal door geneesmiddelen. De lijst is lang. Ook als gevolg van elektrolytische afwijkingen, vooral hypoK en hypoMg. Gecorrigeerd QT-interval (Bazett-correctie = QT gedeeld door de vierkantswortel van het voorafgaande R-R-interval in milliseconden) is meestal groter dan 600 ms. Torsades bij verworven lange QT is veel waarschijnlijker bij bradycardie omdat het QT-interval na een lange pauze nog langer is. Daarom wordt torsade bij verworven lange QT “pauze-afhankelijk” genoemd: als er een sinusklop is na een lange pauze (waardoor een langer QT-interval ontstaat), dan is de kans veel groter dat een vroege PVC (“vroege na-depolarisatie”, EAD) optreedt tijdens de repolarisatie en torsade initieert. De gebruikelijke volgorde is: sinusritme, dan vroege PVC, dan een lange pauze omdat de PVC vroeg was, wat dan resulteert in een bijzonder lang QT, dan weer een PVC met “R op T” die torsades initieert.
2. Aangeboren, met name Congenitaal Lang QT Syndroom. Instabiele PMVT als gevolg van een congenitaal lang QT is veel zeldzamer. (In 26 jaar EM en 125.000 patiënten heb ik nog nooit een geval gezien van torsade PMVT als gevolg van congenitale lange QT). Congenitale oorzaken van torsade omvatten “catecholaminerge PMVT”, waarbij er geen zichtbare QT verlenging is op de 12-lead, maar men denkt dat het een vergelijkbare etiologie heeft. Preventieve therapie van congenitale lange QT omvat het gebruik van bètablokkers (hetzelfde als bij catecholaminerge PMVT, aangezien in beide gevallen bètastimulatie torsade uitlokt); dit in tegenstelling tot verworven lange QT, die kan worden behandeld met bètastimulatie (isopreterenol).
Ik heb geen aanbevelingen gevonden om bètablokkers te gebruiken voor acuut beheer van torsade in deze groep, maar het is bijna onmogelijk om te zeggen of isoproterenol de zaken slechter of beter zal maken voor een gegeven patiënt met congenitale lange QT (zie commentaar van onze elektrofysioloog aan het eind). Het lijkt erop dat de meeste symptomatische patiënten met congenitale lange QT zich presenteren na syncope, of gereanimeerd v fib, en zelden presenteren met aanhoudende torsade of instabiliteit. De behandeling van deze patiënten bestaat dus hoofdzakelijk uit herkenning en preventie van toekomstige syncope en plotselinge hartdood, gewoonlijk met een implanteerbare debribrillator als aanvulling op bètablokkers. Torsades van aangeboren lange QT kunnen worden geïnduceerd door het gebruik van QT-verlengende geneesmiddelen.
Niet-Torsade Etiologieën van PMVT
meest voorkomend door ischemie. Dit zijn bijna altijd openlijke, ernstige episoden van ischemie, met pijn op de borst en/of eenduidige ischemische ECG-afwijkingen. Ook als gevolg van reeds bestaande cardiomyopathie.
Behandeling van polymorfe VT
De meeste torsade is zelfbegrenzend. Als het niet spontaan converteert, dan is defibrillatie nodig als de patiënt onstabiel is. Als de torsade wel converteert, is de kans op herhaling groot en is de therapie gericht op het voorkomen van herhaling.
Therapie van Acute Episoden van Torsades:
1. Cardioversie of defibrillatie indien actief, vooral indien instabiel
2. Verwijdering van de veroorzaker van de storing bij verworven lange QT
3. Correctie van hypoK, zelfs tot licht supranormale niveaus
4. Toediening van 2-4g MgSO4, zelfs indien de Mg-spiegel normaal is (een infuus van 3-10 mg per minuut kan nuttig zijn)
5. Alleen als het verworven lange QT is: beta-adrenerge stimulatie met isoproterenol
6. Als deze niet werken, dan zal overdrive pacing, meestal met een snelheid van ongeveer 100 om pauzes te voorkomen, bijna altijd werken (transcutane pacing is prima voor tijdelijke verlichting als overbrugging naar transveneuze pacing).
7. Lidocaïne kan ook van nut zijn omdat het de PVC’s (vroege na-depolarisaties) kan onderdrukken die torsade inleiden als ze op de T-golf optreden.
8. Amiodaron heeft twijfelachtige voordelen en is mogelijk schadelijk. Op zichzelf verlengt het het QT-interval, zonder echter het risico van torsades sterk te verhogen
9. Geef geen bètablokkers tenzij bij de patiënt de diagnose congenitaal lang QT is gesteld. Juist het omgekeerde: isoproterenol.
10. Als het congenitaal is, dan kan acute bètablokkade geïndiceerd zijn. Ik zou eerst esmolol proberen, omdat het kan worden uitgezet. Het heeft echter geen bèta-2 blokkade en het is mij onduidelijk of dit belangrijk en/of noodzakelijk is. Als esmolol niet werkt, dan zou IV propranolol gegeven moeten worden. Propranolol en Nadolol zijn de beste lange termijn bètablokkers voor congenitale lange QT en de bèta 1 selectieve metoprolol is niet erg effectief. Of dit komt door de beta selectiviteit is mij niet duidelijk.
Hier is een fascinerend geval van congenitale lange QT met Torsade. Er is een geweldige discussie over de rol en functie van bètablokkade bij congenitale lange QT.
Therapie van Acute Non-Torsade PMVT: Vergelijkbaar met Monomorfe VT
1. Cardioversie of defibrillatie indien actief
2. Correctie van elektrolytstoornissen, met name hypoK of hypoMg
3. Preventie van verdere episoden met lidocaïne of amiodaron, eventueel een bètablokker zoals esmolol (die u zou vermijden bij alle verworven lange QT Torsades).
4. Anti-ischemische therapieën, tot en met revascularisatie
5. Implanteerbare cardioverter-defibrillator kan noodzakelijk zijn, zelfs bij succesvolle revascularisatie
Terug naar onze casus
Cardioversie is alleen geïndiceerd wanneer de patiënt in torsade is, en zal slechts tijdelijk werken, aangezien de patiënt in en uit het ritme gaat. Preventie van verdere episoden is essentieel.
In dit geval zien we alleen een lange QT bij de PVC’s, maar niet bij de oorspronkelijke RBBB-slagen. Vaak is de torsade “pauze-afhankelijk” en kan alleen worden gezien in een complex dat volgt op een lange pauze. Er is geen pijn op de borst, en we hebben geen bewijs van ischemie op de sinus ECG-complexen. Polymorfe VT kan alleen aan ischemie te wijten zijn als er eenduidige ECG-bevindingen van ischemie zijn. Dus dit alles is suggestief voor torsades, maar niet diagnostisch. De patient gebruikte geen bekende medicatie die het QT interval verlengt. Ze heeft alleen een voorgeschiedenis van de ziekte van Graves en meldt dat ze van alle medicatie af is.
Wanneer ze niet in VT is, is haar bloeddruk verhoogd tot 190/80 met een voelbare pols van 90 en zuurstofsaturatie van 99.
Een eerste K was normaal. Mg-spiegel was op dit moment onbekend.
Op t = 12 werd 2 gram IV Magnesium gegeven.
Op t = 13 minuten werd 150 mg amiodarone gegeven
Op t = 15 minuten werd 100 mg lidocaïne gegeven
Op t = 30 minuten was er geen verbetering en werden esmolol bolus en infuus gegeven. Isoproterenol moest worden gegeven.
Het cath lab werd geactiveerd. Nog eens 2 gram IV Magnesium werd gegeven.
t = 64 minuten: K komt terug op 2,4 mEq/L (aanvankelijke waarde was foutief). Dit suggereert Torsade nog sterker. KCl gegeven in centrale lijn. Amiodarone infuus gestart. Rectaal aspirine gegeven.
t = 79 minuten: Procainamide 1500 mg over 2 minuten gegeven. (Procainamide kan nuttig zijn bij PMVT zonder torsade, maar zal waarschijnlijk de QT verlengen en torsades instabieler maken. Het is ook een sterk negatief inotroop middel en kan gevaarlijk zijn bij een slechte LV-functie.)
t = 97 minuten: patiënt naar cath lab gebracht:
De patiënt werd naar het cath lab gebracht en er werd een pacer geplaatst. Het ritme werd opgevangen met overdrive pacing en vervolgens vertraagd. Er was diffuse coronaire ziekte, maar geen culprit laesie (geen acuut coronair syndroom). Troponine was negatief.
Er werd vastgesteld dat de patiënt methadon gebruikte en methadon-toxisch was. Het is een van de vele medicijnen die een lange QT veroorzaakt. Dit was Torsade de Pointes door een lang QT als gevolg van methadon en hypokaliëmie.
Hier is de 12-lead tijdens pacing:
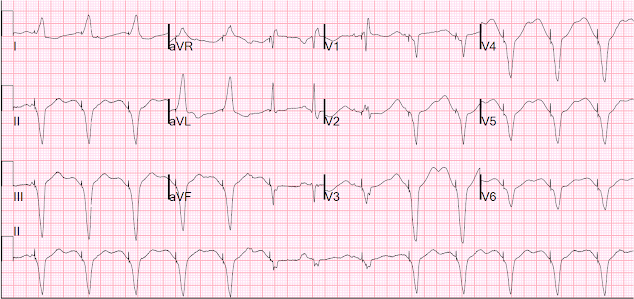
Tijdens pacing
Hier is er nog een met de pacer uitgezet, de volgende dag:
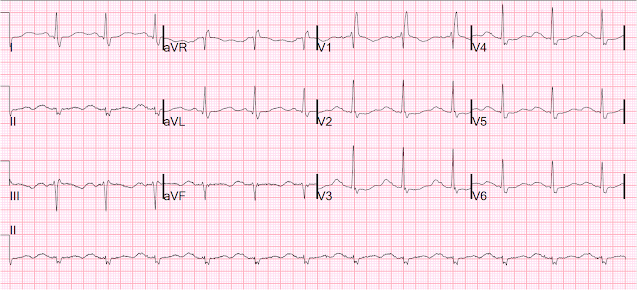
Sinus met RBBB en zeer lange QT
En dan op de vierde dag:
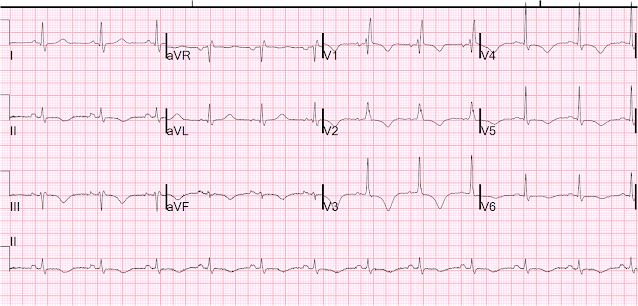
T-golfinversies, QT nog steeds lang
Omwille van de buitengewoon lange halfwaardetijd van methadon duurde het dagen voor de QT verkort was. Uiteindelijk ging het goed met de patiënt.
Opmerking over het gebruik van isoproterenol bij congenitale lange QT:
Ik stelde onze elektrofysioloog (Rehan Karim) de volgende vraag:
“Ik wil zeker weten dat ik het goed heb:
Voor congenitale lange QT is bètablokkade chronisch geïndiceerd, en voor een patiënt met recidiverende VT die in het ziekenhuis ligt, zou men GEEN isoproterenol geven.
Alleen verworven lange QT is “pauze-afhankelijk” en verbetert met een snellere hartslag, en bètablokkade is NIET geïndiceerd. In plaats daarvan is isoproterenol geïndiceerd (en overdrive pacing).
Kunt u mij hierin corrigeren?”
Met andere woorden:
Hier is zijn antwoord:
“Ik zou willen dat alles duidelijk genoeg was om alles in een algoritmische vorm te gieten… maar helaas is dat niet het geval.”
Het hangt er echt van af met wat voor soort aangeboren lange QT je te maken hebt, en zelfs als je het weet – zijn de dingen niet zo eenduidig.
Hier een voorbeeld:
Aangeboren lange QT type-3 is een natriumkanaalmutatie (SCN5A) – dat is hetzelfde gen als Brugada syndroom.
Lange QT type 3 heeft wel pauze-afhankelijke Torsades. In deze situatie worden echter nog steeds bètablokkers gebruikt (nadat natuurlijk atriale pacing is ingesteld om bradycardie te voorkomen) – dit is in de eerste plaats voor het effect van bètablokkers op het verminderen van de QT dispersie.
Even ingewikkelder… klasse I-B natriumkanaalblokker (Mexiletine) wordt soms gebruikt voor LQT-3.
Voor zover ik weet zijn de bètablokkers waarschijnlijk niet zo effectief bij LQT-3 als bij andere vormen – maar ze worden nog steeds gebruikt.
Daarom denk ik niet dat het mogelijk is om met de kennis die we op dit moment hebben met een ja/nee antwoord te komen – dingen moeten in klinisch perspectief worden gezien.
Als iemand duidelijk pauze-afhankelijke torsades heeft, en niet wordt gepaced – zal ik GEEN bètablokker gebruiken, maar in plaats daarvan proberen de snelheid te verhogen door isoproterenol te gebruiken.
Dr. Karim voegde hieraan toe:
Dit is een van de verwarrende onderwerpen – in feite zijn de meeste genetische aritmieën / chanellopathieën behoorlijk uitdagend om klinisch te behandelen. We zijn zo gewend om gegevens te zien van duizenden patiënten in cardiologische trials – en dan komen we in dergelijke situaties waar de ziektelast niet groot genoeg is om ons andere gegevens te geven dan registers van grote klinische centra.