A kémikusok nagyra értékelik az izotópokat, és használják őket az alap- és alkalmazott kutatásban. Azonban jobban foglalkoztatja őket az elektronok mozgása. Amikor egy atom elektronokat nyer vagy veszít, töltött fajjá vagy ionná válik. Ilyenkor az atommag nem változik. Az elektronokat vesztő atomok esetében összességében pozitív töltés keletkezik (#protonok > #elektronok). Az ilyen típusú ionokat alkotó atomokat kationoknak nevezzük. A fématomok (a periódusos rendszer bal oldalán találhatók) mindig elektronokat veszítenek, és így kationokká alakulnak.
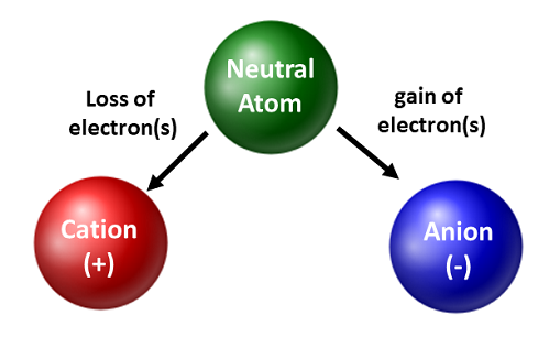
A fématomokkal ellentétben a nemfémek elektronokat nyernek, és anionokká alakulnak. Az ilyen típusú ionok összességében negatív töltéssel rendelkeznek (#elektronok > #protonok). A nemesgázok kivételével a periódusos rendszerben minden atom elektronokat veszít vagy nyer az elektronstabilitás elérése érdekében. Különböző típusú kötések jönnek létre, amikor az atomok elektronokat veszítenek, nyernek vagy osztoznak rajtuk. Az atomi kötések ezen típusait a tankönyv 4. fejezetében tárgyaljuk bővebben.
Interaktív: Atomépítés
Építsünk atomot protonokból, neutronokból és elektronokból, és nézzük meg, hogyan változik az elem, a töltés és a tömeg. Ezután játssz egy játékot, hogy teszteld az ötleteidet!
Ezzel a ponttal ki kell tudnod számítani az összes szubatomi részecskét, ha adott egy adott ion töltése. Ezenkívül el kell sajátítanod az ionok osztályozását (felismerve, hogy a kationok pozitívak, az anionok pedig negatívak). Az egyes ionok töltéseinek memorizálására a tankönyv 4. fejezetének feldolgozása során lesz szükség. Egyelőre az ionok töltéseit adjuk meg, és nem kell memorizálni. Jegyezzétek meg és értékeljétek a főcsoportba tartozó elemek iontöltéseit az alábbi periódusos rendszerben. Végül, a kémikusok nem írnak számot az egyes (1) számot tartalmazó töltésekhez. Ezeknél a fajoknál csak egy + vagy – jelet fog látni. A nagyobb nagyságú töltésekhez mindig tartozik egy szám az elem szimbólumához.
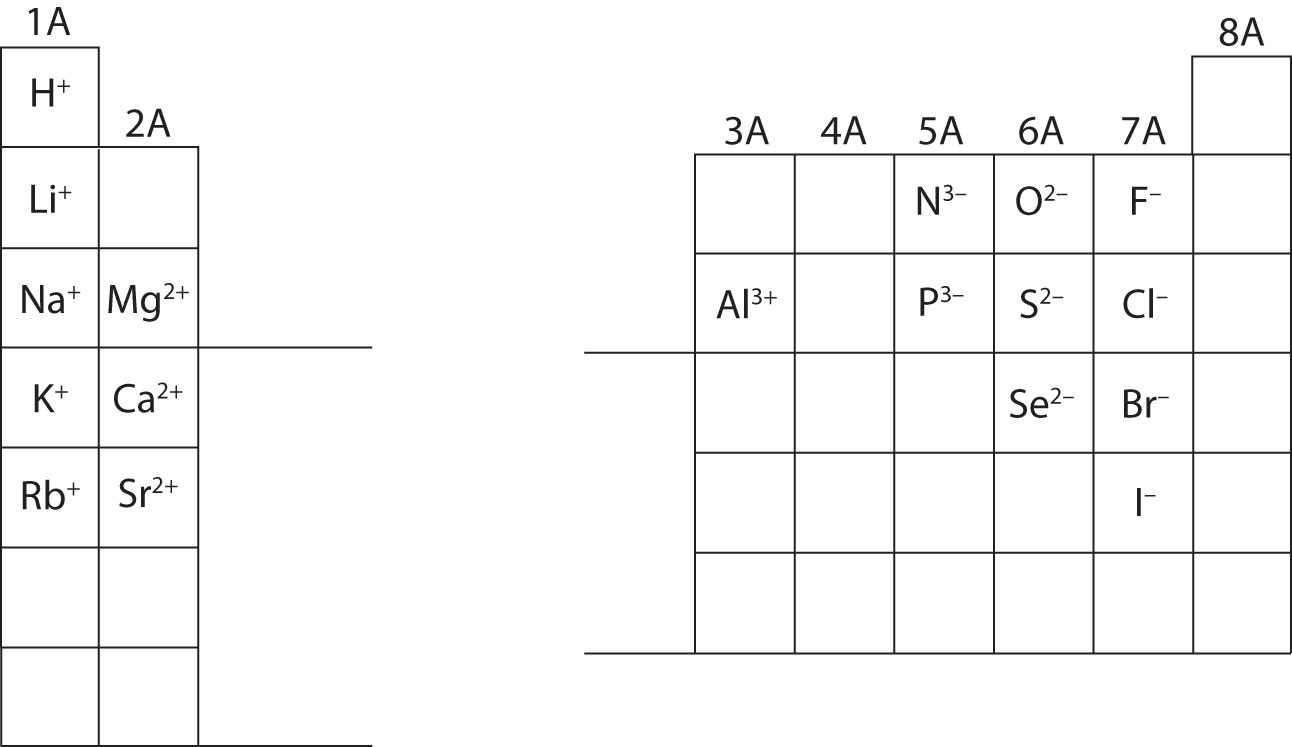
Példa \(\PageIndex{1}\): \(\PageIndex{2}\) ábra információi alapján számítsuk ki az alábbi fajok szubatomi részecskéit. Jelöljön meg minden egyes részecskét atomként, kationként vagy anionként. A tömegeket, az atomszámokat és az ionok fajlagos töltéseit lásd a periódusos rendszerben.
- Alumíniumion
- Cirkóniumatom
- Kénion
Megoldások
- Az alumíniumionban 13 proton, 14 neutron és 10 elektron van. Ez az ion pozitív töltésű, ami azt jelenti, hogy elektronokat vesztett és kationt alkot.
- A cirkóniumatomban 40 proton, 51 neutron és 40 elektron van. Ez egy olyan atom, amelynek nincs teljes töltése.
- A kénionban 16 proton, 16 neutron és 18 elektron van. Ez az ion negatív töltésű, ami azt jelenti, hogy elektronokat nyert és aniont alkot.
Példa \(\PageIndex{2}\): A/Z és szimbólum tömegjelölések
Az előző kérdésben szereplő ionok/atomok A/Z és szimbólum tömegjelölései.
megoldások
- \(\ce{^{27}_{13}Al^{3+}}\) és Al-27
- \(\ce{^{91}_{40}Zr}\) és Zr-91
- \(\ce{^{32}_{16}S}^{2-}\) és S-32
Ha egy atom elektronokat nyer vagy veszít, ezt A/Z formátumban kell ábrázolni. A szimbólum-tömeg formátum nem jeleníti meg az ion töltését. Ne feledje, a neutronokat és a protonokat nem befolyásolják az elektronok változásai.
Kell még gyakorolni?
- Kanyarodjon vissza a 3. szakaszhoz.E részéhez, és dolgozza fel az 5. és 9. feladatot.
Munkatársak
-
Elizabeth R. Gordon (Furman University)