さて、全体像を見てみましょう。 酸や塩基にも他のものと同じように目盛りがあります。 ここで知っておくべき定義をいくつか挙げてみよう。
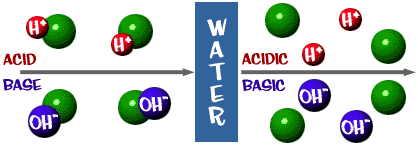
酸。 H+イオンが過剰な溶液。 ラテン語で「鋭い」「酸っぱい」を意味するacidusに由来する。
塩基(えんき)。 OH-イオンが過剰に存在する溶液。 塩基の別称はアルカリ。
水溶液。 水を主成分とする溶液。 水族館という言葉を考えてみてください。 AQUAは水を意味します。
強酸。
強酸:pHが非常に低い酸(0-4)。 pHが非常に高い塩基(10-14)。
弱酸性: 水溶液中で部分的にしか電離しない酸。 つまり、すべての分子がバラバラになるわけではない。 弱酸は通常、pHが7に近い(3~6)。
弱塩基。 水溶液中で部分的にしか電離しない塩基。 これは、すべての分子がバラバラにならないことを意味する。 弱塩基は通常、pHが7に近い(8~10)。
中性。 pH7で、酸性でも塩基性でもない溶液。
アレニウスという人物と、水素イオンと水酸化物イオンの濃度に関する彼の考えについてお話しました。 また、ブレンステッド-ローリーの考えについても学びます。 デンマークとイギリスの二人の化学者は、酸をドナー、塩基をアクセプターとして捉えました。 彼らは何を提供し、何を受け入れたのでしょうか? 水素イオンです。 これは、酸が分解して水素イオンを放出する、という最初の定義とよく似ています。 この新しい定義は、もう少し詳細です。 科学者たちはこの新しい定義を使って、アンモニア(NH3)のような塩基をより多く表現するようになりました。 塩基はプロトン受容体なので、アンモニアがH+を受容してアンモニウムイオン(NH4+)を生成するのを見たとき、塩基とラベル付けすることができたのです。 水酸化物イオンの心配はもうしなくていいのです。 もしアンモニアが水分子からH+を受け取ったのなら、水(H2O)がプロトン供与体であることになります。 ということは、この状況では水が酸だったということですか?
ルイスという化学者は、酸と塩基を見る第三の方法を提示しました。 水素イオンを見る代わりに、彼は電子のペアを見ました(「原子と元素」のドット構造の絵を覚えていますか)。 ルイスの考えでは、酸は電子のペアを受け入れ、塩基は電子のペアを提供します。 このように、酸と塩基は全く逆の言葉で表現されていますが、その考え方は同じです。 水素イオンはやはり2個の電子を受け入れて結合を形成したい。 塩基は電子を手放したいと思っている。 全体として、ルイスの定義は、さらに多くの化合物を酸または塩基に分類することができました。
何が本当に起こるのでしょうか? ここで少し厄介なことになります。 念のため、水溶液中の分子の分解をもう1度見てみましょう。 酸とは、水溶液の中で水素(H+)イオンと別の化合物に解離(分解)する化合物のことです。 酢酸の例、覚えていますか? 塩基は、水溶液の中で水酸化物(OH-)イオンと別の化合物に分解する化合物です。 重曹の話も少しします。
少し言い方を変えましょう。 イオン性・電解性の化合物があって、それを水の中に入れると、2つのイオンに分解されます。 そのイオンの1つがH+であれば、その溶液は酸性になります。 強酸の塩化水素(HCl)がその一例です。 イオンの1つがOH-であれば、その溶液は塩基性である。 強塩基の例は、水酸化ナトリウム(NaOH)です。 他にも酸性や塩基性の溶液を作るイオンはありますが、ここでは触れません。
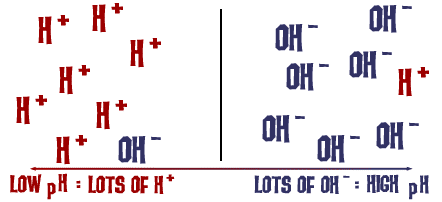
私たちが話したpHスケールは、実際には溶液中のH+イオンの数を示すものです。 H+イオンがたくさんあれば、pHは非常に低くなります。 H+イオンの数に比べてOH-イオンが多ければ、pHは高くなります。
この考えについて少し考えてみましょう。なぜNaOHを多く含む液体は非常に塩基性でありながら、同時に危険なのでしょうか。 溶液中でNa-OH結合が切れ、ナトリウムイオン(プラス)と水酸化物イオン(マイナス)ができます。 ナトリウムイオンは溶液中ではそれほど危険ではありませんが、H3O+(ヒドロニウムイオン)として浮遊している水素イオンに比べて、溶液中には膨大な数の水酸化物イオンがあります。これらの過剰なOH-イオンがすべてpHを非常に高くし、溶液は多くの化合物と容易に反応することになります。 同じことが、より危険の少ない規模で、水に重曹を加えたときにも起こります。 解離の際に、溶液中にOH-イオンと炭酸が放出されます。 OH-イオンの数はH3O+イオン(H+とH2O)の数より多くなり、pHは上昇します。 ただ、水酸化ナトリウムのときほど強い差はありません
基本的には以上です。 (ハハ!わかった?)
詳細は前編で…
関連動画…
Encyclopædia Britannica: 塩基
Wikipedia.org ウィキペディア:酸
ウィキペディア:酸
ウィキペディア:酸 塩基
百科事典ドットコム 酸
百科事典.com: 塩基
のページです。