La valutazione del percorso visivo può essere parte integrante della diagnosi e della gestione di numerose condizioni.
Di Kristie Draskovic, OD, e John J. McSoley, OD
- Release Date:
- Scadenza:
- Dichiarazione sugli obiettivi:
- Facoltà/Comitato editoriale:
- Credit Statement:
- Dichiarazione di sponsorizzazione congiunta:
- Dichiarazione di divulgazione:
- Caso 1. Macroadenoma ipofisario
- Tabella 1. Neuropatie ottiche comunemente rilevate con test del campo visivo
- Caso 2. Sclerosi multipla
- Caso 3. Difetto di glaucoma paracentrale
- Tabella 2. Criteri per il difetto del campo visivo glaucomatoso con alta specificità e sensibilità13,14
- Tabella 3. Suggerimenti per giudicare la progressione
Release Date:
Marzo 2016
Scadenza:
1 marzo 2019
Dichiarazione sugli obiettivi:
Esaminare i campi visivi utilizzando la perimetria automatizzata può aiutare i medici a valutare le lesioni che interessano le vie visive, stabilire linee di base e verificare alcune neuropatie ottiche indotte da farmaci. Può anche aiutare a monitorare la progressione o la ricorrenza delle malattie, guidare le decisioni di trattamento e aiutare a localizzare le lesioni. Questo articolo aiuterà i medici a comprendere meglio e ad interpretare i campi visivi nei processi patologici glaucomatosi e non glaucomatosi.
Facoltà/Comitato editoriale:
Kristie Draskovic, OD, e John J. McSoley, OD
Credit Statement:
Questo corso è approvato da COPE per 2 ore di credito CE. L’ID COPE è 48599-GL. Si prega di controllare il vostro consiglio di licenza statale per vedere se questa approvazione conta per il vostro requisito CE per la ri-licensura.
Dichiarazione di sponsorizzazione congiunta:
Questo corso di formazione continua è sponsorizzato congiuntamente dal Pennsylvania College of Optometry.
Dichiarazione di divulgazione:
I dottori Draskovic e McSoley non hanno relazioni finanziarie da rivelare.
L’esame del campo visivo è essenziale quando si considera la potenziale perdita della vista da condizioni che colpiscono il percorso visivo. La perimetria automatica standard è uno strumento utile per identificare e seguire molte condizioni neurologiche, così come il glaucoma e i sospetti di glaucoma. Mentre diversi dispositivi sono attualmente disponibili, la seguente discussione considererà l’uso dell’Humphrey Field Analyzer (HFA, Zeiss) come esempio.
Anatomia e fisiologia
Grazie all’anatomia della via visiva, i medici possono individuare le aree di preoccupazione in molte condizioni che causano problemi visivi (Figura 1). Poiché la luce che viaggia dal campo visivo temporale cade sulla retina nasale, le lesioni retiniche sono viste nel quadrante esattamente opposto del campo visivo. Tutte le lesioni prechiasmatiche, comprese quelle sulla retina e sul nervo ottico, daranno luogo a difetti isolati all’occhio colpito.1
Siccome le fibre nasali sono responsabili del campo visivo temporale, una lesione al chiasma ottico darà luogo a un difetto del campo visivo che interessa il campo temporale di entrambi gli occhi, e dà origine alla classica emianopsia bitemporale, che rispetta la linea mediana verticale.1 Le lesioni del chiasma ottico possono essere il risultato di adenomi pituitari, meningiomi soprasellari, craniofaringiomi o aneurismi. In alcuni casi, i difetti del campo visivo possono regredire dopo aver trattato la causa.2
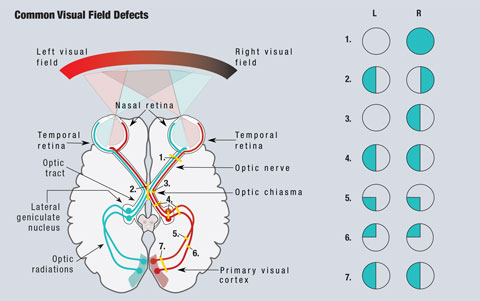
Clicca sull’immagine per ingrandirla. Fig. 1. Viene mostrato uno schema semplificato della via visiva. Le lesioni che interrompono la via visiva portano a difetti del campo visivo. (1) Una lesione completa del nervo ottico destro porta alla perdita completa del campo visivo destro. (2) Una lesione nella linea mediana del chiasma ottico porta a un’emianopsia bitemporale. (3) Una lesione delle fibre non incrociate del nervo ottico destro al chiasma ottico porta a un’emianopsia nasale dell’occhio destro. (4) Una lesione completa del tratto ottico destro, del nucleo genicolato laterale o delle radiazioni ottiche provoca un’emianopsia omonima sinistra completa. (5) Una lesione delle radiazioni ottiche superiori di destra provoca una quadranopsia inferiore sinistra. (6) Una lesione delle radiazioni ottiche inferiori di destra provoca una quadranopsia superiore sinistra. (7) Una lesione delle radiazioni ottiche superiori e inferiori di destra provoca un’emianopsia omonima sinistra. Illustrazione di Miquel Perello Nieto.
Le fibre responsabili del campo visivo a destra della linea mediana si trovano sul lato sinistro del cervello, e viceversa. Come risultato di questo incrocio, tutte le lesioni post-chiasmatiche, comprese le lesioni del tratto ottico e delle radiazioni ottiche, causano un’emianopsia omonima.1 Questi difetti si trovano sullo stesso lato del campo visivo in ogni occhio e rispettano la linea mediana verticale. Quando i difetti si vedono solo superiormente o inferiormente, si parla di quadranopsia. Nel caso di difetti di emianopsia incompleta, le lesioni anteriori sono di solito più incongrue, mentre le lesioni posteriori saranno più congrue tra i due occhi.1
La perdita del campo visivo glaucomatoso rappresenta un danno agli assoni che viaggiano lungo lo strato di fibre nervose retiniche e di solito segue un modello arcuato al nervo ottico. Il danno a questi assoni darà origine a difetti localizzati del campo visivo, più comunemente scotomi arcuati, passi nasali e scotomi paracentrali. Un campo visivo normale si estende temporalmente fino a 90 gradi, 70 gradi sia superiormente che inferiormente e 60 gradi nasalmente e dalla fissazione. Le informazioni più preziose per i deficit neurologici e la gestione del glaucoma si ottengono entro 30 gradi dalla fissazione.2
Strategia di test
La perimetria statica automatizzata – e la perimetria a soglia in particolare – presenta uno stimolo di dimensione fissa ma di intensità variabile. La sensibilità delle diverse sedi di test viene registrata in base alle risposte del paziente a questi stimoli. Uno stimolo di dimensione III (che è di 4 mm2 quando viene proiettato su una ciotola di 30 cm) è comunemente usato nella pratica clinica.
Ci sono diversi modelli di test di soglia disponibili. Il modello di test 30-2 testa 76 posizioni entro 30 gradi dalla fissazione, mentre un modello di test 24-2 testa 54 posizioni rimuovendo l’anello di punti a 30 gradi (tranne i due punti che sono a cavallo del meridiano orizzontale nasale). Questi punti più periferici sono più soggetti alla variabilità, e il 24-2 accorcia il tempo del test eliminando questi punti periferici dal test. La distanza tra i punti del test è di sei gradi.
Inoltre, il modello di test 10-2 mira a 64 punti entro 10 gradi dalla fissazione separati da due gradi. Questa opzione è preferibile quando i difetti centrali o paracentrali emergono con il 24-2 e il 30-2 o quando il campo diventa così ristretto che i punti periferici non sono clinicamente utili. I clinici possono anche scegliere di aumentare la dimensione dello stimolo a V, che può permettere valori di sensibilità più alti e una gamma dinamica più ampia attraverso la quale seguire i pazienti per il cambiamento. Tuttavia, attualmente non esiste un algoritmo di test di tipo SITA, né è disponibile un confronto con un database normativo o un’analisi della progressione.
Caso 1. Macroadenoma ipofisarioUn paziente si è presentato per una consultazione nell’ambito di un glaucoma atipico e progressivo a tensione normale. |
|
|

|
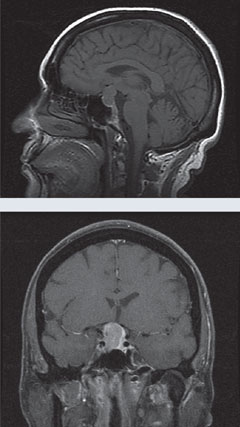
| Sopra, il campo visivo 24-2 del paziente dimostra una perdita del campo visivo bitemporale. Nelle risonanze magnetiche a sinistra, le viste sagittale T1 senza gadolinio e coronale T1 con gadolinio rivelano una grande massa sellare con lieve miglioramento ed effetto compressivo sul chiasma. Questo risultato è coerente con macroadenoma ipofisario. Cliccare le immagini per ingrandire. |
|

|
|
| Dopo che il paziente è stato sottoposto a chirurgia transphenoidal per rimuovere la massa sellar, il campo visivo, sopra, mostra il miglioramento del difetto del campo visivo nell’occhio destro e la risoluzione del difetto nell’occhio sinistro. Clicca sull’immagine per ingrandirla. | |
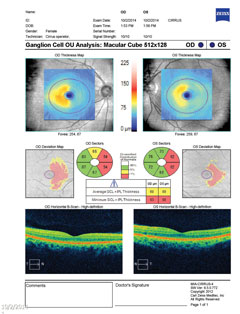
| Sopra, il complesso delle cellule gangliari rivela un assottigliamento nasale in entrambi gli occhi, che è correlato alla perdita del campo visivo temporale. Clicca sull’immagine per ingrandirla. | |
Studi recenti dimostrano che i campi visivi 10-2 possono essere utili per identificare un glaucoma più che avanzato.3,4 Uno studio ha rivelato che alcuni pazienti con glaucoma avevano significativi difetti del cluster centrale visti sui modelli di test 10-2 nonostante un normale campo visivo centrale 30-2.4 Lo studio suggerisce che, a causa dello scarso campionamento spaziale, il deterioramento glaucomatoso del campo centrale non poteva essere rilevato dalla sola griglia del test 30-2, ed era necessaria una stima più densa dei 10 gradi centrali.4 Suggerisce inoltre che la modifica del modello convenzionale di test del campo visivo potrebbe migliorare l’individuazione dei difetti glaucomatosi precoci nei 10 gradi centrali.4
Nella pratica quotidiana, i medici spesso eseguono campi 10-2 quando piccoli scotomi centrali o paracentrali appaiono sui test 30-2 e 24-2, o quando l’acuità è sospettata o rischia di essere depressa a causa della perdita di campo. Inoltre, un modello di test 10-2 può essere un utile complemento quando c’è un’alta variabilità inter-test dei punti paracentrali su un modello 24-2. La crescente attenzione alla funzione delle cellule gangliari nella regione maculare potrebbe anche aumentare l’attenzione all’area del campo visivo testata dal modello 10-2.
Affidabilità
Indicazioni di affidabilità delle prestazioni del campo visivo includono perdite di fissazione e risposte sia false positive che false negative.
Tabella 1. Neuropatie ottiche comunemente rilevate con test del campo visivo |
|
| Ipertensione intracranica idiopatica | Presto: punto cieco ingrandito Tardivo: costrizione generalizzata5,6 (può migliorare con il trattamento) |
| neurite ottica | – Perdita diffusa del campo visivo (in quasi la metà dei casi) – Altro: difetto altitudinale, scotomi centrali o cecocentrali, difetti arcuati o doppi arcuati e difetti emianopici5,7 |
| Neuropatia ottica ischemica anteriore non arteritica | – Difetti altitudinali che rispettano la linea mediana orizzontale sono più comuni – Altro: scotomi centrali, difetti arcuati e quadranopsie5,8 |
| Neuropatia ottica ischemica posteriore | – Difetto di campo centrale5,9 |
| Neuropatie ottiche ereditarie – Neuropatia ottica ereditaria di Leber – Atrofia ottica dominante |
– Perdita del campo visivo cecocentrale e centrale5 |
| Drusen della testa del nervo ottico | – Può imitare un modello glaucomatoso |
| Oftalmopatia tiroidea | – Grande variabilità – Può risolversi parzialmente o completamente dopo il trattamento2 |
| Neuropatia ottica tossica indotta da farmaci | – La tossicità dell’etambutolo (per il trattamento della tubercolosi) può causare scotomi centrali e, meno comunemente, costrizione periferica e difetti altitudinali5 – Vigabatrin (un farmaco antiepilettico), può causare difetti di campo che iniziano come difetti nasali bilaterali e successivamente progrediscono in difetti di campo concentrici mentre il campo centrale rimane intatto12 |
La fissazione può essere monitorata dalla presentazione periodica di uno stimolo al punto cieco fisiologico (metodo Heijl-Krakau) o dal monitoraggio della posizione del riflesso luminoso corneale. Sull’HFA, la deflessione verso l’alto indica un cambiamento di posizione o di fissazione; la deflessione verso il basso indica che il riflesso luminoso corneale non può essere localizzato, come durante un cambiamento di posizione della testa o delle palpebre.
I falsi positivi si verificano quando un paziente risponde in un momento in cui non c’è uno stimolo associato o quando una risposta non è fisiologicamente possibile. I pazienti con alti falsi positivi sono spesso descritti come “trigger happy”. Questo può rivelare un campo visivo che appare più sensibile o più normale del previsto o può portare a valori di sensibilità di soglia anormalmente alti.
I falsi negativi si verificano quando un paziente non risponde a uno stimolo più luminoso di uno già visto o quando la risposta non è coerente con il modello di risposte in quella regione. Il valore falso negativo può essere un’indicazione di affidabilità o un riflesso del processo della malattia. Le regioni anormali del campo visivo sono associate a una maggiore variabilità intra-test e inter-test. Di conseguenza, le regioni del campo visivo con bassa sensibilità non sono incluse nel calcolo del valore falso negativo.
La sensibilità di soglia è un dato grezzo con valori registrati in decibel. I numeri indicano il grado di attenuazione dallo stimolo massimo possibile. Valori di
La deviazione totale rappresenta la deviazione dai valori attesi basati sul database dei normali abbinati per età. La deviazione del modello corregge la sensibilità complessiva del campo rimuovendo le depressioni generalizzate (ad esempio, dalla cataratta) per identificare eventuali aree di anomalie localizzate. Sia la deviazione totale che quella del pattern hanno valori di probabilità associati (p) calcolati in base alla distribuzione all’interno di una popolazione normale. L’intervallo dei valori normali è più ampio alla periferia che al centro. I simboli p indicano la frequenza con cui il valore testato si verifica in una popolazione normale e di pari età. Le deviazioni sono mostrate sulla mappa se la soglia testata è peggiore del 5% inferiore del normale per quell’età.2 Per esempio, se p
Caso 2. Sclerosi multiplaUn paziente con diagnosi di sclerosi multipla (SM) ha presentato una perdita della vista. |
|
|
 |
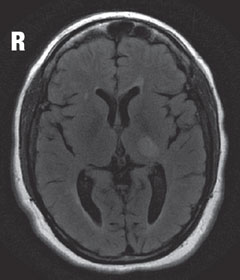
| Sopra, nella RM, la vista assiale T2 flair rivela una lesione focale iperintensa appena posteriore al nucleo genicolato laterale sinistro nel talamo, che è responsabile del difetto del campo visivo visto. La lesione vista, così come altre lesioni iperintense multiple, sono caratteristiche tipiche della malattia demielinizzante come la SM. | |
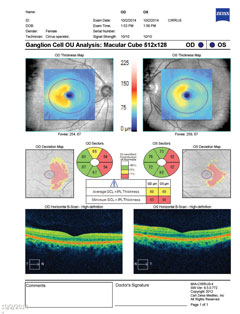
|
|
| Sopra, il campo visivo dimostra una emianopia omonima destra incompleta. Clicca l’immagine per ingrandire. A sinistra, l’analisi delle cellule gangliari rivela un assottigliamento nasale nell’occhio destro e temporale nell’occhio sinistro, che è coerente con i risultati del campo visivo. Clicca sull’immagine per ingrandirla. |
|
La deviazione standard del modello (PSD) è una deviazione standard ponderata dal valore atteso sulla base dei valori normali corrispondenti all’età e dell’indice di deviazione media (MD). La PSD rivela la distanza tra diversi punti all’interno del campo. Il PSD è sensibile ai difetti del glaucoma sia precoci che focali. Un basso valore di PSD può essere visto con campi visivi normali, un campo visivo uniformemente depresso o un campo completamente cieco. Un valore p associato è la probabilità che il valore si verifichi.
Il MD è una media ponderata dei valori nel grafico numerico della deviazione totale. Il MD può essere influenzato da una diminuzione diffusa della sensibilità complessiva o da un difetto localizzato. Una MD di 0 indica un valore normale, mentre un valore negativo rappresenta una deviazione o una perdita dal database normale. La deviazione media pesa di più i punti centrali.
L’indice del campo visivo (VFI) è un’altra valutazione corretta in base all’età, espressa in percentuale, dove il valore perimetricamente normale è 100% e il valore perimetralmente cieco è 0%. Quando si calcola il VFI, i punti centrali sono pesati più forte dei punti periferici. Fornisce un punteggio per un campo visivo individuale e viene utilizzato nell’analisi della progressione.2
Il test dell’emisfero del glaucoma (GHT) confronta la sensibilità relativa dei valori di deviazione del modello di cinque zone negli emisferi superiore e inferiore. Ciascuna di queste zone viene confrontata con la sua zona speculare nell’emisfero opposto, ed entrambe le zone vengono confrontate con il database normativo. Il GHT può rilevare la perdita del campo visivo glaucomatoso con alta sensibilità e alta specificità attraverso cinque possibili categorie: al di fuori dei limiti normali, borderline, riduzione generale della sensibilità, sensibilità anormalmente alta e entro i limiti normali.
Interpretazione
Stabilire un campo visivo di base affidabile è fondamentale nella gestione del glaucoma e nel monitoraggio futuro per una possibile progressione. I medici dovrebbero ottenere almeno due campi visivi di base riproducibili per rilevare piccoli incrementi di cambiamento. Riconoscere la progressione, in particolare dopo l’escalation della terapia nei momenti di progressione, richiederà al medico di stabilire una nuova linea di base.
Caso 3. Difetto di glaucoma paracentrale
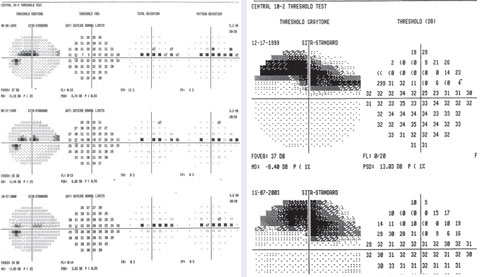
Un esempio di punti variabili nello scotoma paracentrale superiore su 24-2 con un difetto profondo focale su 10-2.
I campi visivi fatti prima dell’attuale trattamento medico o chirurgico, o durante un lungo periodo di perdita del follow up fuori dal trattamento, non dovrebbero essere usati allo scopo di determinare la progressione. I medici dovrebbero usare i nuovi campi visivi di base eseguiti dopo questi cambiamenti di trattamento e qualsiasi campo visivo successivo per giudicare la progressione.
Una linea di base affidabile e rappresentativa è importante anche per i programmi di analisi della progressione. I campi visivi tendono ad avere una maggiore variabilità con una localizzazione più eccentrica e sensibilità di medio livello, e la fluttuazione a lungo termine rende più difficile giudicare la progressione. I punti di sensibilità di livello medio tendono ad essere variabili, mentre i valori dei test negli intervalli di sensibilità superiori e inferiori sono più stabili. Stabilire un campo visivo di base affidabile e riproducibile può aiutare a rimuovere alcune di queste sfide.
Neuropatie ottiche non glaucomatose
I campi visivi possono aiutare a valutare le lesioni che influenzano il percorso visivo, stabilire linee di base e agire come strumenti di screening per alcuni farmaci associati a neuropatie ottiche. Possono anche monitorare la progressione o la ricorrenza delle malattie, aiutando a guidare le decisioni di trattamento e anche aiutare a localizzare le lesioni.5 La manifestazione più comune del campo visivo di una neuropatia ottica non glaucomatosa è un difetto centrale. Più grande è lo scotoma, maggiore è la probabilità che l’acuità visiva sia ridotta (Tabella 1).
Malattia retinica
I difetti del campo visivo causati dalla malattia retinica tendono ad avere bordi ben definiti e netti che appaiono più profondi della maggior parte dei difetti del glaucoma con meno variabilità.2 Le condizioni comuni che colpiscono l’area maculare, come la degenerazione maculare legata all’età e la corioretinopatia sierosa centrale, possono dare origine a scotomi centrali che possono essere visti sul 10-2 così come alcuni test 24-2 e 30-2, a seconda dell’estensione del danno.
La retinite pigmentosa dà luogo a difetti del campo visivo periferico, che possono portare alla visione a tunnel con solo un’isola centrale nella malattia avanzata.
Le occlusioni arteriose mostrano tipicamente aree assolute di difetto mentre le occlusioni venose possono essere più superficiali e diffuse.2 Queste spesso coesistono con il glaucoma, rendendo l’interpretazione più difficile.
La corioretinite, o le cicatrici associate, possono mascherare i difetti glaucomatosi con un difetto arcuato o cuneiforme. Un distacco di retina darà luogo a un difetto relativo mentre la retinoschisi avrà un difetto assoluto. Queste condizioni sono spesso molto più periferiche di quello che apparirebbe sul test centrale convenzionale usando 24-2 o 30-2.
Difetti del glaucoma
Un difetto può essere una depressione generalizzata o localizzata della sensibilità rispetto al database normalizzato. Le depressioni generalizzate si vedono più comunemente con la cataratta, ma possono anche derivare da un errore refrattivo non corretto o dalla miosi. I difetti localizzati possono essere ulteriormente descritti in base alle dimensioni, alla profondità e alla posizione per aiutare la diagnosi. Un difetto relativo si verifica quando la sensibilità è inferiore al normale, o può essere ridotta rispetto ad altre aree del campo, ma la visione rimane. Un difetto assoluto si ha quando lo stimolo viene presentato alla massima luminosità e non viene visto.
La perdita del campo visivo glaucomatoso può verificarsi prima nella regione nasale o in quella arcuata (area di Bjerrum). Questi difetti possono estendersi dal punto cieco, intorno alla regione maculare, finendo bruscamente al meridiano orizzontale nasale. I difetti glaucomatosi precoci sono spesso scotomi relativi localizzati (tabella 2).
La notevole variabilità test-retest è il segno distintivo delle aree del campo visivo colpite dalla perdita del campo visivo glaucomatoso. Riduzioni variabili della sensibilità che si verificano nella stessa area, ma non sempre nelle stesse posizioni dei punti di test, comunemente precedono i difetti di campo glaucomatosi coerenti.2 La variabilità, come si vede con i falsi negativi, può indicare affidabilità, ma quantità maggiori di variabilità sono spesso viste a causa della malattia stessa.
Tabella 2. Criteri per il difetto del campo visivo glaucomatoso con alta specificità e sensibilità13,14
- Cluster di tre o più punti non bordi sulla deviazione del modello con p
- GHT fuori dai limiti normali su due campi consecutivi
- PSD
- Asimmetria del MD >1.50dB che sia ripetibile e nel contesto di un sospetto clinico15,16
Quando i campi visivi non sono affidabili, dovrebbero essere ripetuti per stabilire dei valori di riferimento, confermare un difetto o confermare una progressione sospetta. Di solito, i campi visivi non vengono ripetuti lo stesso giorno a causa della stanchezza del paziente, che può influenzare l’affidabilità. Raramente è urgente ripetere il campo visivo immediatamente, poiché il glaucoma è generalmente una neuropatia ottica lentamente progressiva e le decisioni di trattamento sono guidate dal tasso di cambiamento.2 Ogni studio dovrebbe standardizzare una strategia e un modello di test preferito e ripetere lo stesso test per consentire confronti più accurati sui test di follow-up.10
Progressione
La valutazione del cambiamento consente al medico di determinare se la condizione è stabile, in progresso o in miglioramento. La progressione in un campo visivo può essere dovuta a una diminuzione diffusa della sensibilità, i difetti esistenti possono diventare più profondi o espandersi o possono sorgere nuovi difetti. Le aree depresse più comunemente progrediscono prima che vengano colpite nuove aree del campo visivo. Un aumento iniziale della variabilità del campo visivo è a volte visto prima che un cambiamento o una progressione diventi costante. È importante differenziare se le prove mostrano una fluttuazione a lungo termine o una tendenza al peggioramento. Una volta che i medici stabiliscono che il campo visivo è peggiorato, devono decidere se il cambiamento è dovuto al glaucoma o ad un’altra entità patologica. I cambiamenti statisticamente e clinicamente significativi del campo visivo permettono al medico di apportare le modifiche necessarie al piano di trattamento e gestione del paziente.
I medici devono anche valutare come il tasso di progressione possa alterare la qualità della vita del paziente.2 Per esempio, i medici devono essere più cauti nel trattare i pazienti più giovani con progressione più rapida e i pazienti monoculari (Tabella 3).
Sebbene sia difficile prevedere quali pazienti progrediranno lentamente o rapidamente, una volta valutato il tasso di progressione nel tempo, la gestione del paziente dovrebbe essere modificata di conseguenza. Il paziente più giovane che mostra segni di rapida progressione dei difetti del campo visivo, per esempio, avrà bisogno di un piano di gestione più aggressivo di un paziente anziano con una lenta progressione di un difetto di campo iniziale. È ragionevole che il trattamento e la gestione dei pazienti siano personalizzati in base al loro specifico quadro clinico, compresa la perdita di campo e il tasso di progressione. La ricerca dimostra che se il tasso di progressione è determinato e non viene iniziato alcun cambiamento di trattamento, i tassi di progressione passati possono essere predittivi dei tassi futuri.10,11 Allo stesso tempo, i tassi di declino possono essere modificati dall’intensificazione della terapia. Una volta effettuato un intervento, si dovrebbe stabilire una nuova linea di base.
Tabella 3. Suggerimenti per giudicare la progressione
- Tre punti in una regione anormale diminuiscono di 10dB*
- Due nuovi punti, vicino ad un difetto ridotto di 10dB*
OR
- Due punti nella regione centrale di 15 gradi o tre fuori di 15 gradi diminuiti di 10dB*
OR
- Confronti statistici (p
*Su due o più campi successivi14,17
La valutazione del cambiamento nel tempo è fondamentale nella gestione del glaucoma. Con il software di analisi della progressione guidata (GPA) che si trova su HFA, vengono identificati due test del campo visivo di base. I successivi test del campo visivo vengono poi confrontati con la media della linea di base utilizzando i valori di deviazione del modello. Quando i valori di follow-up diminuiscono in misura maggiore rispetto alla variabilità di una popolazione di pazienti affini per età e difetto di glaucoma stabile, il punto viene identificato. Se il cambiamento persiste su test ripetuti consecutivi, i punti sono contrassegnati come possibili (due consecutivi) o probabili (tre o più campi consecutivi).
GPA utilizza sia l’analisi delle tendenze che quella degli eventi per aiutare i medici a identificare e quantificare la progressione del campo visivo. L’analisi degli eventi cerca un cambiamento statisticamente significativo di un punto o di un gruppo di punti, mentre l’analisi delle tendenze quantifica la direzione del cambiamento nel tempo, o il tasso di cambiamento, comprese le proiezioni future. I medici possono rivolgere la loro attenzione alla potenziale sottostima della perdita diffusa, ai sottili artefatti che possono essere associati alla deviazione del pattern e alla necessità di un numero sufficiente di campi visivi di alta qualità (minimo cinque) per un’analisi ottimale. Tuttavia, la GPA è meno influenzata dalla cataratta rispetto ad altri strumenti di analisi. Ogni strategia di analisi utilizza il proprio database normativo.2 Un ulteriore obiettivo è quello di identificare un tasso di progressione e separare i pazienti che stanno progredendo rapidamente e necessitano di una terapia sempre più aggressiva.
Progressione delle neuropatie ottiche non glaucomatose
Poiché la GPA è stata istituita specificamente per la gestione del glaucoma, i medici devono adottare un approccio diverso quando valutano la possibile progressione in condizioni non glaucomatose. L’analisi di regressione del VFI o della deviazione media, così come il rapporto sulla panoramica delle serie, possono essere utili quando si valutano altre condizioni.2
Follow Up
Utilizzare la stessa strategia di test e lo stesso modello per consentire un confronto più facile e il monitoraggio della progressione. Seguire i pazienti con glaucoma accertato con la perimetria è essenziale per determinare se la gestione attuale è adeguata o se sono necessari cambiamenti nel trattamento in base alla stabilità o alla progressione del campo visivo.
La frequenza del follow-up dipenderà dall’estensione della malattia e dal decorso clinico. I pazienti che dimostrano stabilità potrebbero ragionevolmente aumentare l’intervallo di follow up.
Artificati
Ci sono diversi artefatti che possono sorgere, imponendo ulteriori sfide all’interpretazione dei campi visivi. I clinici devono discernere i veri difetti del campo visivo dalla patologia che sono correlati al quadro clinico rispetto agli artefatti che possono sorgere. A volte, quando non è chiaro se il difetto del campo visivo è reale o un artefatto, il campo visivo dovrebbe essere ripetuto in un tempo appropriato basato sul vostro livello di sospetto e sul quadro clinico. Gli artefatti a cui prestare attenzione includono:
– Ptosi palpebrale e sopraccigliare. Questo può causare un denso difetto superiore lungo i punti del bordo superiore. I pazienti con ptosi visivamente significativa possono trarre beneficio dall’avere le palpebre nastrate per il test.
– Artefatti del bordo. Il posizionamento del supporto della lente di prova può portare a un artefatto del bordo se è troppo lontano dall’occhio del paziente, creando uno scotoma anulare completo o parziale.
– Errore refrattivo errato. Questo può portare ad una depressione generalizzata della sensibilità che può imitare quella di una cataratta. Un errore di rifrazione elevato può creare un effetto di ingrandimento o di minimizzazione e richiede un corretto calcolo della distanza dei vertici. Usare il segno sbagliato del potere della lente o non usare il nuovo errore di rifrazione dopo che un paziente ha subito un intervento di cataratta sono due errori comuni.
– Affaticamento del paziente. Questo può manifestarsi con tempi di test più lunghi, un alto valore di falso negativo o preferibilmente una sensibilità periferica anormale. I punti periferici sono testati più tardi nel corso del test e possono essere notevolmente ridotti in caso di stanchezza o di calo dell’attenzione, risultando in un anello lobulare più scuro o in un modello a quadrifoglio sulla scala di grigi.
Esiste una curva di apprendimento sia per i pazienti che per coloro che amministrano il test. La consapevolezza di questi artefatti comunemente riscontrati permette di migliorare l’interpretazione del campo visivo e il riconoscimento dei limiti dell’affidabilità e della qualità dei risultati dei test.
Perché facciamo i test
La comprensione del percorso visivo può dare a un fornitore un’idea preziosa per localizzare le lesioni. Ogni studio dovrebbe standardizzare una strategia e un modello di test preferito e ripetere lo stesso test nelle visite di follow-up per consentire confronti più accurati nel corso dei test di follow-up.18
La gestione del glaucoma dovrebbe essere focalizzata sulla prevenzione della perdita dei campi visivi fino al punto di influenzare la qualità della vita del paziente. È importante valutare l’intero quadro clinico per assicurarsi che le variabili siano correlate e coincidenti. I test dovrebbero essere ripetuti se c’è incertezza per stabilire misure di base più affidabili e confermare la possibile progressione.
I dottori Draskovic e McSoley sono optometristi dello staff del Bascom Palmer Eye Institute.
1. Lens A, Langley T, Nemeth SC, Shea C. Percorso visivo. In: Anatomia e fisiologia oculare. Thorofare, NJ: SLACK; 1999:90-5.
2. Heijl A, Patella VM, Bengtsson B. The Field Analyzer Primer: Effective Perimetry. 4a ed. Carl Zeiss Meditec; 2012.
3. Park HY, Hwang BE, Shin HY, Park CK. Indizi clinici per prevedere la presenza di scotoma parafoveale sul campo visivo Humphrey 10-2 usando un campo visivo Humphrey 24-2. Am J Ophthalmol. 2016;161:150-9.
4. Ehrlich AC, Raza AS, Ritch R, et al. Modificare il modello convenzionale di prova del campo visivo per migliorare il rilevamento dei difetti glaucomatosi precoci nel 10° centrale. Transl Vis Sci Technol. 2014 Oct;3(6):6.
5. Kedar S, Ghate D, Corbett JJ. Campi visivi in neuro-oftalmologia. Giornale indiano di oftalmologia. 2011;59(2):103-9.
6. Muro M, George D. Ipertensione intracranica idiopatica. Uno studio prospettico di 50 pazienti. Cervello. 1991;114:155-80.
7. Keltner JL, Johnson CA, Spurr JO, Beck RW. Profilo di campo visivo basale di neurite ottica. L’esperienza della prova di trattamento di neurite ottica. Gruppo di studio della neurite ottica. Arch Ophthalmol. 1993;111:231-4.
8. Hayreh SS, Zimmerman B. Anomalie del campo visivo nella neuropatia ottica ischemica anteriore non arteritica: il loro modello e la prevalenza all’esame iniziale. Arch Ophthalmol. 2005;123:1554-62.
9. Hayreh SS. Neuropatia ottica ischemica posteriore: caratteristiche cliniche, patogenesi e gestione. Occhio (Lond). 2004;18:1188–206.
10. Bengtsson B. Previsione della perdita del campo visivo glaucomatoso per estrapolazione delle tendenze lineari. Arch Ophthalmol. 2009;127(12):1610-5.
11. Heijl A. Riduzione della pressione intraoculare e progressione del glaucoma. Arch Ophthalmol. 2002;120(10):1268-79.
12. Willmore LJ, Abelson MB, Ben-Menachem E, et al. Vigabatrin: 2008 aggiornamento. Epilepsia. 2009;50:163–73.
13. Katz J, Sommer A, Gaasterland DE, Anderson DR. Un confronto di algoritmi analitici per rilevare la perdita del campo visivo glaucomatoso. Arch Ophthalmol. 1991;109(12):1017-25.
14. Hodapp E, Parrish RK II, Anderson DR. Decisioni cliniche nel glaucoma. St. Louis: The CV Mosby Co;1993:52-61.
15. Feuer WJ, Anderson DR. Asimmetria della soglia statica nella perdita precoce del campo visivo glaucomatoso. Oftalmologia. 1989;96:1285-97.
16. Brenton RS, Phelps CD, Rojas P, Woolson RF. Differenze interoculari del campo visivo in soggetti normali. Invest Ophthalmol Vis Sci. 1986;27:799-805.
17. Anderson DR, Chauhan B, Johnson C, et al. Criteri per la progressione del glaucoma nella gestione clinica e negli studi di risultato. Am J Ophthalmol. 2000;130(6):827-29.
18. Weinreb RN. Progressione del glaucoma: The 8th Consensus Report of the World Glaucoma Association. Amsterdam: Kugler Publications; 2011.
.