Avaliar o caminho visual pode ser parte integrante do diagnóstico e gerenciamento de inúmeras condições.
Por Kristie Draskovic, OD, e John J. McSoley, OD
- Data de liberação:
- Data de expiração:
- Data de liberação:
- Faculdade/Câmara editorial:
- Crédito:
- Declaração de Patrocínio:
- Disclosure Statement:
- Caso 1. Macroadenoma Pituitário
- Tabela 1. Neuropatias ópticas comumente detectadas com testes de campo visual
- Caso 2. Esclerose Múltipla
- Caso 3. Defeito do Glaucoma Paracentral
- Tabela 2. Critérios para Defeito de Campo Visual Glaucomatoso com Alta Especificidade e Sensibilidade13,14
- Tabela 3. Sugestões para julgar a progressão
Data de liberação:
Março 2016
Data de expiração:
Março 1, 2019
Data de liberação:
Examinar os campos visuais usando perimetria automatizada pode ajudar os clínicos a avaliar lesões que afetam a via visual, estabelecer linhas de base e triagem para certas neuropatias ópticas induzidas por medicamentos. Também pode ajudar a monitorar a progressão ou recorrência de doenças, orientar decisões de tratamento e auxiliar na localização de lesões. Este artigo ajudará os clínicos a entender e interpretar melhor os campos visuais nos processos de doenças glaucomatosas e não glaucomatosas.
Faculdade/Câmara editorial:
Kristie Draskovic, OD, e John J. McSoley, OD
Crédito:
Este curso é aprovado pela COPE por 2 horas de crédito da CE. COPE ID é 48599-GL. Por favor, verifique o seu conselho estadual de licenciamento para ver se esta aprovação conta para a sua exigência CE para relicensure.
Declaração de Patrocínio:
Este curso de educação contínua é patrocinado em conjunto pelo Pennsylvania College of Optometry.
Disclosure Statement:
Drs. Draskovic e McSoley não têm relações financeiras para divulgar.
Examinar o campo visual é essencial ao considerar a potencial perda de visão das condições que afetam o caminho visual. A perimetria automatizada padrão é uma ferramenta útil para identificar e acompanhar muitas condições neurológicas, bem como suspeitos de glaucoma e glaucoma. Embora vários dispositivos estejam atualmente disponíveis, a discussão seguinte considerará o uso do Humphrey Field Analyzer (HFA, Zeiss) como um exemplo.
Anatomia e Fisiologia
A anatomia da via visual, os clínicos podem detectar áreas de preocupação com muitas condições que causam comprometimento visual (Figura 1). Como a luz que viaja do campo visual temporal cai sobre a retina nasal, as lesões da retina são vistas exatamente no quadrante oposto do campo visual. Todas as lesões pré-criasmais, incluindo as da retina e do nervo óptico, dão origem a defeitos isolados do olho afetado.1
Desde que as fibras nasais sejam responsáveis pelo campo visual temporal, uma lesão no quiasma óptico resultará em um defeito do campo visual que afeta o campo temporal de ambos os olhos, e dá origem à clássica hemianopsia bitemporal, que respeita a linha média vertical.1 As lesões do quiasma óptico podem ser resultado de adenomas pituitários, meningiomas supra-selares, craniofaringiomas ou aneurismas. Em alguns casos, defeitos do campo visual podem se reverter após o tratamento da causa.2
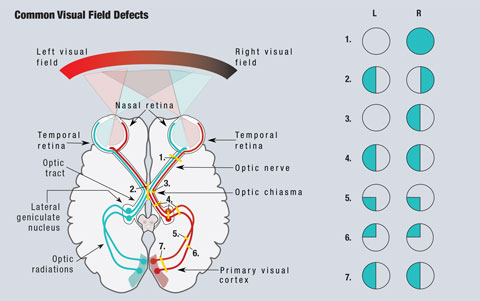
Clique na imagem para ampliá-la. Fig. 1. Um esquema simplificado do caminho visual é mostrado. Lesões que interrompem o caminho visual levam a defeitos no campo visual. (1) Uma lesão completa do nervo óptico direito resulta em perda completa do campo visual direito. (2) Uma lesão na linha média do quiasma óptico leva a uma hemianopsia bitemporal. (3) Uma lesão das fibras não cruzadas do nervo óptico direito no quiasma óptico leva a uma hemianopsia nasal do olho direito. (4) Uma lesão completa do trato óptico direito, núcleo geniculado lateral, ou radiações ópticas resulta em uma hemianopsia homônima esquerda completa. (5) Uma lesão das radiações ópticas superiores direitas resulta em uma quadranopsia inferior esquerda. (6) Uma lesão nas radiações ópticas inferiores direitas resulta em um quadranópsia superior esquerdo. (7) Uma lesão das radiações ópticas superior e inferior direita causa uma hemianopsia homônima esquerda. Ilustração de Miquel Perello Nieto.
Fibras responsáveis pelo campo visual à direita da linha média são encontradas no lado esquerdo do cérebro, e vice-versa. Como resultado desse cruzamento, todas as lesões pós-viasmáticas, incluindo lesões do trato óptico e radiações ópticas, causam uma hemianopsia homônima.1 Esses defeitos estão do mesmo lado do campo visual em cada olho e respeitam a linha média vertical. Quando os defeitos são vistos apenas superiores ou inferiores, é referida como quadranopsia. No caso de defeitos incompletos da hemianopsia, as lesões anteriores são geralmente mais incongruentes, enquanto as posteriores serão mais congruentes entre os dois olhos.1
Perda do campo visual glaucomatoso representa dano aos axônios que viajam ao longo da camada de fibra nervosa da retina e geralmente segue um padrão arcuate para o nervo óptico. Os danos a esses axônios darão origem a defeitos do campo visual localizado, mais comumente escotomas arcuate, passos nasais e escotomas paracentrais. Um campo de visão normal estende-se temporalmente até 90 graus, 70 graus tanto superior como inferior e 60 graus nasais e de fixação. A informação mais valiosa para déficits neurológicos e manejo do glaucoma é obtida dentro de 30 graus a partir da fixação.2
Estratégia de teste
Perimetria estática automatizada – e perimetria de limiar especificamente – apresenta um estímulo de tamanho fixo, mas de intensidade variável. A sensibilidade dos diferentes locais de teste é registrada com base nas respostas do paciente a esses estímulos. Um estímulo de tamanho III (que é de 4mm2 quando projetado em uma bacia de 30cm) é comumente usado na prática clínica.
Existem diferentes padrões de teste de limiar disponíveis. O teste padrão 30-2 testa 76 localizações dentro de 30 graus de fixação, enquanto o teste padrão 24-2 testa 54 localizações removendo para o anel de pontos a 30 graus (exceto os dois pontos que se sobrepõem ao meridiano horizontal nasal). Estes pontos mais periféricos são mais propensos à variabilidade, e 24-2 encurta o tempo de teste ao remover estes pontos periféricos do teste. O espaçamento entre as localizações dos pontos de teste é de seis graus.
Além disso, o padrão de teste 10-2 visa 64 pontos dentro de 10 graus da fixação separados por dois graus. Esta opção é preferível quando surgem defeitos centrais ou paracentrais com os 24-2 e 30-2 ou quando o campo fica tão apertado que os pontos periféricos não são clinicamente úteis. Os médicos também podem optar por aumentar o tamanho do estímulo para V, o que pode proporcionar valores de sensibilidade mais elevados e uma maior amplitude dinâmica através da qual se pode acompanhar os pacientes para mudança. Entretanto, atualmente não há nenhum algoritmo de teste tipo ATIE, nem há uma comparação disponível com uma base de dados normativa ou análise de progressão.
Caso 1. Macroadenoma PituitárioUm paciente apresentado para consulta no cenário de glaucoma atípico de tensão normal progressiva. |
|
|
|
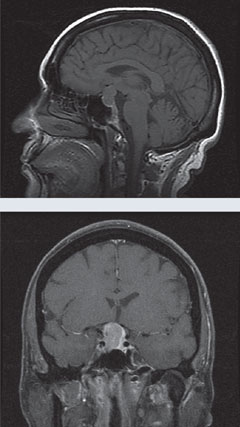
| Acima, o campo visual 24-2 do paciente demonstra perda de campo visual bitemporal. Na RM à esquerda, a visão sagital T1 sem gadolínio e a visão coronal T1 com gadolínio revelam uma grande massa de venda com ligeiro realce e efeito compressivo sobre o quiasma. Este achado é consistente com o macroadenoma pituitário. Click images to enlarge. |
|

|
|
| Após o paciente ter sido submetido à cirurgia trans-esfenoidal para remoção da massa vendedora, o campo visual, acima, mostra melhora do defeito do campo visual no olho direito e resolução do defeito no olho esquerdo. Clique na imagem para ampliá-la. | |
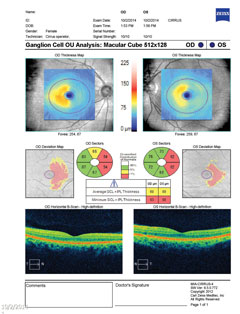
| Acima, o complexo celular ganglionar revela afinamento nasal em ambos os olhos, o que se correlaciona com a perda do campo visual temporal. Clique na imagem para ampliar. | |
Estudos recentes mostram que campos visuais 10-2 podem ser úteis para identificar mais do que glaucoma avançado.3,4 Um estudo revelou que alguns pacientes com glaucoma apresentavam defeitos centrais significativos nos padrões de teste 10-2, apesar do campo visual 30-2 central normal.4 O estudo sugere que, devido à fraca amostragem espacial, a deterioração do campo central glaucomatoso não pôde ser detectada apenas pela grade de teste 30-2, sendo necessária uma estimativa mais densa dos 10 graus centrais.4 Também sugere que a modificação do padrão convencional do teste de campo visual pode melhorar a detecção de defeitos glaucomatosos precoces nos 10 graus centrais.4
Na prática diária, os médicos freqüentemente realizam campos 10-2 quando pequenos escotomas centrais ou paracentrais aparecem nos testes 30-2 e 24-2, ou quando há suspeita ou ameaça de acuidade como resultado da perda do campo. Além disso, um padrão de teste 10-2 pode ser um adjunto útil quando há alta variabilidade inter-teste de pontos paracentrais num padrão 24-2. A crescente atenção à função das células ganglionares na região macular também pode aumentar a atenção à área do campo visual testado pelo padrão 10-2.
Reliabilidade
Indicações de confiabilidade do desempenho do campo visual incluem perdas de fixação e respostas tanto falso-positivas como falso-negativas.
Tabela 1. Neuropatias ópticas comumente detectadas com testes de campo visual |
|
| Hipertensão intracraniana idiopática | Early: enlarged blind spot Late: constrição generalizada5,6 (pode melhorar com o tratamento) |
| N neurite óptica | – Perda de campo visual difusa (em quase metade dos casos) – Outros: defeito altitudinal, escotomas centrais ou cecocentrais, arcuate ou duplo arcuate e defeitos hemianópicos5,7 |
| Neuropatia óptica isquêmica anterior não arterítica | – Defeitos altitudinais que respeitam a linha média horizontal são mais comuns – Outros: escotomas centrais, defeitos arqueados e quadranopsias5,8 |
| Neuropatia óptica isquêmica anterior | – Defeito de campo central5,9 |
| Neuropatias ópticas hereditárias – Neuropatia óptica hereditária de Leber – Atrofia óptica dominante |
– Perda do campo visual central e central5 |
| Nervo óptico de cabeça drusen | – Pode imitar um padrão glaucomatoso |
| Oftalmopatia tireóide | – Grande variabilidade – Pode resolver parcial ou totalmente após o tratamento2 |
| Neuropatia óptica tóxica induzida por medicação | – A toxicidade do etambutol (para tratamento da tuberculose) pode causar escotomas centrais e, menos comumente, constrição periférica e defeitos altitudinais5 – Vigabatrina (um medicamento anti-epiléptico), pode causar defeitos de campo que começam como defeitos nasais bilaterais e depois progridem para defeitos de campo concêntricos enquanto o campo central permanece intacto12 |
Fixação pode ser monitorada pela apresentação periódica de um estímulo ao ponto cego fisiológico (método de Heijl-Krakau) ou pelo monitoramento da posição do reflexo da luz corneana. Na AFA, a deflexão para cima indica mudança na posição ou fixação; a deflexão para baixo indica que o reflexo da luz corneana não pode ser localizado, como durante uma mudança na posição da cabeça ou das pálpebras.
Positivos falsos ocorrem quando um paciente responde em um momento em que não há estímulo associado ou quando uma resposta não é fisiologicamente possível. Pacientes com altos falsos positivos são muitas vezes descritos como “gatilho feliz”. Isto pode revelar um campo visual que parece mais sensível ou mais normal do que o esperado ou pode levar a valores de sensibilidade limiar anormalmente elevados.
Negativos falsos ocorrem quando um paciente não responde a um estímulo mais brilhante do que um já visto ou quando a resposta não é consistente com o padrão de respostas naquela região. O valor falso negativo pode ser uma indicação de confiabilidade ou um reflexo do processo da doença. Regiões anormais do campo visual estão associadas a maior variabilidade intra-teste e inter-teste. Como resultado, regiões do campo visual com baixa sensibilidade não são incluídas no cálculo do valor falso negativo.
O limiar de sensibilidade são dados brutos com valores registrados em decibéis. Os números indicam o grau de atenuação a partir do estímulo máximo possível. Valores de
O desvio total representa o desvio dos valores esperados com base na base de dados normal correspondente à idade. O desvio padrão corrige a sensibilidade global do campo através da remoção de depressões generalizadas (por exemplo, de cataratas) para identificar quaisquer áreas de anormalidades localizadas. Tanto o desvio total como o desvio padrão têm associados valores de probabilidade (p) calculados com base na distribuição dentro de uma população normal. O intervalo de valores normais é mais amplo perifericamente do que centralmente. Os símbolos P indicam a frequência do valor testado que ocorre em uma população normal de acordo com a idade. Os desvios são mostrados no mapa se o limiar testado for pior que os 5% inferiores do normal para aquela idade.2 Por exemplo, se p
Caso 2. Esclerose MúltiplaUm paciente com diagnóstico de esclerose múltipla (EM) apresentou perda de visão. |
|
|
 |
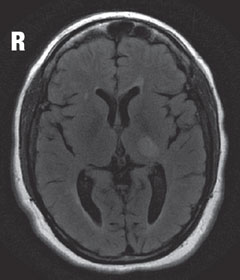
| Acima, na RM, a visão axial em T2 revela uma lesão focal hiperintensa logo após o núcleo geniculado lateral esquerdo no tálamo, que é responsável pelo defeito do campo visual visto. A lesão vista, assim como outras múltiplas lesões hiperintensas, são características típicas da doença demielinativa como a EM. | |
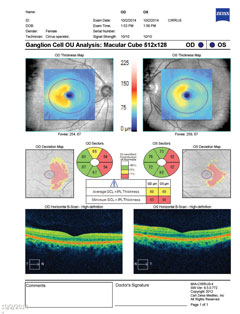 |
|
| Acima, o campo visual demonstra uma hemianopia homônima direita incompleta. Clique na imagem para ampliar. A esquerda, a análise das células ganglionares revela afinamento nasal no olho direito e afinamento temporal no olho esquerdo, o que é consistente com os achados do campo visual. Clique na imagem para ampliar. |
|
Desvio padrão padrão padrão padrão (PSD) é um desvio padrão ponderado em relação ao valor esperado com base nos valores normais correspondentes à idade e no índice de desvio médio (MD). O PSD revela a distância entre diferentes pontos dentro do campo. O PSD é sensível tanto para defeitos de glaucoma precoce como para defeitos de glaucoma focal. Um baixo valor PSD pode ser visto com campos visuais normais, um campo visual que está uniformemente deprimido ou um campo completamente cego. Um valor de p associado é a probabilidade de ocorrência do valor.
O MD é uma média ponderada de valores no gráfico numérico de desvio total. O MD pode ser influenciado por uma diminuição difusa na sensibilidade geral ou por um defeito localizado. Um MD de 0 indica um valor normal, enquanto um valor negativo representa um desvio ou perda em relação à base de dados normal. O desvio médio pesa mais os pontos centrais.
Índice de campo visual (VFI) é outra avaliação com correção de idade, expressa como porcentagem, onde perimetricamente normal é 100% e perimetricamente cego é 0%. Ao calcular a VFI, os pontos centrais são mais fortes do que os pontos periféricos. Ele fornece uma pontuação para um campo visual individual e é usado na análise de progressão.2
O teste de hemifield do glaucoma (GHT) compara a sensibilidade relativa dos valores de desvio padrão de cinco zonas nos campos superiores e inferiores. Cada uma destas zonas é comparada com sua zona espelho na hemifield oposta, e ambas as zonas são comparadas com a base de dados normativa. A GHT pode detectar a perda do campo visual glaucomatoso com alta sensibilidade e alta especificidade através de cinco categorias possíveis: fora dos limites normais, fronteira, redução geral da sensibilidade, sensibilidade anormalmente alta e dentro dos limites normais.
Interpretação
Estabelecer um campo visual de base fiável é crucial na gestão do glaucoma e na monitorização futura para uma possível progressão. Os médicos devem obter pelo menos dois campos visuais de linha de base reprodutíveis para detectar incrementos menores de mudança. O reconhecimento da progressão, particularmente após a escalada da terapia em momentos de progressão, exigirá que o clínico estabeleça uma nova linha de base.
Caso 3. Defeito do Glaucoma Paracentral
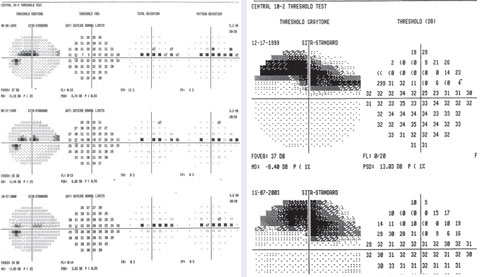
Um exemplo de pontos variáveis no escotoma paracentral superior em 24-2 com um defeito profundo focal em 10-2.
Campos visuais feitos antes do tratamento médico ou cirúrgico atual, ou durante um período prolongado de perda para acompanhamento do tratamento, não devem ser utilizados para determinar a progressão. Os médicos devem utilizar os novos campos visuais de base realizados após estas alterações de tratamento, e qualquer campo visual posterior no julgamento da progressão.
Uma linha de base confiável e representativa também é importante para os programas de análise da progressão. Os campos visuais tendem a ter maior variabilidade com localização mais excêntrica e sensibilidades de médio alcance, e a flutuação a longo prazo torna o julgamento da progressão mais desafiador. Os pontos de sensibilidade de nível médio tendem a ser variáveis, enquanto os valores de teste nas faixas de sensibilidade superior e inferior são mais estáveis. O estabelecimento de um campo visual de base confiável e reprodutível pode ajudar a remover alguns desses desafios.
Neuropatias ópticas não-glaucomatosas
Campos visuais podem ajudar a avaliar lesões que afetam o caminho visual, estabelecer linhas de base e agir como ferramentas de triagem para certas drogas associadas às neuropatias ópticas. Eles também podem monitorar a progressão ou recorrência de doenças enquanto ajudam a orientar as decisões de tratamento e até mesmo ajudar na localização de lesões.5 A manifestação mais comum do campo visual de uma neuropatia óptica não glaucomatosa é um defeito central. Quanto maior o escotoma, maior a probabilidade da acuidade visual ser reduzida (Tabela 1).
Doença Retinal
Defeitos de campo visual causados pela doença da retina tendem a ter bordas bem definidas e agudas que parecem mais profundas do que a maioria dos defeitos de glaucoma com menor variabilidade.2 Condições comuns que afetam a área macular, tais como degeneração macular relacionada à idade e corioretinopatia serosa central, podem dar origem a escotomas centrais que podem ser vistos em 10-2, bem como alguns testes 24-2 e 30-2, dependendo da extensão do dano.
Retinite pigmentosa dá origem a defeitos do campo visual periférico, que podem levar à visão em túnel com apenas uma ilha central em doença avançada.
Oclusões arteriais tipicamente mostram áreas de defeito absolutas, enquanto as oclusões venosas podem ser mais superficiais e difusas.2 Elas freqüentemente coexistem com o glaucoma, tornando a interpretação mais desafiadora.
Corioretinite, ou cicatrizes associadas, podem mascarar defeitos glaucomatosos com um defeito arqueado ou em forma de cunha. Um descolamento da retina dará origem a um defeito relativo enquanto que a retinosquite terá um defeito absoluto. Estas condições são frequentemente muito mais periféricas do que o que apareceria nos testes centrais convencionais usando 24-2 ou 30-2.
Defeitos de glaucoma
Um defeito pode ser uma depressão de sensibilidade generalizada ou localizada em comparação com a base de dados normalizada. As depressões gerais são mais comumente vistas com cataratas, mas também podem surgir de erro refrativo não corrigido ou miose. Os defeitos localizados podem ser descritos mais detalhadamente por tamanho, profundidade e localização para ajudar no diagnóstico. Um defeito relativo ocorre quando a sensibilidade é menor que o normal, ou pode ser reduzido em relação a outras áreas do campo, mas a visão permanece. Um defeito absoluto é quando o estímulo é apresentado no brilho máximo e não é visto.
Perda do campo visual glaucomatoso pode ocorrer primeiro na região nasal ou na região arcada (área de Bjerrum). Estes defeitos podem se estender do ponto cego, ao redor da região macular, terminando abruptamente no meridiano horizontal nasal. Os defeitos glaucomatosos precoces são frequentemente escotomas relativos localizados (Tabela 2).
Considerável variabilidade test-retest é a marca registrada das áreas do campo visual afetadas pela perda do campo visual glaucomatoso. As reduções de sensibilidade variável que ocorrem na mesma área, mas nem sempre nos mesmos pontos de teste, geralmente precedem defeitos consistentes do campo glaucomatoso.2 A variabilidade, como é vista com falsos negativos, pode indicar confiabilidade, mas quantidades maiores de variabilidade são frequentemente vistas devido à própria doença.
Tabela 2. Critérios para Defeito de Campo Visual Glaucomatoso com Alta Especificidade e Sensibilidade13,14
- Cluster de três ou mais pontos sem bordas no desvio padrão com p
- GHT fora dos limites normais em dois campos consecutivos
- PSD
- Assimetria do MD >1.50dB que é repetível e no cenário de suspeita clínica15,16
Quando os campos visuais não são confiáveis, eles devem ser repetidos para estabelecer linhas de base, confirmar um defeito ou confirmar a suspeita de progressão. Normalmente, os campos visuais não são repetidos no mesmo dia devido à fadiga do paciente, o que pode afetar a confiabilidade. Raramente é urgente ter o campo visual repetido imediatamente, pois o glaucoma é geralmente uma neuropatia óptica lentamente progressiva, e as decisões de tratamento são impulsionadas pela taxa de mudança.2 Cada prática deve padronizar uma estratégia e padrão de teste preferido e repetir o mesmo teste para permitir comparações mais precisas nos testes de acompanhamento.10
Progressão
Avaliar a mudança permite ao profissional determinar se a condição é estável, progredindo ou melhorando. A progressão em um campo visual pode ser devida a uma diminuição difusa na sensibilidade, defeitos existentes podem se aprofundar ou se expandir ou novos defeitos podem surgir. As áreas deprimidas progridem mais comumente antes que novas áreas do campo visual sejam afetadas. Um aumento inicial na variabilidade do campo visual é às vezes visto antes que uma mudança ou progressão se torne constante. É importante diferenciar se as evidências mostram uma flutuação a longo prazo ou uma tendência de agravamento. Uma vez que os médicos estabelecem que o campo visual está pior, eles devem decidir se a mudança é devida ao glaucoma ou a outra entidade da doença. Alterações estatisticamente e clinicamente significativas no campo visual permitem ao médico fazer as mudanças necessárias no tratamento e plano de manejo do paciente.
Os médicos também devem avaliar como a taxa de progressão pode alterar a qualidade de vida do paciente.2 Por exemplo, os médicos devem ser mais cautelosos no tratamento de pacientes mais jovens com progressão mais rápida e de pacientes monoculares (Tabela 3).
Embora seja difícil prever quais pacientes irão progredir lentamente vs. rapidamente, uma vez que uma taxa de progressão é avaliada ao longo do tempo, o manejo do paciente deve ser alterado de acordo. O paciente mais jovem que mostra sinais de progressão rápida de defeitos de campo visual, por exemplo, precisará de um plano de manejo mais agressivo do que um paciente idoso com progressão lenta de um defeito de campo precoce. É razoável que o tratamento e a gestão dos pacientes sejam personalizados com base no seu quadro clínico específico, incluindo a sua perda de campo e taxa de progressão. Pesquisas mostram que se a taxa de progressão for determinada e nenhuma mudança de tratamento for iniciada, as taxas de progressão passadas podem ser preditivas de taxas futuras.10,11 Ao mesmo tempo, as taxas de declínio podem ser alteradas pela escalada da terapia. Uma vez feita uma intervenção, uma nova linha de base deve ser estabelecida.
Tabela 3. Sugestões para julgar a progressão
- Três pontos em uma região anormal diminuem em 10dB*
- Dois novos pontos, perto de um defeito reduzido em 10dB*
OR
- Dois pontos no centro 15 graus ou três fora de 15 graus para baixo em 10dB*
OR
- Comparações estatísticas (p
*Em dois ou mais campos consecutivos14,17
Avaliar a mudança ao longo do tempo é crítico na gestão do glaucoma. Com o software de análise de progressão guiada (GPA) encontrado no HFA, dois testes de campo visual de linha de base são identificados. Os testes de campo visual subseqüentes são então comparados com a linha de base média usando os valores de desvio padrão. Quando os valores de seguimento diminuem a um grau maior do que a variabilidade de uma população de pacientes estáveis com glaucoma, o ponto é identificado. Se a alteração persistir em testes repetidos consecutivos, os pontos são marcados como possíveis (dois consecutivos) ou prováveis (três ou mais campos consecutivos).
GPA utiliza tanto a análise de tendências como a análise de eventos para auxiliar os profissionais na identificação e quantificação da progressão do campo visual. A análise de eventos procura uma mudança estatisticamente significativa de um ponto ou grupo de pontos, enquanto a análise de tendências quantifica a direção da mudança ao longo do tempo, ou a taxa de mudança, incluindo projeções futuras. Os clínicos podem direcionar sua atenção para a subestimação potencial da perda difusa, artefatos sutis que podem estar associados ao desvio padrão e a necessidade de um número suficiente de campos visuais de alta qualidade (mínimo de cinco) para uma análise ótima. Entretanto, o GPA é menos influenciado pela catarata do que outras ferramentas de análise. Cada estratégia de teste usa seu próprio banco de dados normativo.2 Um objetivo adicional é identificar uma taxa de progressão e separar os pacientes que estão progredindo rapidamente e precisam de terapia cada vez mais agressiva.
Progressão das Neuropatias Ópticas Não-Glaucomatosas
Porque a GPA foi estabelecida especificamente para o manejo do glaucoma, os clínicos devem adotar uma abordagem diferente ao avaliar a possível progressão em condições não-glaucomatosas. A análise de regressão da IFV ou desvio médio, bem como o relatório geral de série, podem ser úteis ao avaliar outras condições.2
Follow Up
Utilizar a mesma estratégia e padrão de teste para permitir uma comparação e monitoramento mais fáceis para a progressão. Seguir os pacientes de glaucoma estabelecidos com perimetria é essencial para determinar se o manejo atual é adequado ou se são necessárias mudanças no tratamento com base na estabilidade ou progressão do campo visual.
A frequência do seguimento dependerá da extensão da doença e do curso clínico. Os pacientes que demonstram estabilidade podem aumentar razoavelmente o seu intervalo de seguimento.
Artificações
Existem vários artefatos que podem surgir, impondo novos desafios à interpretação dos campos visuais. Os clínicos devem distinguir os verdadeiros defeitos do campo visual da patologia que se correlacionam com o quadro clínico vs. os artefatos que podem surgir. Em momentos em que não está claro se o defeito do campo visual é real ou um artefato, o campo visual deve ser repetido em uma linha de tempo apropriada com base em seu nível de suspeita e no quadro clínico. Os artefatos a serem observados incluem:
– Pálpebra e testa da sobrancelha. Isto pode causar um defeito denso superior ao longo dos pontos superiores da borda. Pacientes com ptose visualmente significativa podem se beneficiar de ter suas pálpebras coladas para testes.
– Artefactos da borda. O posicionamento do suporte da lente experimental pode levar a um artefato de aro se este estiver muito longe do olho do paciente, criando um escotoma total ou parcial do anel.
– Erro de refracção incorrecto. Isto pode levar a uma depressão generalizada na sensibilidade que pode imitar a de uma catarata. O erro refractivo elevado pode criar um efeito de ampliação ou minificação e exigir cálculos apropriados da distância do vértice. Usar o sinal de potência errado da lente ou não usar o novo erro refractivo depois de um paciente ter sido operado à catarata são dois erros comuns.
– Fadiga do paciente. Isto pode manifestar-se com tempos de teste mais longos, alto valor falso negativo ou, preferencialmente, sensibilidade periférica anormal. Os pontos periféricos são testados mais tarde no decorrer do teste e podem ser acentuadamente reduzidos em casos de fadiga ou diminuição da atenção, resultando em um padrão mais escuro, anel lobular ou trevo na escala de cinza.
– Existe uma curva de aprendizagem tanto para os pacientes quanto para aqueles que administram o teste. O conhecimento destes artefatos comumente encontrados permite uma melhor interpretação do campo visual e reconhecimento das limitações da confiabilidade e qualidade dos resultados dos testes.
Por que Testamos
O entendimento do caminho visual pode dar a um provedor uma visão valiosa da localização das lesões. Cada prática deve padronizar uma estratégia e padrão de teste preferido e repetir o mesmo teste nas visitas de acompanhamento para permitir comparações mais precisas ao longo do teste de acompanhamento.18
O manejo do glaucoma deve ser focado na prevenção da perda de campos visuais na medida em que afeta a qualidade de vida de um paciente. É importante avaliar todo o quadro clínico para garantir que as variáveis se correlacionem e coincidam. Os testes devem ser repetidos se houver incerteza para estabelecer medidas de base mais confiáveis e confirmar a possível progressão.
Drs. Draskovic e McSoley são optometristas da equipe do Bascom Palmer Eye Institute.
1. Lente A, Langley T, Nemeth SC, Shea C. Caminho Visual. In: Anatomia Ocular e Fisiologia. Thorofare, NJ: SLACK; 1999:90-5.
3. Park HY, Hwang BE, Shin HY, Park CK. Pistas clínicas para prever a presença de escotoma parafoveal no campo visual Humphrey 10-2 usando um campo visual Humphrey 24-2. Am J Ophthalmol. 2016;161:150-9.
4. Ehrlich AC, Raza AS, Ritch R, et al. Modificando o padrão de teste de campo visual convencional para melhorar a detecção de defeitos glaucomatosos precoces nos 10° centrais. Transl Vis Sci Technol. 2014 Out;3(6):6.
5. Kedar S, Ghate D, Corbett JJ. Campos Visuais em Neuro-Oftalmologia. Jornal Indiano de Oftalmologia. 2011;59(2):103–9.
6. Wall M, George D. Hipertensão intracraniana idiopática. Um estudo prospectivo de 50 pacientes. Cérebro. 1991;114:155-80.
7. Keltner JL, Johnson CA, Spurr JO, Beck RW. Baseline visual field profile of optic neuritis. A experiência do ensaio do tratamento da neurite óptica. Grupo de Estudo da Neurite Óptica. Arco Ophthalmol. 1993;111:231-4.
8. Hayreh SS, Zimmerman B. Visual field abnormalities in nonarteritic anterior ischemic anterior ischemic neuropathy: their pattern and prevalence at initial examination. Arco Ophthalmol. 2005;123:1554–62.
9. Hayreh SS. Neuropatia óptica isquêmica posterior: características clínicas, patogênese e manejo. Olho (Lond). 2004;18:1188–206.
10. Bengtsson B. Predição da perda do campo visual glaucomatoso através da extrapolação de tendências lineares. Arco Ophthalmol. 2009;127(12):1610-5.
11. Heijl A. Redução da pressão intra-ocular e progressão do glaucoma. Arco Oftalmol. 2002;120(10):1268-79.
12. Willmore LJ, Abelson MB, Ben-Menachem E, et al. Vigabatrin: 2008 update. Epilepsia. 2009;50:163–73.
13. Katz J, Sommer A, Gaasterland DE, Anderson DR. Uma comparação de algoritmos analíticos para a detecção de perda de campo visual glaucomatoso. Arco Ophthalmol. 1991;109(12):1017-25.
14. Hodapp E, Parrish RK II, Anderson DR. Decisões clínicas no glaucoma. St. Louis: The CV Mosby Co;1993:52-61.
15. Feuer WJ, Anderson DR. Assimetria do limiar estático na perda precoce do campo visual glaucomatoso. Oftalmologia. 1989;96:1285-97.
16. Brenton RS, Phelps CD, Rojas P, Woolson RF. Diferenças interoculares do campo visual em indivíduos normais. Invest Ophthalmol Vis Sci. 1986;27:799-805.
17. Anderson DR, Chauhan B, Johnson C, et al. Criteria for progression of glaucoma in clinical management and in outcome studies. Am J Ophthalmol. 2000;130(6):827-29.
18. Weinreb RN. Progressão do Glaucoma: O 8º Relatório de Consenso da Associação Mundial de Glaucoma. Amsterdam: Publicações Kugler; 2011.
