視覚経路を評価することは、多くの疾患の診断と管理に不可欠です
By Kristie Draskovic, OD, and John J. McSoley, OD
発表日:
2016年3月
有効期限:
2019年3月1日
目標声明:
自動視野計を用いて視野を調べることは、臨床家が視神経に影響を与える病変の評価、ベースラインの確立、特定の薬剤による視神経障害のスクリーニングに役立つ。 また、疾患の進行や再発のモニタリング、治療方針の決定、病巣の位置確認にも役立ちます。 この記事は、臨床医が緑内障および非緑内障の疾患過程における視野をよりよく理解し、解釈するのに役立ちます。
講師/編集委員会:
Kristie Draskovic, OD, and John J. McSoley, OD
クレジット表記:
This course is approved for 2 hours of CE credit. COPE IDは48599-GLです。
ジョイント・スポンサーのステートメント:
この継続教育コースは、ペンシルバニア・カレッジ・オブ・オプトメトリーによってジョイント・スポンサリングされています。
Disclosure Statement:
Drs. Draskovic and McSoley has no financial relationships to disclose.
Examining the visual field is essential when considering potential vision loss from conditions affecting the visual pathway.視野の検査は、視神経系に影響を与える条件からくる潜在的な視力低下を考慮する際に不可欠です。 標準的な自動視野測定は,緑内障や緑内障の疑いだけでなく,多くの神経学的な状態を特定し,追跡するのに有用なツールである。 現在、いくつかの装置が利用可能であるが、以下の議論では、例としてハンフリーフィールドアナライザー(HFA、Zeiss)の使用について検討する。
解剖学と生理学
視覚経路の解剖学により、臨床医は視覚障害を引き起こす多くの症状で懸念される領域を検出することができます(図1)。 側頭視野から進行する光は鼻側網膜に当たるため、網膜病変は視野の正反対の象限で観察される。 網膜や視神経の病変を含むすべての視神経前病変は、患眼に孤立した欠損を生じます1。
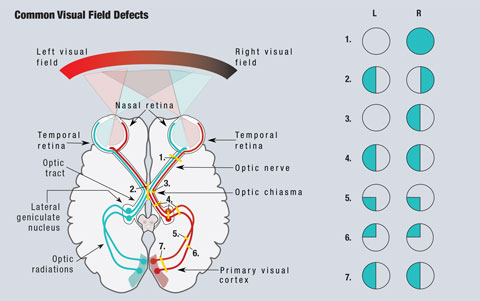
画像をクリックすると拡大表示されます。 図1. 視覚経路の簡略化した模式図を示す。 視覚経路を遮断する病変は視野欠損を引き起こす。 (1)右視神経の完全な病変では、右視野が完全に失われる。 (視交叉の正中線に病変があると、両側性半盲症になる。 (視交叉で右視神経の非交叉線維に病変があると、右目の鼻側半盲症になる。 (右視神経路、外側被蓋核、視神経放射の完全な病変により、左同名半盲症が生じる。 (右上肢視神経放射の病変により、左下肢四頭筋の失認が生じる。 (右下視神経輻射の病変により、左上四頭筋を生じる。 (7) 右視神経放射の上・下両方に病変があると、左同名半盲症になる。 イラスト:Miquel Perello Nieto
正中線より右側の視野を担当する線維は、脳の左側にあり、その逆もまた然り。 この交差の結果、視神経路や視神経放射の病変を含むすべての視神経後障害は、同名半盲症を引き起こす1。これらの障害は、両目の視野の同じ側で、垂直な正中線を基準にしている。 また、上方または下方にのみ欠損が認められる場合は、四半球症と呼ばれる。 不完全半盲症では、通常、前方の病変はより不一致であり、後方の病変は両眼でより一致する。1
緑内障性視野欠損は、網膜神経線維層に沿って走行する軸索への損傷を示し、通常は視神経に弧状パターンを描く。 軸索の損傷は局所的な視野欠損を引き起こし、最も一般的には弧状暗点、鼻状暗点、傍中心暗点である。 正常な視野は、時間的に最も遠いところで90度、上下に70度、鼻側に60度、固視から伸びています。 2
検査方法
自動静的視野測定-特に閾値視野測定-では、大きさは一定だが強さが変化する刺激を与える。 異なる検査位置の感度は、これらの刺激に対する患者の反応に基づいて記録される。 サイズIIIの刺激(30cmのボウルに投影すると4mm2)が臨床でよく使用されている
利用できる閾値テストのパターンはさまざまである。 30-2テストパターンは固定点から30度以内の76ヶ所をテストし、24-2テストパターンは30度の点の輪を除いた54ヶ所(水平経線を鼻側にまたぐ2点を除く)をテストする。 この最周辺の点は変動しやすいので、24-2ではこれらの周辺点をテストから除外することでテスト時間を短縮しています。 テストポイント位置の間隔は6度です。
また、10-2テストパターンは、固視から10度以内の64点を2度間隔でターゲットとする。 このオプションは、24-2および30-2で中心または副中心の欠陥が生じた場合、または視野が狭窄して周辺点が臨床的に有用でない場合に望ましい。 臨床医はまた、刺激サイズをVに拡大することを選択することができ、これにより、より高い感度値と、患者の変化を追跡するためのより大きなダイナミックレンジを得ることができるかもしれない。 しかし、現在のところ、SITAタイプの検査アルゴリズムはなく、また、標準的なデータベースとの比較や進行の分析もありません。 下垂体性巨細胞腫 非定型で進行性の正常眼圧緑内障の患者が受診した。
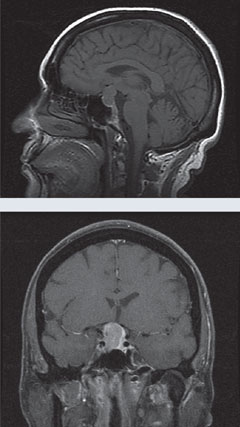

左のMRIでは、ガドリニウムなしのT1矢状面とガドリニウムありのT1冠状面で、わずかな増強と視交叉への圧迫効果を伴う大きな鞍部腫瘤が確認された。 この所見は下垂体巨大腺腫と一致する。
画像をクリックすると拡大します。

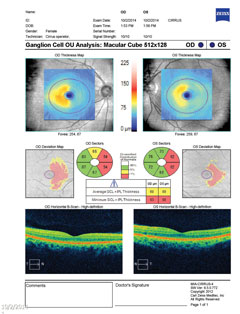
最近の研究では、10-2視野は進行した緑内障以上の識別に有用であることが示されています3,4。ある研究では、一部の緑内障患者は中央の30-2視野が正常であるにもかかわらず、10-2テストパターンで見られる著しい中央群欠損を有することが明らかになりました4。 この研究は、空間サンプリングが不十分なため、緑内障の中心視野の悪化は30-2テストグリッドだけでは拾いきれず、中心10度をより高精度に推定する必要があることを示唆しています4。 また、従来の視野検査パターンを修正することで、中心10度の緑内障性欠損の早期発見が向上する可能性が示唆された4
日常診療では、30-2や24-2検査で小さな中心または傍中心性のスコトーマが出現したり、視野欠損による視力低下の疑いや恐れがあると、10-2視野検査を行うことが多いようです。 また、24-2パターンにおいて傍中心点の検査間変動が大きい場合にも、10-2テストパターンは有用な補助手段となり得る。 黄斑部における神経節細胞機能への注目が高まるにつれ、10-2パターンで検査される視野の領域にも注目が集まるかもしれない。
表1. 視野検査でよく検出される視神経症 |
|
| 特発性頭蓋内圧亢進症 | 初期:盲点拡大 後期:盲点拡大 。 全身性狭窄5,6 (治療により改善することがある) |
| 0視神経炎 | -びまん性視野欠損(ほぼ半数にみられる) -その他。 高度障害、中心性または中間性スコトーマ、弧状または二重弧状障害、半盲症5,7 |
| Non-arteritic anterior ischemic optic neuropathy | – 水平正中を基準にする高度障害が最も多い – その他。 中心性スコトーマ、弧状欠損、四角視野5,8 |
| 後虚血性視神経症 | – 中心視野欠損5,9 |
| 遺伝性視神経症 -レーバー遺伝性視神経症 -優性視神経萎縮 |
– 頭部および中心部の視野欠損5 |
| 視神経頭部鼓膜 | -。 |
| 甲状腺眼症 | – 大きな変動 – 治療後に一部または完全に消失することがある2 |
| 薬剤性中毒性視神経症 | – エタンブトール(結核の治療用)中毒は中心性暗黒腫と、それを引き起こすことがある。 末梢の狭窄や高度障害5 – ビガバトリン(抗てんかん薬)。 は、両側の鼻の欠損から始まり、後に中心視野は無傷のまま同心円状の視野欠損に進行する視野欠損を引き起こすことがある12 |
固定は、生理的盲点に定期的に刺激を与えること(Heijl-Krakau法)や角膜光反射の位置をモニターすることにより観察することが可能である。 HFAでは、上方への偏位は位置の変化または固視を示し、下方への偏位は頭やまぶたの位置が変化したときなど、角膜光反射の位置がわからないことを示す。
偽陽性は、関連する刺激がないときに患者が反応したとき、あるいは生理的に反応が不可能なときに起こる。 偽陽性が高い患者は、しばしば “トリガーハッピー “と表現される。 これにより、予想以上に高感度または正常と思われる視野が明らかになったり、異常に高い閾値感度値になったりすることがある。
偽陰性は、患者がすでに見た刺激よりも明るい刺激に反応しないとき、または反応がその領域の反応のパターンと一致しないときに起こる。 偽陰性値は信頼性の指標となる場合もあれば、疾患過程を反映する場合もある。 視野の異常な領域は、検査内変動や検査間変動が大きくなることと関連している。 その結果、感度の低い視野の領域は偽陰性値の算出に含まれない。
閾値感度は、デシベルで記録された値の生データである。 数値は最大可能刺激からの減衰の度合いを示す。 1150>
総偏差値は、年齢をマッチさせた正常データベースに基づく期待値からの偏差を表します。 パターン偏差は、局所的な異常の領域を識別するために、白内障などによる全体的な落ち込みを除去することによって、視野の全体的な感度を補正したものである。 トータル偏差、パターン偏差ともに、正常集団内の分布に基づいて計算された確率(p)値が関連付けられている。 正常値の範囲は、中心部よりも周辺部で広くなっています。 P記号は、年齢をマッチさせた正常集団における検査値の発生頻度を示す。 例えば、p<1150><6952><8708><6889><8929><5942>の場合、その年齢における正常値の下位5%より悪いと、地図上に偏差が表示される2。 多発性硬化症 多発性硬化症(MS)と診断された患者が視力低下を呈した。
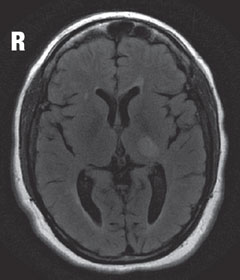

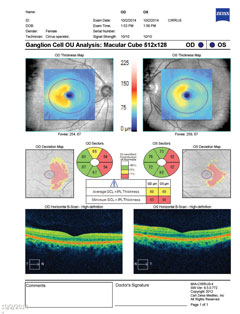
左は神経節細胞解析で、右目は鼻側菲薄化、左目は側頭菲薄化を認め、視野所見と一致する。
パターン標準偏差(PSD)とは、年齢を合わせた正常値と平均偏差(MD)指数に基づいて予想される値から重み付けした標準偏差のことです。 PSDは、フィールド内の異なる点間の距離を明らかにする。 PSDは、緑内障の初期および局所的な欠陥に対して感度が高い。 PSDの値が低いと、正常な視野、一様に落ち込んだ視野、完全な盲点の視野が見られることがあります。 p値はその値が発生する可能性を示す。
MDは総偏差数プロットにおける値の加重平均である。 MDは、全体的な感受性の拡散的な低下または局所的な欠陥によって影響を受ける可能性がある。 MDが0であれば正常値であり、負の値であれば正常なデータベースからの逸脱または損失を示します。 平均偏差は、中心点の重みをより大きくする。
視野指数(VFI)は年齢補正された別の評価で、パーセンテージで表され、視野正常が100%、視野欠損が0%となる。 VFIを計算する際、中心点の方が周辺点よりも強く加重されます。 緑内障半盲検(GHT)は、上半球と下半球の5つのゾーンのパターン偏差値の相対的な感度を比較するもので、個々の視野のスコアが得られ、進行解析に用いられる。 GHTは、上半球と下半球の5つのゾーンのパターン偏差値を比較し、それぞれのゾーンを反対側の半球のミラーゾーンと比較し、さらに両ゾーンを標準データベースと比較するものです。 GHTは、正常範囲外、境界線、全般的な感度低下、異常な高感度、正常範囲内の5つの可能なカテゴリーを通して、緑内障性視野欠損を高い感度と高い特異度で検出することができる。
解釈
信頼できるベースライン視野を確立することは、緑内障管理および将来の進行の可能性を監視する上で極めて重要である。 臨床医は、より小さな変化の増分を検出するために、少なくとも2つの再現性のあるベースライン視野を得るべきである。 特に進行時に治療を強化した後、進行を認識するためには、臨床医は新たなベースラインを確立することが必要である。
症例3. Paracentral Glaucoma Defect
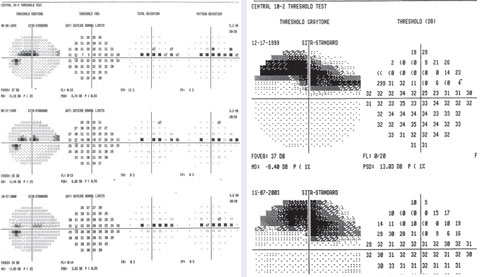
24-2でsuperior paracentral scotomaの可変点を10-2でfocal deep defectとした例。
現在の内科または外科治療以前に、あるいは治療から離れフォローアップに長期間の間、行った視野は、進行を決定する目的で使用されてはならない。 臨床医は、これらの治療変更後に行われた新しいベースライン視野、およびその後のあらゆる視野を、進行の判断に用いるべきである。
信頼できる代表的なベースラインは、進行解析プログラムにとっても重要である。 視野は偏心した位置や中距離の感度で変動が大きくなる傾向があり、長期間の変動は進行の判定を難しくする。 中間の感度点では変動が大きくなる傾向があるが、上下の感度範囲の検査値はより安定する。 信頼性が高く、再現性のあるベースライン視野を確立することで、これらの課題を取り除くことができる。
非緑内障性視神経症 視野は、視覚経路に影響を及ぼす病変の評価、ベースラインの確立、視神経症に関連する特定の薬剤のスクリーニングツールとして機能することができる。 5 非緑内障性視神経症の最も一般的な視野症状は、中心欠損である。 緑内障以外の視神経障害で最も多い視野症状は中心欠損です。暗室が大きいほど視力が低下する可能性が高くなります(表1)。
網膜色素変性症は周辺視野欠損を生じ、進行すると中心のみのトンネル視になることがある。
動脈閉塞は一般的に絶対的な欠損域を示すが、静脈閉塞はより浅く拡散していることがある2。
horioretinitis、またはそれに伴う傷跡は、弧状または楔状の欠損で緑内障性欠損を覆い隠すことができる。 網膜剥離は相対的な欠損を生じ、網膜弛緩症は絶対的な欠損を有する。 これらの状態は、24-2や30-2を用いた従来の中心的な検査で現れるものよりも、はるかに末梢的であることが多いのです。
緑内障の欠陥
欠陥は、正規化されたデータベースと比較して、感度の一般的または局所的な低下である。 一般的な低下は白内障で最もよく見られますが、未矯正の屈折異常やミオシスでも起こり得ます。 局所的な欠陥は、診断に役立つように、大きさ、深さ、位置によってさらに説明することができる。 相対的欠陥は、感度が通常より低い場合、または視野の他の領域と比較して低下する場合がありますが、視力は維持されます。 絶対的欠陥とは、刺激が最大輝度で提示されても見えない場合である。
緑内障性視野欠損は、最初に鼻側または弧状領域(Bjerrum領域)に生じることがある。 これらの欠損は盲点から黄斑部周辺に広がり、鼻側の水平子午線で突然終了することがある。 初期の緑内障性欠損は、しばしば局所的な相対的スコトーマである(表2)。
かなりのテスト-レテスト変動は、緑内障性視野欠損によって影響を受けた視野領域の特徴である。 2偽陰性に見られるような変動は信頼性を示すかもしれないが、より大きな変動は病気そのものに起因することが多い。 特異度・感度の高い緑内障性視野欠損の基準13,14
- p
- GHT 連続2視野で正常範囲外のパターン偏移上の非エッジ点3点以上のクラスター
- PSD
- MDの非対称>1.MDの非対称性
GHTが2視野で正常範囲外
視野が信頼できない場合、ベースラインの確立、欠損の確認、進行の疑いの確認のために繰り返される必要があります。 通常、患者の疲労が信頼性に影響するため、同じ日に視野を繰り返すことはない。 緑内障は一般的にゆっくりと進行する視神経障害であり、治療の決定は変化率によって行われるため、すぐに視野を再確認する必要があることは稀である2。 視野の進行は、感度のびまん性低下、既存の欠陥の深化または拡大、または新しい欠陥の発生による場合がある。 視野の新しい領域が影響を受ける前に、陥凹領域が進行することが最も一般的である。 変化や進行が一定になる前に、最初に視野の変動が大きくなることがある。 長期的な変動と悪化傾向のどちらを示すかを鑑別することが重要である。 臨床医は、視野が悪化していることを確認したら、その変化が緑内障によるものなのか、それとも他の疾患によるものなのかを判断しなければならない。 統計学的、臨床的に有意な視野の変化により、臨床医は患者の治療と管理計画に必要な変更を行うことができる。
どの患者がゆっくり進行し、どの患者が急速に進行するかを予測するのは難しいが、時間の経過とともに進行速度が評価されれば、それに応じて患者の管理を変更する必要がある。 例えば,視野欠損の急速な進行の兆候を示す若い患者は,初期の視野欠損の進行が遅い高齢の患者よりも積極的な管理計画が必要である。 患者の治療と管理は、視野欠損や進行速度など、患者固有の臨床像に基づいて個別に行うのが妥当である。 進行速度が決定され、治療の変更が開始されない場合、過去の進行速度が将来の進行速度を予測できることが研究で示されている10,11。同時に、治療のエスカレーションにより、進行速度を変更することが可能である。 介入した後は、新しいベースラインを設定する必要があります。
表3. 進行の判定に関する提案
- 異常領域の3点が10dB減少*
- 新たに2点が減少。 欠陥付近が10dB低下*
OR
- 中心15度の2点または外側15度の3点が10dB低下*
OR
- 統計比較(p
※2フィールド以上連続14点時。17
経年変化を評価することは、緑内障管理において非常に重要である。 HFAに搭載されているGPA(Guided Progression Analysis)ソフトウェアを使用すると、2つのベースライン視野検査が特定されます。 その後の視野検査は、パターン偏差値を用いて平均化されたベースラインと比較される。 年齢と欠陥をマッチさせた安定した緑内障患者の集団の変動より大きい程度にフォローアップ値が低下したとき、そのポイントが特定される。 連続した再検査で変化が持続する場合、ポイントは可能性がある(連続2フィールド)または可能性がある(連続3フィールド以上)としてマークされる。
GPAはトレンド解析とイベント解析の両方を用いて、視野の進行を特定し定量化することで医師を支援する。 イベント解析では、ある点または点のグループの統計的に有意な変化を調べ、トレンド解析では、将来の予測を含む経時的な変化の方向または変化率を定量化します。 臨床医は、びまん性損失の過小評価の可能性、パターン逸脱に関連する可能性のある微妙なアーチファクト、最適な分析のための十分な数の高品質な視野(最低5枚)の必要性に注意を向けることができます。 しかし、GPAは他の解析ツールに比べ、白内障の影響を受けにくい。 各検査法は、それぞれ独自の規範データベースを使用する2。さらなる目標は、進行速度を特定し、急速に進行し、ますます積極的な治療が必要となる患者を分離することである。
非緑内障性視神経症の進行
GPAは特に緑内障の管理のために確立されたので、臨床医は非緑内障性疾患の進行の可能性を評価する際に異なるアプローチを取らなければなりません。 2
フォローアップ
同じ検査方法とパターンを使用することで、比較と進行のモニタリングが容易になる。 確立された緑内障患者をペリメトリーでフォローすることは、現在の管理が適切であるか、視野の安定または進行に基づいて治療の変更が必要であるかを判断するのに不可欠である。
フォローアップの頻度は、疾患の程度と臨床経過に依存する。 安定性を示す患者は、フォローアップの間隔を合理的に長くすることができる。
アーチファクト
視野の解釈にさらなる課題をもたらす、いくつかのアーチファクトが存在する。 臨床医は、臨床像に関連する病理からの真の視野欠損と、発生しうるアーチファクトを見分けなければならない。 視野欠損が本物かアーチファクトかはっきりしない場合、疑いと臨床像のレベルに基づいて、適切な時間軸で視野を再確認する必要がある。 注意すべきアーチファクトは以下の通りです:
– 眼瞼下垂と眉毛下垂。 これは、上端ポイントに沿った密な上端欠損を引き起こす可能性があります。 視覚的に著しい眼瞼下垂のある患者は、検査のために瞼をテープで固定するとよいでしょう。
– リムアーチファクト。 トライアルレンズホルダーの位置が患者の眼から遠すぎる場合、リムアーチファクトが発生し、完全または部分的なリングスコトーマが発生することがある。
– 不正確な屈折率。 白内障を模倣した全般的な感度の低下を招くことがあります。 高い屈折異常は拡大または縮小効果を生み出し、適切な頂点距離の計算を必要とします。 間違ったレンズパワー記号を使用したり、患者が白内障手術を受けた後に新しい屈折誤差を使用しなかったりすることは、よくある2つの誤りです。
– 患者の疲労。 これは検査時間の長さ、高い偽陰性値、または優先的に周辺部感度の異常として現れることがある。 末梢点は検査の後半に検査され、疲労や注意力が低下している場合には著しく低下し、グレースケール上でより暗い、葉状リングまたはクローバーリーフパターンになることがあります。 これらの一般的に遭遇するアーチファクトを認識することで、視野の解釈を改善し、検査結果の信頼性と品質の限界を認識することができる。 各診療所では、望ましい検査方法とパターンを標準化し、フォローアップ検査を通してより正確な比較を可能にするために、フォローアップ診察時に同じ検査を繰り返すべきである18。 臨床像全体を評価し、変数の相関と一致を確認することが重要である。 不確実性がある場合は検査を繰り返し、より信頼性の高い基準値を設定し、進行の可能性を確認する必要があります。
Drs. DraskovicとMcSoleyは、Bascom Palmer Eye Instituteのスタッフオプトメトリストです。 レンズA、Langley T、Nemeth SC、Shea C。 視覚経路。 で。 眼球の解剖学と生理学。 茨木市:SLACK; 1999:90-5.
2. Heijl A, Patella VM, Bengtsson B. The Field Analyzer Primer: Effective Perimetry. 第4版. カールツァイスメディテック; 2012.
3. パークHY、ホワンBE、シンHY、パークCK. ハンフリー10-2視野における鳩目傍スコトーマの存在をハンフリー24-2視野を用いて予測するための臨床的手がかり。 Am J Ophthalmol. 2016;161:150-9.
4. Ehrlich AC, Raza AS, Ritch R, et al. 従来の視野検査パターンを修正し、中心10°の早期緑内障性欠損の検出を向上させること。 Transl Vis Sci Technol. 2014 Oct;3(6):6.
5. ケダーS、ガテD、コルベットJJ. 神経眼科における視野(Visual Fields in Neuro-Ophthalmology). Indian Journal of Ophthalmology. 2011;59(2):103-9.
6. Wall M, George D. Idiopathic intracranial hypertension. 50名の患者を対象としたプロスペクティブスタディ。 Brain. 1991;114:155-80.
7. ケルトナーJL、ジョンソンCA、スパーJO、ベックRW. 視神経炎のベースライン視野プロファイル。 視神経炎治療トライアルの経験。 視神経炎研究会。 Arch Ophthalmol. また、このような場合にも、「視力検査」を実施する。 Arch Ophthalmol. 2005;123:1554-62.
9. Hayreh SS. 後発性虚血性視神経症:臨床的特徴、病因、管理。 目(Lond)。 2004;18:1188–206.
10. Bengtsson B. Prediction of glaucomatous visual field loss by extrapolation of linear trends(線形トレンドの外挿による緑内障性視野欠損の予測). Arch Ophthalmol. 2009;127(12):1610-5.
11. Heijl A. 眼圧の低下と緑内障の進行. Arch Ophthalmol. 2002;120(10):1268-79.
12. Willmore LJ, Abelson MB, Ben-Menachem E, et al.ビガバトリン:2008年最新情報. Epilepsia. 2009;50:163–73.
13. Katz J, Sommer A, Gaasterland DE, Anderson DR. 緑内障性視野欠損を検出するための解析アルゴリズムの比較。 Arch Ophthalmol. 1991;109(12):1017-25.
14. Hodapp E, Parrish RK II, Anderson DR. 緑内障の臨床的判断。 St: CV Mosby Co;1993:52-61。
15. フォイヤーWJ、アンダーソンDR. 初期の緑内障性視野欠損における静的閾値の非対称性。 Ophthalmology。 1989;96:1285-97.
16. Brenton RS, Phelps CD, Rojas P, Woolson RF. 健常者における視野の眼間差。 このような場合、「己の眼で見る」ことが重要です。 緑内障の臨床管理およびアウトカム研究における進行の基準. Am J Ophthalmol. 2000;130(6):827-29.
18. Weinreb RN. 緑内障の進行. 世界緑内障協会の第8回コンセンサスレポート。 Amsterdam: Kugler Publications; 2011.
.