Evaluating the visual pathway can be integral to diagnosing and managing numerous conditions.
By Kristie Draskovic, OD, and John J. McSoley, OD
- Release Date:
- Expiration Date:
- Goal Statement:
- Faculteit/redactieraad:
- Credit Statement:
- Joint-Sponsorship Statement:
- Verklaring van openbaarmaking:
- Case 1. Hypofyse Macroadenoom
- Tabel 1. Optische neuropathieën die vaak worden gedetecteerd met gezichtsveldtests
- Geval 2. Multiple Sclerose
- Geval 3. Paracentraal glaucoomdefect
- Tabel 2. Criteria voor glaucoom gezichtsvelddefect met hoge specificiteit en sensitiviteit13,14
- Tabel 3. Suggesties voor het beoordelen van progressie
Release Date:
Maart 2016
Expiration Date:
Maart 1, 2019
Goal Statement:
Het onderzoeken van de visuele velden met behulp van geautomatiseerde perimetrie kan clinici helpen bij het evalueren van laesies die de visuele baan beïnvloeden, het vaststellen van basislijnen en het screenen op bepaalde medicatie-geïnduceerde optische neuropathieën. Het kan ook helpen bij het monitoren van progressie of recidief van ziekten, het begeleiden van behandelingsbeslissingen en helpen bij het lokaliseren van laesies. Dit artikel zal clinici helpen visuele velden bij glaucoom- en niet-glaucoom-ziekteprocessen beter te begrijpen en te interpreteren.
Faculteit/redactieraad:
Kristie Draskovic, OD, en John J. McSoley, OD
Credit Statement:
Deze cursus is COPE goedgekeurd voor 2 uur CE-krediet. COPE ID is 48599-GL. Controleer uw staat licentie board om te zien of deze goedkeuring telt voor uw CE vereiste voor relicensure.
Joint-Sponsorship Statement:
Deze permanente educatie cursus wordt gezamenlijk gesponsord door de Pennsylvania College of Optometry.
Verklaring van openbaarmaking:
Drs. Draskovic en McSoley hebben geen financiële relaties openbaar te maken.
Het onderzoeken van het gezichtsveld is essentieel bij het overwegen van mogelijk gezichtsverlies door aandoeningen die het visuele pad beïnvloeden. Standaard geautomatiseerde perimetrie is een nuttig hulpmiddel voor het identificeren en volgen van vele neurologische aandoeningen, evenals glaucoom en glaucoomverdachten. Hoewel er momenteel verschillende apparaten beschikbaar zijn, zal in de volgende bespreking het gebruik van de Humphrey Field Analyzer (HFA, Zeiss) als voorbeeld worden beschouwd.
Anatomie en fysiologie
Dankzij de anatomie van het visuele pad, kunnen clinici probleemgebieden detecteren bij vele aandoeningen die visuele stoornissen veroorzaken (figuur 1). Omdat het licht van het temporale gezichtsveld op het nasale netvlies valt, worden netvliesbeschadigingen in het tegenovergestelde kwadrant van het gezichtsveld gezien. Alle prechiasmale laesies, inclusief die op het netvlies en de oogzenuw, zullen aanleiding geven tot defecten die geïsoleerd zijn van het aangetaste oog.1
Aangezien de neusvezels verantwoordelijk zijn voor het temporale gezichtsveld, zal een laesie aan het optische chiasme resulteren in een gezichtsvelddefect dat het temporale veld van beide ogen beïnvloedt, en aanleiding geeft tot de klassieke bitemporale hemianopsie, die de verticale middellijn respecteert.1 Laesies van het optische chiasme kunnen het gevolg zijn van hypofyse-adenomen, suprasellaire meningiomen, craniofaryngiomen of aneurysma’s. In sommige gevallen kunnen gezichtsveldafwijkingen omkeren na behandeling van de oorzaak.2
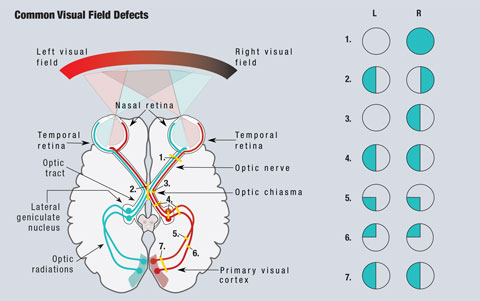
Klik op de afbeelding om te vergroten. Afb. 1. Een vereenvoudigd schema van de visuele pathway wordt getoond. Lesies die de visuele pathway onderbreken leiden tot gezichtsvelddefecten. (1) Een volledige laesie van de rechter oogzenuw leidt tot een volledig verlies van het rechter gezichtsveld. (2) Een laesie in de middellijn van het optische chiasme leidt tot een bitemporale hemianopsie. (3) Een laesie van de ongekruiste vezels van de rechter oogzenuw ter hoogte van het optisch chiasme leidt tot een nasale hemianopsie van het rechteroog. (4) Een volledige laesie van de rechter optische tractus, laterale geniculate nucleus, of optische radiaties leidt tot een volledige linker homonieme hemianopsie. (5) Een laesie van de rechter bovenste optische radiaties resulteert in een linker inferieure quadranopsie. (6) Een laesie aan de rechter onderste optische radiaties veroorzaakt een linker superieure quadranopsie. (7) Een laesie van zowel de superieure als de inferieure rechter optische radiaties veroorzaakt een linker homonieme hemianopsie. Illustratie van Miquel Perello Nieto.
Vezels die verantwoordelijk zijn voor het gezichtsveld rechts van de middellijn worden aan de linkerkant van de hersenen aangetroffen, en omgekeerd. Als gevolg van deze cross-over veroorzaken alle post-chiasmale laesies, inclusief laesies van de optische tractus en de optische radiaties, een homonieme hemianopsie.1 Deze defecten bevinden zich aan dezelfde kant van het gezichtsveld in elk oog en respecteren de verticale middellijn. Wanneer de defecten alleen superieur of inferieur worden gezien, spreekt men van een quadranopsie. In het geval van onvolledige hemianopsie defecten, zijn anterior laesies meestal meer incongruent, terwijl posterior laesies meer congruent zullen zijn tussen de twee ogen.1
Glaucoomateuze gezichtsvelduitval vertegenwoordigt schade aan de axonen die langs de retinale zenuwvezellaag reizen en gewoonlijk een arcuate patroon volgen naar de oogzenuw. Schade aan deze axonen geeft aanleiding tot gelokaliseerde gezichtsvelddefecten, meestal arcuate scotomen, nasale stappen en paracentrale scotomen. Een normaal gezichtsveld strekt zich in de breedte uit tot 90 graden in de breedte, 70 graden zowel in de hoogte als in de diepte en 60 graden in de breedte en vanaf de fixatie. De meest waardevolle informatie voor neurologische tekorten en glaucoom management wordt verkregen binnen 30 graden van fixatie.2
Teststrategie
Automatische statische perimetrie-en drempelperimetrie in het bijzonder-voorziet een stimulus van vaste grootte maar van variabele intensiteit. De gevoeligheid van de verschillende testlocaties wordt geregistreerd op basis van de reacties van de patiënt op deze stimuli. Een grootte III stimulus (die 4mm2 is wanneer geprojecteerd op een schaal van 30cm) wordt gewoonlijk gebruikt in de klinische praktijk.
Er zijn verschillende drempeltestpatronen beschikbaar. De 30-2 test patroon test 76 locaties binnen 30 graden van fixatie, terwijl een 24-2 test patroon test 54 locaties verwijderen voor de ring van punten op 30 graden (met uitzondering van de twee punten die straddle de horizontale meridiaan nasaal). Deze meest perifere punten zijn gevoeliger voor variabiliteit, en 24-2 verkort de testtijd door deze perifere punten uit de test te halen. De afstand tussen de testpunten is zes graden.
Daarnaast richt het 10-2 testpatroon zich op 64 punten binnen 10 graden van fixatie, gescheiden door twee graden. Deze optie verdient de voorkeur wanneer centrale of paracentrale defecten ontstaan met de 24-2 en 30-2 of wanneer het veld zo vernauwd wordt dat de perifere punten klinisch niet bruikbaar zijn. De clinicus kan er ook voor kiezen de stimulusgrootte te verhogen tot V, hetgeen zich hogere gevoeligheidswaarden kan veroorloven en een groter dynamisch bereik waardoor patiënten kunnen worden gevolgd voor verandering. Momenteel bestaat er echter geen testalgoritme van het SITA-type, noch is er een vergelijking met een normatieve databank of progressie-analyse beschikbaar.
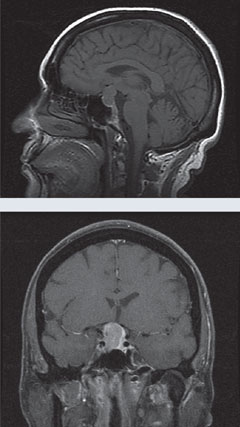
Case 1. Hypofyse MacroadenoomEen patiënt presenteerde zich voor consultatie in de setting van atypische, progressieve normale spanning glaucoom. |
|
|

|
| Hierboven toont het 24-2 gezichtsveld van de patiënt bitemporaal gezichtsvelduitval aan. In de MRI’s links, de T1 sagittale zonder gadolinium en T1 coronale beelden met gadolinium onthullen een grote sellaire massa met lichte versterking en een drukkend effect op het chiasme. Deze bevinding is consistent met hypofyse macroadenoom. Klik op de beelden om ze te vergroten. |
|

|
|
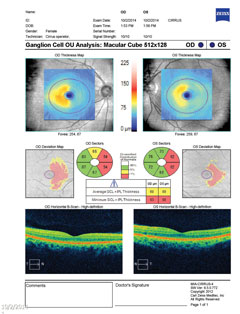
| Nadat de patiënt een transsfenoïdale operatie onderging om de sellar-massa te verwijderen, toont het gezichtsveld hierboven verbetering van het gezichtsvelddefect in het rechteroog en oplossing van het defect in het linkeroog. Klik op de afbeelding om te vergroten. | |
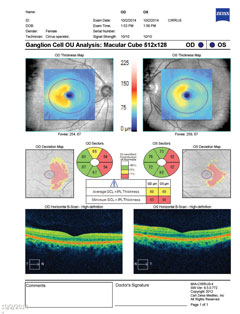
| Hierboven toont het ganglioncelcomplex nasale verdunning in beide ogen, wat correleert met het temporale gezichtsveldverlies. Klik op de afbeelding om te vergroten. | |
Recente studies tonen aan dat 10-2 gezichtsvelden nuttig kunnen zijn voor het identificeren van meer dan gevorderd glaucoom.3,4 Eén studie toonde aan dat sommige glaucoompatiënten significante centrale clusterafwijkingen hadden die werden gezien op 10-2 testpatronen, ondanks een normaal centraal 30-2 gezichtsveld.4 De studie suggereert dat, als gevolg van slechte ruimtelijke sampling, glaucoom centrale veld verslechtering niet kon worden opgepikt door de 30-2 test raster alleen, en een dichtere schatting van de centrale 10 graden nodig was.4 Het suggereert ook dat het wijzigen van het conventionele visuele veldtestpatroon de detectie van vroege glaucoomafwijkingen in de centrale 10 graden zou kunnen verbeteren.4
In de dagelijkse praktijk voeren artsen vaak 10-2 velden uit wanneer kleine centrale of paracentrale scotomen verschijnen op 30-2 en 24-2 testen, of wanneer de scherpte wordt vermoed of dreigt te worden verlaagd als gevolg van veldverlies. Ook kan een 10-2 testpatroon een nuttige aanvulling zijn wanneer er een grote inter-test variabiliteit is van paracentrale punten op een 24-2 patroon. De groeiende aandacht voor de ganglion cel functie in de maculaire regio zou ook de aandacht kunnen verhogen voor het gebied van het gezichtsveld getest door het 10-2 patroon.
Betrouwbaarheid
Aanduidingen van betrouwbaarheid van de gezichtsveld prestatie omvatten fixatie verliezen en zowel vals positieve als vals negatieve reacties.
Tabel 1. Optische neuropathieën die vaak worden gedetecteerd met gezichtsveldtests |
|
| Idiopathische intracraniële hypertensie | Vroeg: vergrote blinde vlek Laat: gegeneraliseerde vernauwing5,6 (kan verbeteren met behandeling) |
| 0ptische neuritis | – Diffuus gezichtsveldverlies (in bijna de helft van de gevallen) – Andere: altitudinale defecten, centrale of cecocentrale scotomen, arcuate of dubbele arcuate defecten en hemianopische defecten5,7 |
| Non-arteritic anterior ischemic optic neuropathy | – Altitudinale defecten die de horizontale middellijn respecteren komen het meest voor – Andere: centrale scotomen, arcuate defecten en quadranopsias5,8 |
| Posterior ischemic optic neuropathy | – Centraal veld defect5,9 |
| Hereditaire optische neuropathieën – Erfelijke optische neuropathie van Leber – Dominante optische atrofie |
– Cecocentraal en centraal gezichtsvelduitval5 |
| Optische zenuwkop drusen | – Kan een glaucoom patroon imiteren |
| Thyroid ophthalmopathy | – Grote variabiliteit – Kan gedeeltelijk of geheel verdwijnen na behandeling2 |
| Medication-induced toxic optic neuropathy | – Ethambutol (voor tuberculose behandeling) toxiciteit kan centrale scotomas veroorzaken en, minder vaak, perifere vernauwing en afwijkingen in het gezichtsveld5 – Vigabatrine (een anti-epileptisch geneesmiddel) kan velddefecten veroorzaken die beginnen als bilaterale nasale defecten en later overgaan in concentrische velddefecten terwijl het centrale veld intact blijft12 |
Fixatie kan worden gecontroleerd door periodieke presentatie van een stimulus op de fysiologische blindspot (Heijl-Krakau methode) of door de positie van de corneale lichtreflex te controleren. Op de HFA duidt opwaartse afbuiging op verandering van positie of fixatie; neerwaartse afbuiging duidt erop dat de cornea-lichtreflex niet kan worden gelokaliseerd, zoals tijdens een verandering van hoofd- of ooglidpositie.
Vals-positieven treden op wanneer een patiënt reageert op een moment dat er geen geassocieerde stimulus is of wanneer een reactie fysiologisch niet mogelijk is. Patiënten met veel fout-positieven worden vaak omschreven als “trigger happy”. Dit kan een visueel veld onthullen dat gevoeliger of normaler lijkt dan verwacht of kan leiden tot abnormaal hoge drempelgevoeligheidswaarden.
Vals-negatieven treden op wanneer een patiënt niet reageert op een stimulus die helderder is dan een stimulus die al is gezien of wanneer de reactie niet consistent is met het patroon van reacties in dat gebied. De vals-negatieve waarde kan een aanwijzing zijn voor de betrouwbaarheid of een weerspiegeling van het ziekteproces. Abnormale regio’s van het gezichtsveld worden geassocieerd met meer intra-test en inter-test variabiliteit. Dientengevolge worden regio’s van het gezichtsveld met lage gevoeligheid niet opgenomen in de berekening van de fout-negatieve waarde.
De drempelgevoeligheid zijn ruwe gegevens met waarden in decibels. De getallen geven de mate van verzwakking ten opzichte van de maximaal mogelijke stimulus aan. Waarden van
De totale afwijking geeft de afwijking van de verwachte waarden aan op basis van de leeftijdsgematchte normale database. De patroonafwijking corrigeert voor de algemene gevoeligheid van het veld door veralgemeende depressies te verwijderen (b.v. door cataract) om eventuele gebieden met gelokaliseerde afwijkingen te identificeren. Zowel de totale als de patroonafwijking hebben bijbehorende waarschijnlijkheidswaarden (p), berekend op basis van de verdeling binnen een normale populatie. Het bereik van normale waarden is perifeer groter dan in het centrum. P-symbolen geven de frequentie aan van het voorkomen van de geteste waarde in een normale leeftijdsgematchte populatie. Afwijkingen worden op de kaart getoond als de geteste drempelwaarde slechter is dan de onderste 5% van normaal voor die leeftijd.2 Bijvoorbeeld, als p
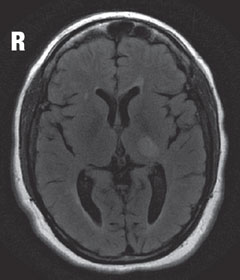
Geval 2. Multiple ScleroseEen patiënt met de diagnose multiple sclerose (MS) had gezichtsverlies. |
|
|
 |
|
|
Patroon standaarddeviatie (PSD) is een gewogen standaardafwijking van de waarde die wordt verwacht op basis van leeftijdsgematchte normale waarden en de gemiddelde deviatie (MD) index. De PSD geeft de afstand tussen verschillende punten in het veld weer. PSD is gevoelig voor zowel vroege als focale glaucoomafwijkingen. Een lage PSD-waarde kan worden gezien bij normale gezichtsvelden, een gezichtsveld dat uniform gedeprimeerd is of een volledig blind veld. Een bijbehorende p-waarde is de waarschijnlijkheid dat de waarde zich voordoet.
De MD is een gewogen gemiddelde van waarden in de numerieke plot van de totale afwijking. De MD kan worden beïnvloed door een diffuse daling van de totale gevoeligheid of door een gelokaliseerde afwijking. Een MD van 0 wijst op een normale waarde, terwijl een negatieve waarde staat voor een afwijking of verlies ten opzichte van het normale gegevensbestand. Gemiddelde afwijking weegt centrale punten zwaarder.
Visual field index (VFI) is een andere leeftijdgecorrigeerde beoordeling, uitgedrukt in een percentage, waarbij perimetrisch normaal 100% is en perimetrisch blind 0%. Bij de berekening van de VFI worden centrale punten zwaarder gewogen dan perifere punten. Het levert een score op voor een individueel gezichtsveld en wordt gebruikt bij progressieanalyse.2
De glaucoom hemifield test (GHT) vergelijkt de relatieve gevoeligheid van patroonafwijkingswaarden van vijf zones in de superieure en inferieure hemifields. Elk van deze zones wordt vergeleken met zijn spiegelzone in het tegenoverliggende hemiveld, en beide zones worden vergeleken met de normatieve database. GHT kan glaucoom gezichtsvelduitval detecteren met hoge gevoeligheid en hoge specificiteit via vijf mogelijke categorieën: buiten normale grenzen, borderline, algemene vermindering van gevoeligheid, abnormaal hoge gevoeligheid en binnen normale grenzen.
Interpretatie
Het vaststellen van een betrouwbaar visueel basisveld is van cruciaal belang bij het beheer van glaucoom en de toekomstige controle op mogelijke progressie. Clinici moeten ten minste twee reproduceerbare basislijn gezichtsvelden verkrijgen om kleinere toename van verandering te detecteren. Het herkennen van progressie, met name na escalatie van de therapie op momenten van progressie, zal de clinicus vereisen om een nieuwe basislijn vast te stellen.
Geval 3. Paracentraal glaucoomdefect
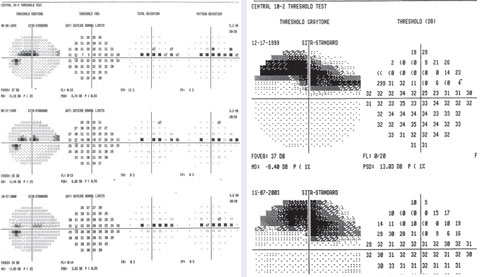
Een voorbeeld van variabele punten in superieur paracentraal scotoom op 24-2 met een focaal diep defect op 10-2.
Zichtvelden die zijn gemaakt vóór de huidige medische of chirurgische behandeling, of tijdens een lange periode waarin geen follow-up van de behandeling heeft plaatsgevonden, mogen niet worden gebruikt om progressie vast te stellen. Artsen moeten de nieuwe basislijn visuele velden uitgevoerd na deze behandelingswijzigingen, en elk visueel veld daarna gebruiken bij het beoordelen van progressie.
Een betrouwbare en representatieve uitgangslijn is ook belangrijk voor progressieanalyseprogramma’s. Visuele velden hebben de neiging een hogere variabiliteit te hebben met meer excentrische locatie en gevoeligheden in het middengebied, en fluctuatie op lange termijn maakt het beoordelen van progressie een grotere uitdaging. Gevoeligheidspunten in het middengebied hebben de neiging variabel te zijn, terwijl testwaarden in de hogere en lagere gevoeligheidsbereiken stabieler zijn. Het vaststellen van een betrouwbare, reproduceerbare basislijn gezichtsveld kan helpen sommige van deze uitdagingen weg te nemen.
Niet-glaucoomateuze Optische Neuropathieën
Visuele velden kunnen helpen bij het evalueren van laesies die de visuele route beïnvloeden, basislijnen vaststellen en fungeren als screening-instrumenten voor bepaalde geneesmiddelen die geassocieerd zijn met optische neuropathieën. Ze kunnen ook de progressie of recidief van ziekten controleren en helpen bij het nemen van beslissingen over behandeling en zelfs bij het lokaliseren van laesies.5 De meest voorkomende gezichtsveld manifestatie van een niet-glaucoomateuze optische neuropathie is een centraal defect. Hoe groter het scotoma, hoe groter de kans dat de gezichtsscherpte verminderd is (tabel 1).
Retinale ziekte
Zichtvelddefecten veroorzaakt door retinale ziekte hebben meestal goed gedefinieerde, scherpe grenzen die dieper lijken dan de meeste glaucoomdefecten met minder variabiliteit.2 Veel voorkomende aandoeningen die het maculaire gebied aantasten, zoals leeftijdsgebonden maculaire degeneratie en centrale sereuze chorioretinopathie, kunnen aanleiding geven tot centrale scotomen die kunnen worden gezien op 10-2 evenals sommige 24-2 en 30-2 testen, afhankelijk van de mate van schade.
Retinitis pigmentosa geeft aanleiding tot perifere gezichtsvelddefecten, die kunnen leiden tot tunnelvisie met alleen een centraal eiland bij gevorderde ziekte.
Chorioretinitis, of geassocieerde littekens, kunnen glaucoom defecten maskeren met een arcuate of wig-achtig defect. Een netvliesloslating zal aanleiding geven tot een relatief defect, terwijl retinoschisis een absoluut defect zal vertonen. Deze aandoeningen zijn vaak veel perifeerder dan wat zou blijken uit conventionele centrale tests met 24-2 of 30-2.
Glaucoomdefecten
Een defect kan een algemene of plaatselijke depressie van de gevoeligheid zijn in vergelijking met de genormaliseerde database. Algemene depressies worden het meest gezien bij cataract, maar kunnen ook het gevolg zijn van ongecorrigeerde refractieafwijking of miosis. Gelokaliseerde defecten kunnen verder worden beschreven aan de hand van grootte, diepte en plaats om de diagnose te helpen stellen. Een relatief defect treedt op wanneer de gevoeligheid minder is dan normaal, of verminderd is ten opzichte van andere delen van het veld, maar het gezichtsvermogen behouden blijft. Van een absoluut defect is sprake wanneer de stimulus op maximale helderheid wordt gepresenteerd en niet wordt gezien.
Glaucoom gezichtsvelduitval kan eerst optreden in het nasale of in het arcuate gebied (Bjerrum gebied). Deze defecten kunnen zich uitbreiden van de blinde vlek, rond de maculaire regio, abrupt eindigend bij de horizontale meridiaan nasaal. Vroege glaucoom defecten zijn vaak gelokaliseerde relatieve scotomen (tabel 2).
Aanzienlijke test-hertest variabiliteit is het kenmerk van gezichtsveldgebieden aangetast door glaucomateus gezichtsveldverlies. Variabele gevoeligheidsreducties die zich in hetzelfde gebied voordoen, maar niet altijd op dezelfde testpuntlocaties, gaan gewoonlijk vooraf aan consistente glaucoom-velddefecten.2 Variabiliteit, zoals wordt gezien bij vals-negatieven, kan wijzen op betrouwbaarheid, maar grotere hoeveelheden variabiliteit worden vaak gezien als gevolg van de ziekte zelf.
Tabel 2. Criteria voor glaucoom gezichtsvelddefect met hoge specificiteit en sensitiviteit13,14
- Cluster van drie of meer niet-randpunten op de patroonafwijking met p
- GHT buiten de normale grenzen op twee opeenvolgende velden
- PSD
- Asymmetrie van MD >1.50dB die herhaalbaar is en in de setting van klinische verdenking15,16
Wanneer visuele velden onbetrouwbaar zijn, moeten ze worden herhaald om basislijnen vast te stellen, een defect te bevestigen of vermoedelijke progressie te bevestigen. Gewoonlijk worden de gezichtsvelden niet op dezelfde dag herhaald in verband met vermoeidheid van de patiënt, wat de betrouwbaarheid kan beïnvloeden. Het is zelden urgent om het gezichtsveld onmiddellijk te laten herhalen, omdat glaucoom over het algemeen een langzaam progressieve optische neuropathie is, en beslissingen over behandeling worden gestuurd door de snelheid van verandering.2 Elke praktijk zou een voorkeurs teststrategie en -patroon moeten standaardiseren en dezelfde test moeten herhalen om nauwkeurigere vergelijkingen bij vervolgonderzoek mogelijk te maken.10
Progressie
Evaluatie van verandering stelt de arts in staat om te bepalen of de toestand stabiel is, progressie vertoont of verbetert. Progressie in een gezichtsveld kan het gevolg zijn van een diffuse afname in gevoeligheid, bestaande defecten kunnen dieper worden of uitbreiden of er kunnen nieuwe defecten ontstaan. Gedeprimeerde gebieden gaan het vaakst vooruit voordat nieuwe gebieden van het gezichtsveld worden aangetast. Een aanvankelijke toename van de variabiliteit van het gezichtsveld wordt soms gezien voordat een verandering of progressie constant wordt. Het is belangrijk om te onderscheiden of er sprake is van lange termijn fluctuatie of een verslechterende trend. Zodra clinici vaststellen dat het gezichtsveld slechter is, moeten zij beslissen of de verandering te wijten is aan glaucoom of aan een andere ziekte-entiteit. Statistisch en klinisch significante veranderingen op het gezichtsveld stellen de arts in staat om de nodige wijzigingen aan te brengen in het behandelings- en beheersplan van de patiënt.
Behandelaars moeten ook evalueren hoe de snelheid van progressie de levenskwaliteit van de patiënt kan veranderen.2 Bijvoorbeeld, clinici moeten voorzichtiger zijn met het behandelen van jongere patiënten met snellere progressie en monoculaire patiënten (tabel 3).
Hoewel het moeilijk te voorspellen is welke patiënten langzaam versus snel zullen vooruitgaan, moet, zodra een progressiesnelheid in de tijd is geëvalueerd, het beheer van de patiënt dienovereenkomstig worden gewijzigd. De jongere patiënt die tekenen van snelle progressie van gezichtsvelddefecten vertoont, bijvoorbeeld, zal een agressiever beheersplan nodig hebben dan een oudere patiënt met langzame progressie van een vroeg velddefect. Het is redelijk dat de behandeling en het beheer van patiënten worden gepersonaliseerd op basis van hun specifieke klinische beeld, met inbegrip van hun veldverlies en de snelheid van progressie. Onderzoek toont aan dat als de progressiesnelheid wordt bepaald en er geen verandering in de behandeling wordt aangebracht, de progressiesnelheid in het verleden voorspellend kan zijn voor de toekomst.10,11 Tegelijkertijd kan de progressiesnelheid worden veranderd door de therapie te escaleren. Zodra wordt ingegrepen, moet een nieuwe uitgangswaarde worden vastgesteld.
Tabel 3. Suggesties voor het beoordelen van progressie
- Drie punten in een abnormaal gebied verminderen met 10dB*
- Twee nieuwe punten nabij een defect verminderd met 10dB*
OR
- Twee punten in centrale 15 graden of drie buiten 15 graden verminderd met 10dB*
OR
- Statistische vergelijkingen (p
*Op twee of meer opeenvolgende velden14,17
Evaluatie van veranderingen in de tijd is van cruciaal belang bij glaucoombehandeling. Met de GPA-software (Guided Progression Analysis) op de HFA worden twee basislijn-visusveldtests geïdentificeerd. Latere gezichtsveldtesten worden dan vergeleken met de gemiddelde basislijn aan de hand van de patroonafwijkingswaarden. Wanneer de follow-up waarden dalen in een mate die groter is dan de variabiliteit van een leeftijd en afwijking gematchte populatie van stabiele glaucoompatiënten, wordt het punt geïdentificeerd. Indien de verandering bij opeenvolgende herhalingstests aanhoudt, worden de punten gemarkeerd als mogelijk (twee opeenvolgende) of waarschijnlijk (drie of meer opeenvolgende velden).
GPA gebruikt zowel trend- als gebeurtenisanalyse om artsen te helpen bij het identificeren en kwantificeren van progressie van het gezichtsveld. Gebeurtenisanalyse zoekt naar een statistisch significante verandering van een punt of groep van punten, terwijl trendanalyse de richting van verandering in de tijd kwantificeert, of de snelheid van verandering, met inbegrip van toekomstverwachtingen. Clinici kunnen hun aandacht richten op de mogelijke onderschatting van diffuus verlies, subtiele artefacten die geassocieerd kunnen worden met patroonafwijking en de noodzaak van een voldoende aantal hoogwaardige gezichtsvelden (minimaal vijf) voor een optimale analyse. De GPA wordt echter minder beïnvloed door cataract dan andere analyse-instrumenten. Elke teststrategie maakt gebruik van een eigen normatieve database.2 Een bijkomend doel is het identificeren van een progressiesnelheid en het scheiden van de patiënten die snel progressie vertonen en een steeds agressievere therapie nodig hebben.
Progressie van niet-glaucoomateuze Optische Neuropathieën
Omdat GPA specifiek voor glaucoombehandeling werd opgericht, moeten clinici een andere aanpak hanteren bij de evaluatie van mogelijke progressie bij niet-glaucoomateuze aandoeningen. Regressieanalyse van VFI of gemiddelde afwijking, evenals serie-overzichtsrapporten, kunnen nuttig zijn bij het evalueren van andere aandoeningen.2
Follow Up
Gebruik dezelfde teststrategie en hetzelfde testpatroon om gemakkelijker te kunnen vergelijken en te controleren op progressie. Het volgen van gevestigde glaucoompatiënten met perimetrie is essentieel om te bepalen of de huidige behandeling adequaat is of dat veranderingen in de behandeling nodig zijn op basis van de stabiliteit of progressie van het gezichtsveld.
De frequentie van de follow-up zal afhangen van de omvang van de ziekte en het klinische beloop. Patiënten die stabiliteit vertonen kunnen redelijkerwijs hun follow-up interval verhogen.
Artifacten
Er zijn verschillende artefacten die kunnen optreden, waardoor verdere uitdagingen bij de interpretatie van visuele velden. Clinici moeten onderscheid maken tussen echte gezichtsvelddefecten van pathologie die correleren met het klinische beeld en artefacten die zich kunnen voordoen. Op momenten dat het niet duidelijk is of het gezichtsvelddefect echt is of een artefact, moet het gezichtsveld worden herhaald in een geschikte tijdlijn op basis van uw niveau van verdenking en het klinische beeld. Artefacten om op te letten zijn:
– Ooglid en wenkbrauw ptosis. Dit kan een dicht superieur defect veroorzaken langs de superieure randpunten. Patiënten met visueel significante ptosis kunnen er baat bij hebben hun oogleden te laten tapen voor het testen.
– Rand artefacten. De plaatsing van de houder van de testlens kan leiden tot een randartefact als deze te ver van het oog van de patiënt is geplaatst, waardoor een volledig of gedeeltelijk ringscotoma ontstaat.
– Onjuiste refractiefout. Dit kan leiden tot een veralgemeende depressie in gevoeligheid die die van cataract kan nabootsen. Een hoge refractieafwijking kan een vergrotings- of verkleiningseffect veroorzaken en vereist een juiste berekening van de vertexafstand. Het gebruik van het verkeerde lenssterkteteken of het niet gebruiken van de nieuwe refractiefout nadat een patiënt een cataractoperatie heeft ondergaan, zijn twee veel voorkomende fouten.
– Vermoeidheid van de patiënt. Dit kan zich uiten in langere testtijden, hoge fout-negatieve waarde of bij voorkeur abnormale perifere gevoeligheid. Perifere punten worden later in het verloop van de test getest en kunnen bij vermoeidheid of verslapping van de aandacht duidelijk verminderd zijn, wat resulteert in een donkerder, lobulaire ring of klaverbladpatroon op de grijsschaal.
Er bestaat een leercurve voor zowel patiënten als degenen die de test uitvoeren. Bewustwording van deze veel voorkomende artefacten maakt een betere visuele veldinterpretatie mogelijk en erkenning van beperkingen van de betrouwbaarheid en kwaliteit van testresultaten.
Waarom testen we
Inzicht in de visuele pathway kan een zorgverlener waardevol inzicht geven in het lokaliseren van laesies. Elke praktijk moet een voorkeurteststrategie en -patroon standaardiseren en dezelfde test herhalen bij follow-upbezoeken om nauwkeurigere vergelijkingen mogelijk te maken tijdens follow-uponderzoek.18
Glaucoombeheer moet gericht zijn op het voorkomen van verlies van gezichtsvelden in de mate dat het de kwaliteit van leven van een patiënt beïnvloedt. Het is belangrijk om het gehele klinische beeld te evalueren om er zeker van te zijn dat variabelen correleren en samenvallen. Tests moeten worden herhaald als er onzekerheid bestaat om betrouwbaardere nulmetingen vast te stellen en mogelijke progressie te bevestigen.
1. Lens A, Langley T, Nemeth SC, Shea C. Visuele paden. In: Anatomie en fysiologie van de oogbol. Thorofare, NJ: SLACK; 1999:90-5.
2. Heijl A, Patella VM, Bengtsson B. The Field Analyzer Primer: Effective Perimetry. 4e ed. Carl Zeiss Meditec; 2012.
3. Park HY, Hwang BE, Shin HY, Park CK. Clinical clues to predict the presence of parafoveal scotoma on Humphrey 10-2 visual field using a Humphrey 24-2 visual field. Am J Ophthalmol. 2016;161:150-9.
4. Ehrlich AC, Raza AS, Ritch R, et al. Modifying the conventional visual field test pattern to improve the detection of early glaucomatous defects in the central 10°. Transl Vis Sci Technol. 2014 Oct;3(6):6.
5. Kedar S, Ghate D, Corbett JJ. Visual Fields in Neuro-Ophthalmology. Indian Journal of Ophthalmology. 2011;59(2):103-9.
6. Wall M, George D. Idiopathic intracranial hypertension. Een prospectieve studie van 50 patiënten. Brain. 1991;114:155-80.
7. Keltner JL, Johnson CA, Spurr JO, Beck RW. Baseline gezichtsveld profiel van optische neuritis. De ervaring van de optic neuritis treatment trial. Optic Neuritis Studie Groep. Arch Ophthalmol. 1993;111:231-4.
8. Hayreh SS, Zimmerman B. Visual field abnormalities in nonarteritic anterior ischemic optic neuropathy: their pattern and prevalence at initial examination. Arch Ophthalmol. 2005;123:1554-62.
9. Hayreh SS. Posterior ischaemic optic neuropathy: clinical features, pathogenesis, and management. Eye (Lond). 2004;18:1188–206.
10. Bengtsson B. Prediction of glaucomatous visual field loss by extrapolation of linear trends. Arch Ophthalmol. 2009;127(12):1610-5.
11. Heijl A. Reduction of intraocular pressure and glaucoma progression. Arch Ophthalmol. 2002;120(10):1268-79.
12. Willmore LJ, Abelson MB, Ben-Menachem E, et al. Vigabatrin: 2008 update. Epilepsia. 2009;50:163–73.
13. Katz J, Sommer A, Gaasterland DE, Anderson DR. A comparison of analytic algorithms for detecting glaucomatous visual field loss. Arch Ophthalmol. 1991;109(12):1017-25.
14. Hodapp E, Parrish RK II, Anderson DR. Klinische beslissingen bij glaucoom. St. Louis: The CV Mosby Co;1993:52-61.
15. Feuer WJ, Anderson DR. Static threshold asymmetry in early glaucomatous visual field loss. Ophthalmology. 1989;96:1285-97.
16. Brenton RS, Phelps CD, Rojas P, Woolson RF. Interocular differences of the visual field in normal subjects. Invest Ophthalmol Vis Sci. 1986;27:799-805.
17. Anderson DR, Chauhan B, Johnson C, et al. Criteria voor progressie van glaucoom in klinisch management en in uitkomststudies. Am J Ophthalmol. 2000;130(6):827-29.
18. Weinreb RN. Progressie van Glaucoom: The 8th Consensus Report of the World Glaucoma Association. Amsterdam: Kugler Publications; 2011.