US Pharm. 2014;39(3):HS2-HS8.
ABSTRACT : La toxicité de l’acétaminophène est l’une des causes les plus courantes d’empoisonnement intentionnel et non intentionnel aux États-Unis. Elle est devenue la cause la plus courante d’insuffisance hépatique aiguë et la deuxième cause la plus fréquente d’insuffisance hépatique nécessitant une transplantation. L’acétaminophène est souvent recommandé par les médecins et très utilisé par les patients dans les produits sur ordonnance et en vente libre pour une variété d’affections. La FDA a depuis longtemps mis à jour ses recommandations concernant l’utilisation de l’acétaminophène afin d’améliorer la sécurité des patients. Cet article passe en revue l’étiologie, les signes et les symptômes de la toxicité de l’acétaminophène et le rôle du pharmacien dans la prévention du mésusage de l’acétaminophène.
L’acétaminophène est souvent recommandé par les médecins et hautement utilisé par les patients dans les produits sur ordonnance et en vente libre pour une variété d’affections, ce qui en fait sans aucun doute l’un des médicaments les plus couramment rencontrés par les pharmaciens1-3. Aux États-Unis, 40 % de la population adulte a déclaré utiliser de l’acétaminophène en vente libre tous les mois, et 23 % de la population adulte a déclaré utiliser de l’acétaminophène en vente libre ou sur ordonnance toutes les semaines.1,2
L’acétaminophène (paracétamol ou APAP) a des propriétés analgésiques et antipyrétiques similaires à celles de l’aspirine, mais des propriétés anti-inflammatoires minimes.4 Il est indiqué pour les douleurs ou la fièvre légères à modérées, et il n’est pas associé à des malaises ou des saignements d’estomac aux doses recommandées. Lorsqu’il est utilisé de manière appropriée, il présente un profil d’innocuité et d’efficacité très bien établi.5 Cependant, l’hépatotoxicité est une conséquence fréquente de la surconsommation, qui peut entraîner toute une série de problèmes, notamment des anomalies de la fonction hépatique, une insuffisance hépatique aiguë et même la mort6.
La toxicité de l’acétaminophène est l’une des causes les plus courantes d’empoisonnement intentionnel et non intentionnel aux États-Unis. En fait, on a constaté une augmentation constante de l’incidence de la toxicité liée à l’acétaminophène au cours de la dernière décennie.7,8 Cela est probablement attribué à la disponibilité généralisée de l’acétaminophène à la fois comme ingrédient unique et en combinaison avec d’autres médicaments en vente libre et sur ordonnance dans diverses concentrations et formulations. Les surdoses associées à l’acétaminophène sont à l’origine d’environ 56 000 visites au service des urgences, de 26 000 hospitalisations et de plus de 450 décès par an.9 La toxicité hépatique induite par l’acétaminophène est devenue la cause la plus fréquente d’insuffisance hépatique aiguë et la deuxième cause la plus fréquente d’insuffisance hépatique nécessitant une transplantation.10,11 Par conséquent, il est impératif que les pharmaciens reconnaissent les signes et les symptômes de surdosage et de toxicité, et qu’ils conseillent leurs patients sur la posologie et l’utilisation appropriées.
Pharmacocinétique
Après ingestion, l’acétaminophène est rapidement absorbé par le tractus gastro-intestinal (GI) et rapidement distribué dans tout le corps. Les concentrations plasmatiques maximales sont atteintes dans un délai de 30 à 60 minutes4 ; la nourriture peut retarder le délai d’obtention de la concentration maximale, mais l’étendue de l’absorption n’est pas affectée.12 En cas de surdosage, les concentrations plasmatiques maximales sont généralement atteintes dans un délai de 4 heures13. La demi-vie de l’acétaminophène est d’environ 2 à 3 heures après l’administration de doses thérapeutiques, mais elle peut être portée à plus de 4 heures chez les patients présentant une atteinte hépatique.4,12,14
L’acétaminophène est largement métabolisé par le foie par l’intermédiaire de trois voies hépatiques principales : la glucuronidation, la sulfatation et l’oxydation par le CYP450 2E1.12 Environ 90 % de l’acétaminophène est conjugué en métabolites sulfatés et glucuronidés qui sont éliminés par voie rénale14. Sur le reste de l’acétaminophène, environ 2 % sont excrétés sous forme inchangée dans l’urine et le reste subit une oxydation médiée par le CYP450 pour former un métabolite réactif, la N-acétyl-p-benzoquinone imine (NAPQI).15-18 Dans des circonstances normales, ce métabolite toxique réagit avec les groupes sulfhydryles du glutathion, le convertissant en métabolites inoffensifs avant d’être excrété dans l’urine4.
Toxicité
Les médicaments peuvent avoir des effets toxiques pour diverses raisons. La toxicité de certains médicaments est liée à la formation d’un métabolite indésirable ; par conséquent, la toxicité de l’acétaminophène est liée à la production de NAPQI. En cas de doses aiguës importantes ou d’utilisation chronique, les principales voies métaboliques – les systèmes de conjugaison glucuronide et sulfate – deviennent saturées, et une plus grande quantité d’acétaminophène est métabolisée par le système CYP450. Il en résulte une production accrue de NAPQI. Lorsque le glutathion est épuisé à environ 70 %, le NAPQI commence à s’accumuler dans les hépatocytes, ce qui entraîne des lésions hépatiques.15,16,18 Par conséquent, le remplacement du glutathion par des composés imitant le glutathion, comme la N-acétylcystéine, sert d’antidote utile à la toxicité de l’acétaminophène.
La toxicité de l’acétaminophène peut résulter d’un surdosage aigu ou d’une surconsommation chronique. Le surdosage aigu est défini comme la consommation d’une quantité toxique d’un médicament dans une période de 8 heures, tandis que le surdosage chronique survient à la suite de doses répétées égales ou supérieures à la limite recommandée.12 Des surdoses involontaires peuvent également survenir à la suite de l’ingestion de plusieurs produits contenant de l’acétaminophène. La dose recommandée d’acétaminophène chez les adultes est de 650 à 1 000 mg toutes les 4 à 6 heures, sans dépasser 4 000 mg par période de 24 heures ; chez les enfants, la dose recommandée est de 10 à 15 mg/kg toutes les 4 à 6 heures, sans dépasser 50 à 70 mg/kg par 24 heures.12 Des doses uniques de plus de 150 mg/kg ou 7,5 g chez les adultes ont été considérées comme potentiellement toxiques, bien que la dose minimale associée à des lésions hépatiques puisse varier entre 4 et 10 g.6,12,14,19 Chez les enfants, des doses uniques de 120 mg/kg à 150 mg/kg ont été associées à une hépatotoxicité ; cependant, des doses <200 mg/kg sont peu susceptibles d’entraîner une toxicité.14,20
Bien que la dose maximale exacte n’ait pas été bien définie, l’American Association of Poison Control Centers (AAPCC) a recommandé que, quelle que soit la quantité de médicament ingérée, un patient soit amené pour une évaluation médicale s’il présente des signes ou des symptômes correspondant à une toxicité.21 L’AAPCC a fourni des lignes directrices pour l’orientation vers un hôpital à la fois pour une ingestion aiguë, unique et non intentionnelle d’acétaminophène et pour une ingestion suprathérapeutique répétée d’acétaminophène (TABLEAU 1).21
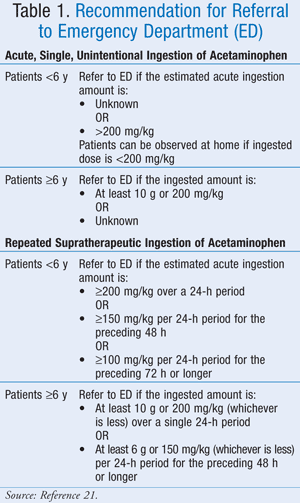
Présentation clinique
Que la toxicité de l’acétaminophène survienne en raison d’une surdose unique ou après une ingestion suprathérapeutique répétée, la progression de l’empoisonnement à l’acétaminophène peut être décrite en quatre phases séquentielles : effets toxiques précliniques (phase un), lésion hépatique (phase deux), insuffisance hépatique (phase trois) et rétablissement (phase quatre).6,22 Les patients traités pendant la phase préclinique peuvent développer des lésions hépatiques transitoires mais se rétablir complètement22. Les patients qui ne sont pas traités avant que les lésions hépatiques ne soient déjà évidentes ont un pronostic variable ; cependant, ceux qui présentent une insuffisance hépatique ont un taux de mortalité de 20 à 40 %.22
La première phase se produit quelques heures après l’ingestion d’une dose toxique et dure de 12 à 24 heures. Il est important de noter le retard dans l’apparition des symptômes, car les prestataires de soins de santé doivent comprendre les implications de la toxicité qui suivra cette période de quiescence. Les symptômes au cours des 24 premières heures ne sont pas diagnostiques ou spécifiques et comprennent les nausées, les vomissements, la diaphorèse, l’anorexie et la léthargie, dont la gravité sera en corrélation directe avec l’importance de la dose ingérée8.
Dans la deuxième phase, survenant jusqu’à 24 à 48 heures après l’ingestion, il peut y avoir un faux sentiment de rétablissement alors que les symptômes gastro-intestinaux s’améliorent ou disparaissent.6,8 Cependant, à mesure que l’hépatotoxicité continue d’apparaître, des douleurs abdominales ou une sensibilité du quadrant supérieur droit peuvent faire surface. De plus, les valeurs de laboratoire commenceront à montrer des signes d’hépatotoxicité ; les enzymes hépatiques, le lactate, le phosphate, le temps de prothrombine et le rapport international normalisé (RIN) augmenteront de façon spectaculaire.6,8,12 La plupart des patients ne dépassent pas ce stade, surtout si l’antidote acétylcystéine est administré.8,12
Un petit nombre de patients passeront à la troisième phase, qui survient habituellement de 3 à 5 jours après l’ingestion. Cette phase se caractérise par la réapparition ou l’aggravation des nausées et des vomissements accompagnés d’un malaise, d’un ictère et de symptômes nerveux centraux, notamment la confusion, la somnolence et le coma.6 Une nécrose hépatique grave, voire mortelle, peut survenir. Bien que moins fréquente, l’insuffisance rénale, démontrée par une oligurie, peut se manifester à la suite d’une nécrose tubulaire induite par l’acétaminophène.6,8,12 Les taux d’enzymes hépatiques atteindront leur maximum, mesurant jusqu’à 10 000 UI/L. La jaunisse, l’hypoglycémie, les anomalies de l’hémorragie et de la coagulation et l’encéphalopathie hépatique seront également évidentes.8,12 La mort peut survenir à la suite de complications associées à l’insuffisance hépatique, y compris la défaillance de plusieurs organes, l’œdème cérébral et la septicémie.15
Enfin, la phase quatre implique la survie et le rétablissement, généralement avec le retour d’une fonction hépatique complète et sans effets à long terme.6 Environ 70 % des patients qui entrent dans la phase quatre se rétablissent complètement, tandis que 1 à 2 % des patients développent une insuffisance hépatique fatale.6 Une toxicité sévère et non traitée à l’acétaminophène entraînera la mort dans les 4 à 18 jours suivant l’ingestion.6
Patients à risque accru
Parce que le mécanisme de toxicité de l’acétaminophène se produit via la formation de NAPQI, tout facteur qui influence la disponibilité des enzymes métaboliques affectera donc la toxicité. La consommation d’alcool, la malnutrition et l’induction des enzymes du CYP450 par des médicaments, y compris le traitement à long terme par la carbamazépine, la primidone, la rifampine, l’éfavirenz et le millepertuis, peuvent avoir un impact sur la façon dont une personne réagit à l’acétaminophène23. Les patients affectés par l’un des facteurs ci-dessus doivent être identifiés afin que les pharmaciens puissent les conseiller étroitement sur la manière d’utiliser l’acétaminophène en toute sécurité.
Acuité, l’éthanol sert à la fois de substrat et d’inhibiteur du CYP2E1, limitant la quantité de NAPQI formée. A l’inverse, en cas de consommation chronique d’alcool, l’éthanol est un inducteur du CYP2E1, entraînant une augmentation potentielle de la formation de NAPQI en cas de surdosage en acétaminophène. Une autre conséquence de la consommation chronique d’alcool est l’épuisement des réserves de glutathion, réduisant ainsi la dernière défense contre la formation de NAPQI.17 Il n’existe aucune preuve suggérant que l’utilisation d’acétaminophène à des doses thérapeutiques est toxique chez une personne alcoolique ; par conséquent, en quantités thérapeutiques, l’acétaminophène peut être utilisé en toute sécurité à la fois de manière aiguë et chronique23-25.
Bien que controversés, la famine (jeûne prolongé) et la malnutrition sont des facteurs de risque supplémentaires de toxicité de l’acétaminophène.16,18,23 Comme pour la consommation chronique d’alcool, la malnutrition entraîne un épuisement des réserves de glutathion. Cependant, il existe également des preuves que la fonction du CYP2E1 est nettement réduite dans cette population de patients. Ces effets se neutraliseraient donc mutuellement, ce qui pourrait n’entraîner aucune modification de la toxicité.26 Néanmoins, il est toujours prudent d’identifier ces patients et de les avertir de leur potentiel de risque accru.
Prise en charge
Lors de la présentation, le patient doit être évalué de manière approfondie. Un historique détaillé des médicaments récents doit être obtenu. Les taux sériques d’acétaminophène doivent idéalement être prélevés au moins 4 heures après l’ingestion. Les pharmaciens peuvent jouer un rôle important en recueillant des informations pertinentes telles que la quantité de médicament prise, la forme posologique ingérée, le temps écoulé depuis la dernière dose ingérée et si d’autres médicaments ont été consommés. Tous ces facteurs sont importants lors de l’analyse des concentrations sériques d’acétaminophène.
Si le patient se présente dans l’heure qui suit l’ingestion, une décontamination gastrique peut être envisagée ; le charbon actif est la seule méthode de décontamination GI recommandée. L’administration de charbon actif peut être envisagée, en particulier chez les patients qui ont ingéré des formulations à libération retardée d’acétaminophène ou qui ont consommé d’autres médicaments qui ralentiraient l’absorption de l’acétaminophène.12 Cependant, en raison de la rapidité des phases d’absorption et de distribution de l’acétaminophène, cette méthode n’a par ailleurs que peu d’utilité au fil du temps.27-29 Le charbon actif ne doit être administré que si le patient est mentalement alerte et que ses voies respiratoires sont intactes. Il doit également être évité chez les personnes présentant un risque accru d’aspiration, de vomissements incontrôlés ou de coingestion d’un corrosif ou d’un proconvulsivant.30
Acétylcystéine : Le pilier du traitement de la toxicité de l’acétaminophène est l’acétylcystéine. Cet agent reconstitue les réserves hépatiques de glutathion et augmente la conjugaison des sulfates, empêchant ainsi l’accumulation de NAPQI.31 L’acétylcystéine peut être bénéfique chez les patients présentant une insuffisance hépatique induite par l’acétaminophène, car elle améliore l’hémodynamique et l’utilisation de l’oxygène, diminue l’œdème cérébral et améliore la production d’énergie mitochondriale14,22.
L’acétylcystéine peut prévenir l’insuffisance hépatique due à une surdose d’acétaminophène lorsqu’elle est administrée suffisamment tôt (dans les 8 à 10 heures suivant une surdose aiguë), mais elle peut encore être utile jusqu’à 48 heures après l’ingestion.6,11,14,31 Le nomogramme standard de toxicité de l’acétaminophène, le nomogramme de Rumack-Matthew, peut être utilisé pour déterminer la probabilité d’une atteinte hépatique grave. Cependant, il est rendu inefficace lorsqu’il s’agit d’évaluer une éventuelle toxicité due à de multiples ingestions dans le temps, lorsque le moment de l’ingestion est inconnu ou lorsqu’une altération du métabolisme se produit.Compte tenu de ces éléments, l’acétylcystéine doit être administrée dans tous les cas d’insuffisance hépatique aiguë ou lorsqu’il y a des signes de toxicité hépatique dans lesquels on soupçonne un surdosage d’acétaminophène.11
L’acétylcystéine est disponible par voie orale et intraveineuse ; le choix dépend du scénario clinique.21 L’administration par voie orale peut être bénéfique pour les patients présentant des effets toxiques précliniques ou des lésions hépatiques, bien que la présence d’une altération de l’état mental et de vomissements puisse limiter son utilisation22. Le schéma posologique de l’acétylcystéine orale est une dose de charge de 140 mg/kg, suivie de 17 doses de 70 mg/kg toutes les 4 heures pendant un total de 72 heures.11 Les patients souffrant d’insuffisance hépatique doivent recevoir un traitement IV.22 La perfusion IV continue est recommandée à raison d’une dose d’attaque de 150 mg/kg IV dans 200 ml de D5W en 60 minutes, suivie d’une dose d’entretien de 50 mg/kg en 4 heures, puis d’une seconde dose d’entretien de 100 mg/kg dans 1 000 ml de D5W administrée en 16 heures.11 Si le patient pèse moins de 40 kg, il convient d’ajuster l’apport liquidien conformément aux directives pour éviter la surcharge liquidienne, l’hyponatrémie et les convulsions. Si le patient se porte bien mais ne s’est pas complètement rétabli après l’administration de la dose recommandée, le traitement à l’acétylcystéine peut être poursuivi en utilisant soit la dernière dose orale, soit le dernier débit de perfusion IV. L’acétylcystéine doit être poursuivie au-delà de la durée du protocole jusqu’à ce que les concentrations d’acétaminophène soient indétectables, que le taux sérique d’ASAT se soit normalisé ou considérablement amélioré et que tout signe d’insuffisance hépatique ait disparu.13
En raison de son goût et de son odeur désagréables, des vomissements surviennent fréquemment lors de l’administration d’acétylcystéine par voie orale.31,32 Les effets indésirables associés à l’acétylcystéine IV comprennent des réactions anaphylactoïdes, notamment des éruptions cutanées, un prurit, un œdème de Quincke, un bronchospasme, une tachycardie et une hyper-tension.31,32 En outre, lors de l’utilisation de l’acétylcystéine IV, les pharmaciens doivent être conscients du risque d’erreurs médicamenteuses. Le régime complexe, la durée du traitement et la nécessité pour plusieurs professionnels de la santé d’administrer des doses à différents sites de traitement augmentent considérablement le risque d’erreurs.33 Une étude rétrospective a identifié une incidence de 33 % d’erreurs de médication avec l’acétylcystéine IV.33 Le type d’erreur le plus courant trouvé dans cette étude était un retard dans le traitement, ce qui peut potentiellement réduire l’efficacité de l’acétylcystéine. Une autre erreur courante identifiée était l’administration inutile d’acétylcystéine, entraînant des coûts inutiles. Il est important que les prestataires de soins de santé consultent les centres antipoison en cas de surdose d’acétaminophène. Ils peuvent fournir les informations et les protocoles de dosage les plus à jour pour assurer une administration correcte de l’acétylcystéine.
Étiquetage de la FDA
Dans l’espoir d’accroître la sécurité et de réduire la toxicité, la FDA met depuis longtemps à jour ses recommandations concernant l’utilisation de l’acétaminophène. À la fin des années 1990, des recherches ont démontré que l’acétaminophène était l’une des principales causes d’insuffisance hépatique aiguë aux États-Unis, la majorité des cas ayant résulté de surdoses accidentelles.34 En 1998, la FDA a publié une étiquette d’avertissement sur les produits à base d’acétaminophène qui invitait les patients consommant plus de trois boissons alcoolisées par jour à consulter un médecin avant d’utiliser ce médicament. Les années passant et la corrélation entre l’acétaminophène et la toxicité hépatique devenant encore plus évidente, la FDA a convoqué une réunion pour donner suite à ces conclusions. En 2002, le comité consultatif de la FDA a recommandé qu’une mise en garde contre la toxicité hépatique soit apposée sur tous les produits contenant de l’acétaminophène. En 2009, un nouvel étiquetage a été mis au point pour aider les patients à identifier facilement les produits contenant de l’acétaminophène, réduisant ainsi le risque de surdosage accidentel. Un avertissement de boîte noire a ensuite été placé sur tous les produits d’acétaminophène sur ordonnance, soulignant le risque potentiel de lésions hépatiques graves, et un avertissement concernant l’anaphylaxie rare mais grave et d’autres réactions d’hypersensibilité a été mis en œuvre34.
En août 2013, la FDA a alerté les consommateurs sur des réactions cutanées rares mais graves et potentiellement mortelles, telles que le syndrome de Stevens-Johnson (SJS), la nécrolyse épidermique toxique (TEN) et la pustulose exanthématique aiguë généralisée (PEAG), liées à la prise d’acétaminophène35. Les patients doivent être conseillés sur les signes et symptômes de réactions cutanées, tels que la desquamation, la formation de cloques, le rougissement et le décollement de la peau, dans lesquels ils doivent cesser toute autre utilisation du médicament et consulter immédiatement un médecin.
La FDA a également annoncé qu’à partir de janvier 2014, la quantité d’acétaminophène présente dans les produits combinés sur ordonnance doit être limitée à 325 mg par comprimé ou capsule36,37. En mai 2011, les fabricants de produits d’acétaminophène en vente libre ont volontairement annoncé qu’une seule concentration d’acétaminophène liquide pour enfants (160 mg/5 mL) sera la seule disponible ; les gouttes concentrées pour nourrissons ne seront plus produites.38
Bien que des progrès aient été réalisés, certaines choses restent à déterminer. Le comité consultatif de la FDA a voté en faveur de nombreux changements censés améliorer la sécurité et diminuer la toxicité, mais la FDA n’a pas encore pris de mesures. Par exemple, alors que la dose quotidienne maximale d’acétaminophène était auparavant fixée à 4 g/jour, le comité consultatif de la FDA suggère de la diminuer dans le but de réduire les surdoses.37 Il est important de noter que certains fabricants ont déjà mis à jour leur étiquetage pour refléter ces recommandations, bien que cela ne soit pas encore obligatoire. Des efforts sont également déployés pour améliorer l’étiquetage des produits, renforcer l’éducation des patients, créer une formulation pédiatrique universelle, éliminer les produits combinés à base d’acétaminophène et réduire la concentration des produits d’acétaminophène en vente libre à 325 mg par comprimé, avec une dose unique maximale de 650 mg37. Bien qu’aucun consensus final n’ait été atteint sur l’une ou l’autre de ces questions, les fournisseurs de soins de santé devraient éduquer leurs patients sur l’importance de suivre les instructions de l’étiquetage.
Rôle du pharmacien
Les pharmaciens sont en mesure de promouvoir efficacement l’utilisation sécuritaire de l’acétaminophène. De nombreux patients ne connaissent pas la dose quotidienne maximale d’acétaminophène et le potentiel de toxicité.39 En outre, les patients peuvent ne pas comprendre que l’acétaminophène est contenu dans plus de 600 produits différents.39 Tous les patients recevant une ordonnance pour un produit contenant de l’acétaminophène doivent être conseillés pour s’assurer qu’ils connaissent l’ingrédient actif. Les pharmaciens doivent jouer un rôle proactif dans l’éducation des patients qui achètent des produits en vente libre contenant de l’acétaminophène. Les pharmaciens jouent un rôle essentiel dans la prévention de l’abus d’acétaminophène en garantissant une utilisation sûre du médicament par l’éducation des patients et l’examen des antécédents de médication des patients.
En outre, les pharmaciens doivent recommander aux patients de contacter la ligne nationale d’aide antipoison s’ils soupçonnent une surdose d’acétaminophène. Le numéro gratuit est le 1-800-222-1222.40 En appelant ce numéro, les patients seront mis en relation avec le centre antipoison régional le plus proche dont les spécialistes sont disponibles 24 heures sur 24, 7 jours sur 7. Ces spécialistes seront en mesure d’aider à évaluer et à gérer la surdose potentielle d’acétaminophène. Ces activités minimiseront le risque de dosage inapproprié, de duplication de la thérapie et d’utilisation inappropriée des médicaments.
1. Kaufman DW, Kelly JP, Rosenberg L, et al. Recent patterns of medication use in the ambulatory adult population of the United States : the Slone survey. JAMA. 2002;287:337-344.
2 Paulose-Ram R, Hirsch R, Dillon C, et al. Prescription and nonprescription analgesic use among the US adult population : results from the third National Health and Nutrition Examination Survey (NHANES III). Pharmacoepidemiol Drug Saf. 2003;12:315-326.
3. Paulose-Ram R, Hirsch R, Dillon C, et al. Frequent monthly use of selected nonprescription and prescription non-narcotic analgesics among U.S. adults. Pharmacoepidemiol Drug Saf. 2005;14:257-266.
4. Burke A, Smyth EM, Fitzgerald GA. Agents analgésiques-antipyrétiques ; pharmacothérapie de la goutte. In : Brunton LL, Laso JS, Parker K, eds. Goodman and Gilman’s the Pharmacological Basis of Therapeutics. 11th ed. New York, NY : McGraw-Hill; 2006:671-716.
5. Watkins PB, Kaplowitz N, Slattery JT, et al. Amino-transferase elevations in healthy adults receiving 4 grams of acetaminophen daily : a randomized controlled trial. JAMA. 2006;296:87-93.
6. Chun LJ, Tong MJ, Busuttil RW, et al. Acetaminophen hepatotoxicity and acute liver failure. J Clin Gastroenterol. 2009;43:342-349.
7. Bronstein AC, Spyker DA, Cantilena LR, et al. Rapport annuel 2011 du système national de données sur les poisons (NPDS) de l’American Association of Poison Control Centers : 29e rapport annuel. Clin Toxicol. 2012;50:911-1164.
8. Schilling A, Corey R, Leonard M, et al. Acétaminophène : ancien médicament, nouveaux avertissements. Cleve Clin J Med. 2010;77:19-27.
9. Nourjah P, Ahmad SR, Karwoski C, et al. Estimations des surdoses d’acétaminophène (paracétamol) associées aux États-Unis. Pharmacoepidemiol Drug Saf. 2006;15:398-405.
10. Larson AM, Polson J, Fontana RJ, et al. Acetaminophen-induced acute liver failure : results of a United States multicenter, prospective study. Hépatologie. 2005;42:1364-1372.
11. Lee WM, Larson AM, Stravitz T. AASLD position paper : the management of acute liver failure : update 2011. Baltimore, MD : Association américaine pour l’étude des maladies du foie ; septembre 2011. www.aasld.org/practiceguidelines/Documents/AcuteLiverFailureUpdate2011.pdf. Consulté le 15 décembre 2013.
12. Information professionnelle sur le produit Tylenol (acétaminophène). Fort Washington, PA : McNeil Consumer Healthcare ; 2010.
13. Hendrickson RG. Acetaminophen. In : Nelson LS, Lewin NA, Howland M, eds. Goldfrank’s Toxicologic Emergencies. 9th ed. New York, NY : McGraw-Hill; 2011:483-99.
14. Hodgman MJ, Garrard AR. Une revue de l’empoisonnement à l’acétaminophène. Crit Care Clin. 2012;499-516.
15. Larson AM. L’hépatotoxicité de l’acétaminophène. Clin Liver Dis. 2007;11:525-548.
16. Rumack BH. Hépatotoxicité de l’acétaminophène : les 35 premières années. J Toxicol Clin Toxicol. 2002;40:3-20.
17. Nelson SD. Mécanismes moléculaires de l’hépatotoxicité causée par l’acétaminophène. Semin Liver Dis. 1990;10:267-278.
18. Lee WH. Hépatotoxicité induite par les médicaments. N Engl J Med. 1995;333:1118-1127.
19. Fontana RJ. Insuffisance hépatique aiguë incluant une surdose d’acétaminophène. Med Clin North Am. 2008;92:761-794.
20. Comité des médicaments de l’Académie américaine de pédiatrie. Toxicité de l’acétaminophène chez les enfants. Pediatrics. 2001;108:1020-1024.
21. Dart RC, Erdman AR, Olson KR, et al. Empoisonnement à l’acétaminophène : une directive de consensus fondée sur des preuves pour la gestion extra-hospitalière. Clin Toxicol. 2006;44:1-18.
22. Heard KJ. L’acétylcystéine pour l’empoisonnement à l’acétaminophène. N Engl J Med. 2008;359:285-292.
23. Ferner RE, Dear JW, Bateman DN. Gestion de l’empoisonnement au paracétamol. BMJ. 2011;342:d2218.
24. Kuffner EK, Dart RC, Bogdan GM, et al. Effet des doses quotidiennes maximales d’acétaminophène sur le foie des patients alcooliques : un essai randomisé, en double aveugle, contrôlé par placebo. Arch Intern Med. 2001;161:2247-2252.
25. Kuffner EK, Green JL, Bogdan GM, et al. The effect of acetaminophen (quatre grammes par jour pendant trois jours consécutifs) on hepatic tests in alcoholic patients-a multicenter randomized study. BMC Med. 2007;5:13.
26. Rumack BH. Idées fausses sur l’acétaminophène. Hepatology. 2004;40:10-15.
27. Christophersen AB, Levin D, Hoegberg LC, et al. Charbon actif seul ou après lavage gastrique : une simulation de grande intoxication au paracétamol. Br J Clin Pharmacol. 2002;53;312-317.
28. Sato RL, Wong JJ, Sumida SM, et al. Efficacité de l’administration de charbon super-activé tard (3 heures) après une overdose d’acétaminophène. Am J Emerg Med. 2003;21:189-191.
29. Spiller HA, Winter ML, Klein-Schwartz W, et al. Efficacité du charbon actif administré plus de quatre heures après une surdose d’acétaminophène. J Emerg Med. 2006;30:1-5.
30. Chyka PA, Seger D, Krenzelok EP, et al. Position paper : single-dose activated charcoal. Clin Toxicol. 2005;43:61-87.
31. Kozer E, Koren G. Management of paracetamol overdose : current controversies. Sécurité des médicaments. 2001;24:503-512.
32. Sandilands EA, Bateman DN. Effets indésirables associés à l’acétylcystéine. Clin Toxicol. 2009;47:81-88.
33. Hayes BD, Klein-Schwartz W, Doyon S. Frequency of medication errors with intravenous acetylcysteine for acetaminophen overdose. Ann Pharmacother. 2008;42:766-770.
34. 29-30 juin 2009 : Réunion conjointe du Comité consultatif sur la sécurité des médicaments et la gestion des risques avec le Comité consultatif sur les médicaments d’anesthésie et de réanimation et le Comité consultatif sur les médicaments en vente libre : Document d’information de la FDA. Mis à jour le 30 juillet 2013. www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/Drugs/DrugSafetyandRiskManagementAdvisoryCommittee/UCM164897.pdf. Consulté le 15 décembre 2013.
35. Communication sur la sécurité des médicaments de la FDA : La FDA met en garde contre des réactions cutanées rares mais graves avec l’acétaminophène, un analgésique/réducteur de fièvre. 1er août 2013. www.fda.gov/Drugs/DrugSafety/ucm363041.htm. Consulté le 16 décembre 2013.
36. Communication sur la sécurité des médicaments de la FDA : Les produits d’acétaminophène sur ordonnance seront limités à 325 mg par unité posologique ; l’avertissement encadré soulignera le potentiel d’insuffisance hépatique grave. 13 janvier 2011. www.fda.gov/Drugs/DrugSafety/ucm239821.htm. Consulté le 16 décembre 2013.
37. Krenzelok EP. Commentaire : la réunion du comité consultatif de la FDA sur l’acétaminophène. Quel est l’avenir de l’acétaminophène aux États-Unis ? Le point de vue d’un membre du comité. Clin Toxicol. 2009;47:784-789.
38. Pappas M, Bryan K. L’industrie des médicaments en vente libre annonce une transition volontaire vers une seule concentration de médicaments pédiatriques liquides à base d’acétaminophène à ingrédient unique. Produits de soins de santé grand public. 11 mai 2011. www.chpa.org/05_04_11_PedAcet.aspx. Consulté le 15 décembre 2013.
39. Hornsby LB, Whitley HP, Hester EK, et al. Enquête sur les connaissances des patients liées à la reconnaissance, au dosage et à la toxicité de l’acétaminophène. J Am Pharm Assoc. 2010;50:485-489.
40. Association américaine des centres antipoison. www.aapcc.org. Consulté le 25 février 2014.
.