US Pharm. 2014;39(3):HS2-HS8.
ABSTRACT: Paracetamol-Toxizität ist eine der häufigsten Ursachen für absichtliche und unbeabsichtigte Vergiftungen in den Vereinigten Staaten. Sie ist inzwischen die häufigste Ursache für akutes Leberversagen und die zweithäufigste Ursache für Leberversagen, das eine Transplantation erfordert. Paracetamol wird häufig von Ärzten empfohlen und von Patienten sowohl in verschreibungspflichtigen als auch in rezeptfreien Arzneimitteln für eine Vielzahl von Beschwerden verwendet. Die FDA aktualisiert seit langem ihre Empfehlungen zur Verwendung von Paracetamol, um die Sicherheit der Patienten zu verbessern. Dieser Artikel befasst sich mit der Ätiologie, den Anzeichen und Symptomen der Paracetamol-Toxizität und der Rolle des Apothekers bei der Verhinderung des Paracetamol-Missbrauchs.
Paracetamol wird häufig von Ärzten empfohlen und von Patienten sowohl in verschreibungspflichtigen als auch in rezeptfreien Produkten für eine Vielzahl von Erkrankungen verwendet, was es zweifellos zu einem der häufigsten Arzneimittel macht, mit denen Apotheker zu tun haben.1-3 In den Vereinigten Staaten gaben 40 % der erwachsenen Bevölkerung an, monatlich rezeptfreies Paracetamol zu verwenden, und 23 % der erwachsenen Bevölkerung gaben an, wöchentlich rezeptfreies oder verschreibungspflichtiges Paracetamol zu konsumieren.1,2
Acetaminophen (Paracetamol oder APAP) hat schmerzlindernde und fiebersenkende Eigenschaften, die denen von Aspirin ähneln, aber nur minimale entzündungshemmende Eigenschaften.4 Es ist für leichte bis mäßige Schmerzen oder Fieber indiziert und wird bei den empfohlenen Dosen nicht mit Magenbeschwerden oder Blutungen in Verbindung gebracht. Bei sachgemäßer Anwendung hat es ein sehr gut etabliertes Sicherheits- und Wirksamkeitsprofil.5 Hepatotoxizität ist jedoch eine häufige Folge eines übermäßigen Konsums, der zu einer Reihe von Problemen führen kann, einschließlich Störungen der Leberfunktion, akutem Leberversagen und sogar zum Tod.6
Die Paracetamol-Toxizität ist eine der häufigsten Ursachen für absichtliche und unabsichtliche Vergiftungen in den USA. Tatsächlich hat die Häufigkeit von Paracetamol-bedingter Toxizität in den letzten zehn Jahren stetig zugenommen.7,8 Dies ist wahrscheinlich auf die weit verbreitete Verfügbarkeit von Paracetamol sowohl als Einzelbestandteil als auch in Kombination mit anderen rezeptfreien und verschreibungspflichtigen Medikamenten in unterschiedlichen Konzentrationen und Formulierungen zurückzuführen. Paracetamol-bedingte Überdosierungen sind jährlich für etwa 56.000 Besuche in der Notaufnahme, 26.000 Krankenhausaufenthalte und mehr als 450 Todesfälle verantwortlich.9 Paracetamol-induzierte Lebertoxizität ist inzwischen die häufigste Ursache für akutes Leberversagen und die zweithäufigste Ursache für Leberversagen, das eine Transplantation erfordert.10,11 Daher ist es unerlässlich, dass Apotheker die Anzeichen und Symptome einer Überdosierung und Toxizität erkennen und ihre Patienten über die richtige Dosierung und Anwendung beraten.
Pharmakokinetik
Nach der Einnahme wird Paracetamol schnell aus dem Magen-Darm-Trakt absorbiert und schnell im Körper verteilt. Die maximalen Plasmakonzentrationen werden innerhalb von 30 bis 60 Minuten erreicht4; die Nahrungsaufnahme kann die Zeit bis zum Erreichen der maximalen Konzentration verzögern, das Ausmaß der Absorption wird jedoch nicht beeinflusst.12 Bei Überdosierungen werden die maximalen Plasmakonzentrationen in der Regel innerhalb von 4 Stunden erreicht.13 Die Halbwertszeit von Paracetamol beträgt nach therapeutischen Dosen etwa 2 bis 3 Stunden, kann sich jedoch bei Patienten mit Leberschäden auf mehr als 4 Stunden erhöhen.4,12,14
Acetaminophen wird von der Leber über drei Hauptwege umfassend metabolisiert: Glucuronidierung, Sulfatierung und CYP450 2E1-Oxidation.12 Etwa 90 % des Acetaminophens werden zu sulfatierten und glucuronidierten Metaboliten konjugiert, die über die Nieren ausgeschieden werden.14 Von dem verbleibenden Acetaminophen werden etwa 2 % unverändert im Urin ausgeschieden, der Rest unterliegt einer CYP450-vermittelten Oxidation zu einem reaktiven Metaboliten, dem N-Acetyl-p-Benzochinon-Imin (NAPQI).15-18 Unter normalen Umständen reagiert dieser toxische Metabolit mit Sulfhydrylgruppen im Glutathion und wandelt sich in harmlose Metaboliten um, bevor er im Urin ausgeschieden wird.4
Toxizität
Drogen können aus verschiedenen Gründen toxische Wirkungen haben. Die Toxizität einiger Arzneimittel hängt mit der Bildung eines unerwünschten Metaboliten zusammen; so ist die Toxizität von Paracetamol mit der Bildung von NAPQI verbunden. Bei hohen akuten Dosen oder bei chronischem Gebrauch werden die wichtigsten Stoffwechselwege – die Glucuronid- und Sulfatkonjugationssysteme – gesättigt, und mehr Paracetamol wird durch das CYP450-System metabolisiert. Dies führt zu einer erhöhten Produktion von NAPQI. Wenn Glutathion zu etwa 70 % verbraucht ist, beginnt sich NAPQI in den Hepatozyten anzusammeln, was zu Leberschäden führt.15,16,18 Daher dient der Ersatz von Glutathion durch Glutathion-ähnliche Verbindungen wie N-Acetylcystein als nützliches Gegenmittel bei Paracetamol-Toxizität.
Paracetamol-Toxizität kann entweder durch eine akute Überdosierung oder durch chronischen Übergebrauch entstehen. Eine akute Überdosierung ist definiert als die Einnahme einer toxischen Menge eines Arzneimittels innerhalb eines Zeitraums von 8 Stunden, während eine chronische Überdosierung durch wiederholte Einnahme von Dosen bei oder über dem empfohlenen Grenzwert entsteht.12 Unbeabsichtigte Überdosierungen können auch durch die Einnahme mehrerer Paracetamol-haltiger Produkte entstehen. Die empfohlene Dosis von Paracetamol liegt bei Erwachsenen bei 650 bis 1.000 mg alle 4 bis 6 Stunden, wobei 4.000 mg in einem Zeitraum von 24 Stunden nicht überschritten werden dürfen; bei Kindern liegt die empfohlene Dosis bei 10 bis 15 mg/kg alle 4 bis 6 Stunden, wobei 50 bis 70 mg/kg in 24 Stunden nicht überschritten werden dürfen.12 Einzeldosen von mehr als 150 mg/kg oder 7,5 g bei Erwachsenen wurden als potenziell toxisch angesehen, obwohl die minimale Dosis, die mit einer Leberschädigung einhergeht, zwischen 4 und 10 g liegen kann.6,12,14,19 Bei Kindern wurden Einzeldosen von 120 mg/kg bis 150 mg/kg mit Hepatotoxizität in Verbindung gebracht; es ist jedoch unwahrscheinlich, dass Dosen <200 mg/kg zu Toxizität führen.14,20
Während die genaue Höchstdosis nicht genau definiert wurde, hat die American Association of Poison Control Centers (AAPCC) empfohlen, dass ein Patient unabhängig von der Menge des eingenommenen Medikaments zur medizinischen Untersuchung gebracht werden sollte, wenn er oder sie Anzeichen oder Symptome zeigt, die auf eine Toxizität hinweisen.21 Die AAPCC hat Richtlinien für die Krankenhauseinweisung sowohl bei akuter, einmaliger, unbeabsichtigter Einnahme von Paracetamol als auch bei wiederholter supratherapeutischer Einnahme von Paracetamol aufgestellt (TABELLE 1).21
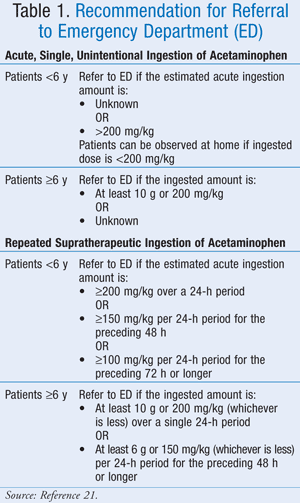
Klinische Darstellung
Unabhängig davon, ob die Paracetamol-Toxizität aufgrund einer einmaligen Überdosierung oder nach wiederholter supratherapeutischer Einnahme auftritt, kann der Verlauf einer Paracetamol-Vergiftung in vier aufeinander folgenden Phasen beschrieben werden: präklinische toxische Wirkungen (Phase eins), Leberschädigung (Phase zwei), Leberversagen (Phase drei) und Erholung (Phase vier).6,22 Bei Patienten, die in der präklinischen Phase behandelt werden, kann es zu einer vorübergehenden Leberschädigung kommen, die sich jedoch vollständig erholt.22 Patienten, die erst behandelt werden, wenn bereits eine Leberschädigung vorliegt, haben eine unterschiedliche Prognose; bei Patienten mit Leberversagen liegt die Sterblichkeitsrate jedoch bei 20 % bis 40 %.22
Die erste Phase tritt einige Stunden nach der Einnahme einer toxischen Dosis auf und dauert 12 bis 24 Stunden. Es ist wichtig, die Verzögerung beim Auftreten von Symptomen zu beachten, da Gesundheitsdienstleister die Auswirkungen der Toxizität, die auf diese Ruhephase folgt, verstehen sollten. Die Symptome während der ersten 24 Stunden sind weder diagnostisch noch spezifisch und umfassen Übelkeit, Erbrechen, Diaphorese, Anorexie und Lethargie, deren Schweregrad in direktem Zusammenhang mit der Höhe der eingenommenen Dosis steht.8
In der zweiten Phase, die bis zu 24 bis 48 Stunden nach der Einnahme auftritt, kann ein falsches Gefühl der Genesung auftreten, da sich die Symptome des Magen-Darm-Trakts verbessern oder verschwinden.6,8 Wenn die Hepatotoxizität jedoch weiter zunimmt, können Bauchschmerzen oder Druckempfindlichkeit im rechten oberen Quadranten auftreten. Außerdem beginnen die Laborwerte, Anzeichen einer Hepatotoxizität zu zeigen; Leberenzyme, Laktat, Phosphat, Prothrombinzeit und internationales normalisiertes Verhältnis (INR) steigen dramatisch an.6,8,12 Die meisten Patienten kommen über dieses Stadium nicht hinaus, insbesondere wenn das Gegenmittel Acetylcystein verabreicht wird.8,12
Ein paar Patienten erreichen die dritte Phase, die in der Regel nach 3 bis 5 Tagen eintritt. Diese Phase ist gekennzeichnet durch das Wiederauftreten oder die Verschlimmerung von Übelkeit und Erbrechen, begleitet von Unwohlsein, Gelbsucht und zentralnervösen Symptomen wie Verwirrung, Somnolenz und Koma.6 Es kann zu einer schweren und möglicherweise tödlichen Lebernekrose kommen. Obwohl weniger häufig, kann eine Niereninsuffizienz, die sich durch Oligurie zeigt, als Folge einer Acetaminophen-induzierten tubulären Nekrose auftreten.6,8,12 Die Leberenzymwerte erreichen ihren Höchststand und können bis zu 10.000 IU/L betragen. Gelbsucht, Hypoglykämie, Blutungs- und Gerinnungsanomalien sowie hepatische Enzephalopathie sind ebenfalls zu beobachten.8,12 Der Tod kann als Folge der mit dem Leberversagen verbundenen Komplikationen eintreten, einschließlich Multiorganversagen, Hirnödem und Sepsis.15
Die vierte Phase schließlich umfasst das Überleben und die Genesung, wobei im Allgemeinen die volle Leberfunktion wiederhergestellt ist und keine Langzeitfolgen auftreten.6 Etwa 70 % der Patienten, die in die vierte Phase eintreten, erholen sich vollständig, während 1 bis 2 % der Patienten ein tödliches Leberversagen entwickeln.6 Eine schwere, unbehandelte Paracetamol-Toxizität führt innerhalb von 4 bis 18 Tagen nach der Einnahme zum Tod.6
Patienten mit erhöhtem Risiko
Da der Mechanismus der Paracetamol-Toxizität über die Bildung von NAPQI erfolgt, wirken sich alle Faktoren, die die Verfügbarkeit von Stoffwechselenzymen beeinflussen, auf die Toxizität aus. Alkoholkonsum, Unterernährung und die Induktion von CYP450-Enzymen durch Medikamente, einschließlich der Langzeitbehandlung mit Carbamazepin, Primidon, Rifampin, Efavirenz und Johanniskraut, können sich darauf auswirken, wie eine Person auf Acetaminophen reagiert.23 Patienten, die von einem der oben genannten Faktoren betroffen sind, sollten identifiziert werden, damit Apotheker sie eingehend über die sichere Verwendung von Paracetamol beraten können.
Akut wirkt Ethanol sowohl als Substrat als auch als Inhibitor von CYP2E1, wodurch die Menge des gebildeten NAPQI begrenzt wird. Umgekehrt ist Ethanol bei chronischem Alkoholkonsum ein Induktor von CYP2E1, was bei einer Überdosierung von Paracetamol zu einem potenziellen Anstieg der Bildung von NAPQI führt. Eine weitere Folge des chronischen Alkoholkonsums ist die Erschöpfung der Glutathionspeicher, wodurch der letzte Schutz gegen die Bildung von NAPQI verringert wird.17 Es gibt keine Hinweise darauf, dass die Verwendung von Paracetamol in therapeutischen Dosen bei einer alkoholabhängigen Person toxisch ist; daher kann Paracetamol in therapeutischen Mengen sowohl akut als auch chronisch sicher verwendet werden.23-25
Auch wenn dies umstritten ist, sind Hunger (längeres Fasten) und Unterernährung zusätzliche Risikofaktoren für die Paracetamol-Toxizität.16,18,23 Ähnlich wie bei chronischem Alkoholkonsum führt Unterernährung zu einer Erschöpfung der Glutathion-Speicher. Es gibt jedoch auch Hinweise darauf, dass die CYP2E1-Funktion in dieser Patientenpopulation deutlich reduziert ist. Diese Effekte würden sich somit gegenseitig aufheben, so dass sich die Toxizität möglicherweise nicht verändert.26 Dennoch ist es ratsam, solche Patienten zu identifizieren und sie auf ihr erhöhtes Risikopotenzial hinzuweisen.
Management
Bei der Vorstellung sollte der Patient gründlich untersucht werden. Es sollte eine ausführliche Medikamentenanamnese erhoben werden. Der Acetaminophen-Serumspiegel sollte idealerweise mindestens 4 Stunden nach der Einnahme bestimmt werden. Apotheker können eine wichtige Rolle spielen, indem sie sachdienliche Informationen sammeln, wie z. B. die eingenommene Medikamentenmenge, die eingenommene Darreichungsform, die Zeit, die seit der letzten Einnahme verstrichen ist, und ob andere Medikamente eingenommen wurden. All diese Faktoren sind wichtig für die Analyse der Paracetamolkonzentration im Serum.
Wenn der Patient innerhalb einer Stunde nach der Einnahme vorstellig wird, kann eine Magendekontamination in Betracht gezogen werden; Aktivkohle ist die einzige empfohlene Methode zur Dekontamination des Magen-Darm-Trakts. Die Verabreichung von Aktivkohle kann in Erwägung gezogen werden, insbesondere bei Patienten, die Paracetamol mit verzögerter Wirkstofffreisetzung eingenommen oder andere Medikamente eingenommen haben, die die Absorption von Paracetamol verlangsamen.12 Aufgrund der schnellen Absorptions- und Verteilungsphase von Paracetamol spielt diese Methode im Laufe der Zeit jedoch kaum noch eine Rolle.27-29 Aktivkohle sollte nur verabreicht werden, wenn der Patient geistig wach ist und die Atemwege intakt sind. Sie sollte auch bei Patienten mit erhöhtem Aspirationsrisiko, unkontrolliertem Erbrechen oder bei gleichzeitiger Einnahme eines ätzenden oder krampflösenden Mittels vermieden werden.30
Acetylcystein: Die Hauptstütze der Behandlung von Paracetamol-Toxizität ist Acetylcystein. Dieser Wirkstoff füllt die hepatischen Glutathionspeicher auf und erhöht die Sulfatkonjugation, wodurch die Akkumulation von NAPQI verhindert wird.31 Acetylcystein kann bei Patienten mit Acetaminophen-induziertem Leberversagen von Vorteil sein, da es die Hämodynamik und den Sauerstoffverbrauch verbessert, das Hirnödem verringert und die mitochondriale Energieproduktion verbessert.14,22
Acetylcystein kann ein Leberversagen infolge einer Paracetamol-Überdosis verhindern, wenn es früh genug verabreicht wird (innerhalb von 8-10 Stunden nach einer akuten Überdosis), kann aber auch noch bis zu 48 Stunden nach der Einnahme von Nutzen sein.6,11,14,31 Das Standard-Nomogramm für Paracetamol-Toxizität, das Rumack-Matthew-Nomogramm, kann zur Bestimmung der Wahrscheinlichkeit einer schweren Leberschädigung verwendet werden. Es ist jedoch unwirksam, wenn es um die Bewertung einer möglichen Toxizität aufgrund mehrfacher Einnahme im Laufe der Zeit geht, wenn der Zeitpunkt der Einnahme nicht bekannt ist oder wenn ein veränderter Metabolismus auftritt.11 In Anbetracht dessen sollte Acetylcystein in jedem Fall eines akuten Leberversagens oder bei Anzeichen einer Lebertoxizität verabreicht werden, wenn eine Überdosierung von Paracetamol vermutet wird.11
Acetylcystein ist oral und intravenös erhältlich; die Wahl hängt vom klinischen Szenario ab.21 Die orale Verabreichung kann bei Patienten mit präklinischen toxischen Wirkungen oder Leberschäden von Vorteil sein, obwohl das Vorhandensein eines veränderten mentalen Status und Erbrechen den Einsatz einschränken kann.22 Das Dosierungsschema für orales Acetylcystein ist eine Ladedosis von 140 mg/kg, gefolgt von 17 Dosen von 70 mg/kg alle 4 Stunden über einen Zeitraum von insgesamt 72 Stunden.11 Patienten mit Leberversagen sollten eine IV-Therapie erhalten.22 Empfohlen wird eine kontinuierliche IV-Infusion mit einer Ladedosis von 150 mg/kg in 200 ml D5W, die über 60 Minuten infundiert wird, gefolgt von einer Erhaltungsdosis von 50 mg/kg über 4 Stunden, gefolgt von einer zweiten Erhaltungsdosis von 100 mg/kg in 1.000 ml D5W, die über 16 Stunden verabreicht wird.11 Wenn der Patient weniger als 40 kg wiegt, sollte die Flüssigkeitszufuhr gemäß den Leitlinien angepasst werden, um Flüssigkeitsüberlastung, Hyponatriämie und Krampfanfälle zu vermeiden. Wenn es dem Patienten gut geht, er sich aber nach der empfohlenen Dosierung noch nicht vollständig erholt hat, kann die Acetylcystein-Therapie entweder mit der letzten oralen Dosis oder der letzten IV-Infusionsrate fortgesetzt werden. Acetylcystein sollte über die Dauer des Protokolls hinaus fortgesetzt werden, bis die Acetaminophen-Konzentrationen nicht mehr nachweisbar sind, sich die AST-Werte im Serum normalisiert oder deutlich verbessert haben und alle Anzeichen eines Leberversagens verschwunden sind.13
Aufgrund des unangenehmen Geschmacks und Geruchs kommt es bei der oralen Verabreichung von Acetylcystein häufig zu Erbrechen.31,32 Zu den unerwünschten Wirkungen von intravenös verabreichtem Acetylcystein gehören anaphylaktoide Reaktionen wie Hautausschlag, Juckreiz, Angioödem, Bronchospasmus, Tachykardie und Hypertonie.31,32 Darüber hinaus müssen Apotheker bei der intravenösen Verabreichung von Acetylcystein auf die Gefahr von Medikationsfehlern achten. Das komplizierte Schema, die Dauer der Therapie und die Notwendigkeit, dass mehrere medizinische Fachkräfte die Dosen an verschiedenen Behandlungsorten verabreichen, erhöhen das Risiko von Fehlern erheblich.33 In einer retrospektiven Studie wurde eine 33%ige Inzidenz von Medikationsfehlern bei der intravenösen Verabreichung von Acetylcystein festgestellt.33 Die häufigste Fehlerart, die in dieser Studie festgestellt wurde, war eine Verzögerung der Therapie, die die Wirksamkeit von Acetylcystein potenziell verringern kann. Ein weiterer häufiger Fehler war die unnötige Verabreichung von Acetylcystein, was zu unnötigen Kosten führte. Es ist wichtig, dass Gesundheitsdienstleister in Fällen von Paracetamol-Überdosierungen die Giftnotrufzentralen konsultieren. Sie können die aktuellsten Dosierungsinformationen und Protokolle zur Verfügung stellen, um eine ordnungsgemäße Verabreichung von Acetylcystein zu gewährleisten.
FDA-Kennzeichnung
In der Hoffnung, die Sicherheit zu erhöhen und die Toxizität zu verringern, aktualisiert die FDA seit langem ihre Empfehlungen zur Verwendung von Paracetamol. In den späten 1990er Jahren zeigten Untersuchungen, dass Paracetamol eine der Hauptursachen für akutes Leberversagen in den USA war, wobei die meisten Fälle auf eine versehentliche Überdosierung zurückzuführen waren.34 1998 gab die FDA einen Warnhinweis auf Paracetamolprodukten heraus, der Patienten, die mehr als drei alkoholische Getränke pro Tag konsumierten, dringend empfahl, vor der Einnahme dieses Medikaments einen Arzt zu konsultieren. Als die Jahre vergingen und der Zusammenhang zwischen Paracetamol und Lebertoxizität immer deutlicher wurde, berief die FDA eine Sitzung ein, um auf diese Erkenntnisse zu reagieren. Im Jahr 2002 empfahl der FDA-Beratungsausschuss, alle Paracetamol-haltigen Produkte mit einem Warnhinweis zur Lebertoxizität zu versehen. Im Jahr 2009 wurde eine neue Kennzeichnung entwickelt, mit der Patienten leicht erkennen können, welche Produkte Paracetamol enthalten, wodurch die Gefahr einer versehentlichen Überdosierung verringert wird. Später wurde auf allen verschreibungspflichtigen Paracetamol-Produkten eine Blackbox-Warnung angebracht, die das potenzielle Risiko für schwere Leberschäden hervorhebt, und es wurde eine Warnung vor seltenen, aber schwerwiegenden Anaphylaxien und anderen Überempfindlichkeitsreaktionen eingeführt.34
Im August 2013 warnte die FDA die Verbraucher vor seltenen, aber schwerwiegenden und potenziell tödlichen Hautreaktionen wie dem Stevens-Johnson-Syndrom (SJS), der toxischen epidermalen Nekrolyse (TEN) und der akuten generalisierten exanthematischen Pustulose (AGEP) im Zusammenhang mit der Einnahme von Paracetamol.35 Patienten sollten auf Anzeichen und Symptome von Hautreaktionen wie Schälen, Blasenbildung, Rötung und Ablösen der Haut hingewiesen werden, wobei sie die weitere Einnahme des Medikaments einstellen und sofort einen Arzt aufsuchen sollten.
Die FDA hat außerdem angekündigt, dass ab Januar 2014 die Paracetamolmenge in verschreibungspflichtigen Kombinationsprodukten auf 325 mg pro Tablette oder Kapsel begrenzt werden muss.36,37 Im Mai 2011 kündigten die Hersteller rezeptfreier Paracetamolprodukte freiwillig an, dass nur noch eine einzige Kinderstärke von flüssigem Paracetamol (160 mg/5 ml) erhältlich sein wird; die konzentrierten Säuglingstropfen werden nicht mehr hergestellt.38
Auch wenn Fortschritte erzielt wurden, sind einige Dinge noch nicht geklärt. Der Beratende Ausschuss der FDA hat sich für zahlreiche Änderungen ausgesprochen, die die Sicherheit verbessern und die Toxizität verringern sollen, doch die FDA hat noch keine Maßnahmen ergriffen. So wurde beispielsweise die Tageshöchstdosis von Paracetamol bisher auf 4 g/Tag festgesetzt, während der FDA-Beratungsausschuss vorschlägt, diese Dosis zu senken, um Überdosierungen zu verringern.37 Es ist wichtig zu erwähnen, dass einige Hersteller ihre Kennzeichnung bereits aktualisiert haben, um diesen Empfehlungen Rechnung zu tragen, obwohl dies noch nicht vorgeschrieben ist. Es werden auch Anstrengungen unternommen, um die Produktkennzeichnung zu verbessern, die Patientenaufklärung zu verstärken, eine universelle pädiatrische Formulierung zu schaffen, Paracetamol-Kombinationsprodukte zu eliminieren und die Stärke von rezeptfreien Paracetamolprodukten auf 325 mg pro Tablette mit einer maximalen Einzeldosis von 650 mg zu reduzieren.37 Auch wenn zu keinem dieser Punkte ein endgültiger Konsens erzielt wurde, sollten Gesundheitsdienstleister ihre Patienten darüber aufklären, wie wichtig es ist, die Anweisungen auf dem Etikett zu befolgen.
Rolle des Apothekers
Apotheker sind in der Lage, die sichere Verwendung von Paracetamol wirksam zu fördern. Viele Patienten sind sich der maximalen Tagesdosis von Paracetamol und des Toxizitätspotenzials nicht bewusst.39 Darüber hinaus ist den Patienten möglicherweise nicht klar, dass Paracetamol in mehr als 600 verschiedenen Produkten enthalten ist.39 Alle Patienten, die ein Rezept für ein Paracetamol-haltiges Produkt erhalten, müssen beraten werden, um sicherzustellen, dass sie über den Wirkstoff informiert sind. Apotheker müssen bei der Aufklärung von Patienten, die rezeptfreie Paracetamolprodukte kaufen, eine proaktive Rolle übernehmen. Apotheker sind von entscheidender Bedeutung für die Verhinderung des Paracetamol-Missbrauchs, indem sie die sichere Verwendung des Medikaments durch Patientenaufklärung und eine Überprüfung der Medikamentenhistorie der Patienten gewährleisten.
Außerdem sollten Apotheker ihren Patienten empfehlen, bei Verdacht auf eine Paracetamol-Überdosierung die nationale Giftnotrufzentrale zu kontaktieren. Die gebührenfreie Nummer lautet 1-800-222-1222.40 Bei einem Anruf unter dieser Nummer werden die Patienten mit dem nächstgelegenen regionalen Giftnotrufzentrum verbunden, in dem Spezialisten 24 Stunden am Tag und 7 Tage die Woche erreichbar sind. Diese Spezialisten können bei der Beurteilung und Behandlung einer möglichen Paracetamol-Überdosierung helfen. Dadurch wird das Risiko einer unangemessenen Dosierung, einer doppelten Therapie und eines unangemessenen Arzneimittelgebrauchs minimiert.
1. Kaufman DW, Kelly JP, Rosenberg L, et al. Recent patterns of medication use in the ambulatory adult population of the United States: the Slone survey. JAMA. 2002;287:337-344.
2. Paulose-Ram R, Hirsch R, Dillon C, et al. Verschreibungspflichtige und nicht verschreibungspflichtige Analgetika in der erwachsenen Bevölkerung der USA: Ergebnisse der dritten National Health and Nutrition Examination Survey (NHANES III). Pharmacoepidemiol Drug Saf. 2003;12:315-326.
3. Paulose-Ram R, Hirsch R, Dillon C, et al. Frequent monthly use of selected nonprescription and prescription non-narcotic analgesics among U.S. adults. Pharmacoepidemiol Drug Saf. 2005;14:257-266.
4. Burke A, Smyth EM, Fitzgerald GA. Analgetika-Antipyretika; Pharmakotherapie der Gicht. In: Brunton LL, Laso JS, Parker K, eds. Goodman and Gilman’s the Pharmacological Basis of Therapeutics. 11th ed. New York, NY: McGraw-Hill; 2006:671-716.
5. Watkins PB, Kaplowitz N, Slattery JT, et al. Amino-Transferase-Erhöhungen bei gesunden Erwachsenen, die täglich 4 Gramm Paracetamol erhalten: eine randomisierte kontrollierte Studie. JAMA. 2006;296:87-93.
6. Chun LJ, Tong MJ, Busuttil RW, et al. Acetaminophen hepatotoxicity and acute liver failure. J Clin Gastroenterol. 2009;43:342-349.
7. Bronstein AC, Spyker DA, Cantilena LR, et al. 2011 annual report of the American Association of Poison Control Centers‘ National Poison Data System (NPDS): 29th annual report. Clin Toxicol. 2012;50:911-1164.
8. Schilling A, Corey R, Leonard M, et al. Acetaminophen: old drug, new warnings. Cleve Clin J Med. 2010;77:19-27.
9. Nourjah P, Ahmad SR, Karwoski C, et al. Estimates of acetaminophen (paracetamol)-associated overdoses in the United States. Pharmacoepidemiol Drug Saf. 2006;15:398-405.
10. Larson AM, Polson J, Fontana RJ, et al. Acetaminophen-induziertes akutes Leberversagen: Ergebnisse einer multizentrischen, prospektiven Studie in den USA. Hepatology. 2005;42:1364-1372.
11. Lee WM, Larson AM, Stravitz T. AASLD position paper: the management of acute liver failure: update 2011. Baltimore, MD: American Association for the Study of Liver Diseases; September 2011. www.aasld.org/practiceguidelines/Documents/AcuteLiverFailureUpdate2011.pdf. Accessed December 15, 2013.
12. Tylenol (Paracetamol) – Professionelle Produktinformation. Fort Washington, PA: McNeil Consumer Healthcare; 2010.
13. Hendrickson RG. Acetaminophen. In: Nelson LS, Lewin NA, Howland M, eds. Goldfrank’s Toxicologic Emergencies. 9th ed. New York, NY: McGraw-Hill; 2011:483-99.
14. Hodgman MJ, Garrard AR. A review of acetaminophen poisoning. Crit Care Clin. 2012;499-516.
15. Larson AM. Acetaminophen hepatotoxicity. Clin Liver Dis. 2007;11:525-548.
16. Rumack BH. Acetaminophen-Hepatotoxizität: die ersten 35 Jahre. J Toxicol Clin Toxicol. 2002;40:3-20.
17. Nelson SD. Molekulare Mechanismen der durch Acetaminophen verursachten Hepatotoxizität. Semin Liver Dis. 1990;10:267-278.
18. Lee WH. Drug-induced hepatotoxicity. N Engl J Med. 1995;333:1118-1127.
19. Fontana RJ. Akutes Leberversagen bei Überdosierung von Paracetamol. Med Clin North Am. 2008;92:761-794.
20. American Academy of Pediatrics Committee on Drugs. Acetaminophen toxicity in children. Pediatrics. 2001;108:1020-1024.
21. Dart RC, Erdman AR, Olson KR, et al. Acetaminophen poisoning: an evidence-based consensus guideline for out-of-hospital management. Clin Toxicol. 2006;44:1-18.
22. Heard KJ. Acetylcystein bei Paracetamol-Vergiftungen. N Engl J Med. 2008;359:285-292.
23. Ferner RE, Dear JW, Bateman DN. Management of paracetamol poisoning. BMJ. 2011;342:d2218.
24. Kuffner EK, Dart RC, Bogdan GM, et al. Effect of maximum daily doses of acetaminophen on the liver of alcoholic patients: a randomized, double-blind, placebo-controlled trial. Arch Intern Med. 2001;161:2247-2252.
25. Kuffner EK, Green JL, Bogdan GM, et al. The effect of acetaminophen (four grams a day for three consecutive days) on hepatic tests in alcoholic patients-a multicenter randomized study. BMC Med. 2007;5:13.
26. Rumack BH. Acetaminophen misconceptions. Hepatology. 2004;40:10-15.
27. Christophersen AB, Levin D, Hoegberg LC, et al. Aktivkohle allein oder nach Magenspülung: eine simulierte große Paracetamol-Intoxikation. Br J Clin Pharmacol. 2002;53;312-317.
28. Sato RL, Wong JJ, Sumida SM, et al. Efficacy of super-activated charcoal administration late (3 hours) after acetaminophen overdose. Am J Emerg Med. 2003;21:189-191.
29. Spiller HA, Winter ML, Klein-Schwartz W, et al. Efficacy of activated charcoal administered more than four hours after acetaminophen overdose. J Emerg Med. 2006;30:1-5.
30. Chyka PA, Seger D, Krenzelok EP, et al. Positionspapier: Single-dose activated charcoal. Clin Toxicol. 2005;43:61-87.
31. Kozer E, Koren G. Management of paracetamol overdose: current controversies. Drug Safety. 2001;24:503-512.
32. Sandilands EA, Bateman DN. Unerwünschte Reaktionen im Zusammenhang mit Acetylcystein. Clin Toxicol. 2009;47:81-88.
33. Hayes BD, Klein-Schwartz W, Doyon S. Frequency of medication errors with intravenous acetylcysteine for acetaminophen overdose. Ann Pharmacother. 2008;42:766-770.
34. June 29-30, 2009: Gemeinsame Sitzung des Beratenden Ausschusses für Arzneimittelsicherheit und Risikomanagement mit dem Beratenden Ausschuss für Anästhetika und lebenserhaltende Medikamente und dem Beratenden Ausschuss für nicht verschreibungspflichtige Medikamente: FDA Briefing Material. Updated July 30, 2013. www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/Drugs/DrugSafetyandRiskManagementAdvisoryCommittee/UCM164897.pdf. Accessed December 15, 2013.
35. FDA Drug Safety Communication: FDA warnt vor seltenen, aber schwerwiegenden Hautreaktionen mit dem Schmerzmittel/Fiebersenker Acetaminophen. August 1, 2013. www.fda.gov/Drugs/DrugSafety/ucm363041.htm. Accessed December 16, 2013.
36. FDA Drug Safety Communication: Verschreibungspflichtige Paracetamol-Produkte sollen auf 325 mg pro Dosierungseinheit begrenzt werden; Warnhinweis im Kasten hebt das Potenzial für schweres Leberversagen hervor. January 13, 2011. www.fda.gov/Drugs/DrugSafety/ucm239821.htm. Accessed December 16, 2013.
37. Krenzelok EP. Commentary: the FDA Acetaminophen Advisory Committee meeting. Was ist die Zukunft von Paracetamol in den Vereinigten Staaten? The perspective of a committee member. Clin Toxicol. 2009;47:784-789.
38. Pappas M, Bryan K. OTC industry announces voluntary transition to one concentration of single-ingredient pediatric liquid acetaminophen medicines. Consumer Health Care Products. May 11, 2011. www.chpa.org/05_04_11_PedAcet.aspx. Accessed December 15, 2013.
39. Hornsby LB, Whitley HP, Hester EK, et al. Survey of patient knowledge related to acetaminophen recognition, dosing, and toxicity. J Am Pharm Assoc. 2010;50:485-489.
40. American Association of Poison Control Centers. www.aapcc.org. Accessed February 25, 2014.