Formation posologique : gélule, liquide rempli
Médicaments examinés par Drugs.com. Dernière mise à jour le 1er avril 2020.
- Aperçu
- Effets secondaires
- Dosage
- Professionnel
- Interactions
- Plus
- Vitamine D Ergocalciférol Description
- Vitamine D Ergocalciférol – Pharmacologie clinique
- Indications et utilisation de la vitamine D Ergocalciférol
- Contre-indications
- Avertissements
- Précautions
- Généralités
- Interactions médicamenteuses
- Carcinogenèse, mutagenèse, altération de la fertilité
- Grossesse Catégorie C
- Mères allaitantes
- Utilisation pédiatrique
- Utilisation gériatrique
- Effets indésirables
- Surdosage
- Les effets de la vitamine D administrée peuvent persister pendant deux mois ou plus après l’arrêt du traitement.
- Vitamine D Ergocalciférol Posologie et administration
- Comment la vitamine D Ergocalciférol est-elle fournie
- Étiquette d’emballage.PANNEAU D’AFFICHAGE PRINCIPAL
- Plus d’informations sur l’ergocalciférol
- Ressources pour les consommateurs
- Ressources pour les professionnels
- Guides thérapeutiques associés
- Guides de traitement associés
Vitamine D Ergocalciférol Description
Gélules d’ergocalciférol, USP sont un régulateur synthétique du calcium pour une administration orale.
L’ergocalciférol est un cristal blanc, incolore, insoluble dans l’eau, soluble dans les solvants organiques et légèrement soluble dans les huiles végétales. Il est affecté par l’air et par la lumière. L’ergostérol ou provitamine D 2 se trouve dans les plantes et les levures et n’a pas d’activité antirachitique.
Il existe plus de 10 substances appartenant à un groupe de composés stéroïdes, classées comme ayant une activité vitaminique D ou antirachitique.
Une unité USP de vitamine D 2 est équivalente à une unité internationale (UI), et 1 mcg de vitamine D 2 est égal à 40 unités USP.
Chaque capsule contient de la vitamine D (Ergocalciférol) 1,25 mg équivalent à 50 000 unités USP dans une huile végétale comestible.
L’ergocalciférol, également appelé vitamine D 2, est le 9,10-sécoergosta-5,7,10(19), 22-tétraène-3-ol, (3β,5Z,7E,22 E)- ; (C 28H 44O) avec un poids moléculaire de 396,65, et a la formule structurelle suivante:
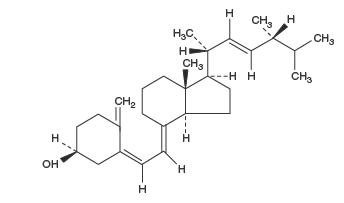
Ingrédients inactifs : FD&C Bleu #1, FD&C Jaune #5, gélatine, glycérine, lécithine, triglycéride à chaîne moyenne, eau purifiée, glaçage à la gomme-laque, alcool N-butylique, siméthicone, huile de soja et dioxyde de titane.
Vitamine D Ergocalciférol – Pharmacologie clinique
La synthèse in vivo des principaux métabolites biologiquement actifs de la vitamine D se produit en deux étapes. La première hydroxylation de l’ergocalciférol a lieu dans le foie (en 25-hydroxyvitamine D) et la seconde dans les reins (en 1, 25-dihydroxyvitamine D). Les métabolites de la vitamine D favorisent l’absorption active du calcium et du phosphore par l’intestin grêle, ce qui élève suffisamment les taux sériques de calcium et de phosphate pour permettre la minéralisation osseuse. Les métabolites de la vitamine D mobilisent également le calcium et le phosphate des os et augmentent probablement la réabsorption du calcium et peut-être aussi du phosphate par les tubules rénaux.
Il existe un décalage de 10 à 24 heures entre l’administration de la vitamine D et le début de son action dans l’organisme en raison de la nécessité de la synthèse des métabolites actifs dans le foie et les reins. L’hormone parathyroïdienne est responsable de la régulation de ce métabolisme dans les reins.
Indications et utilisation de la vitamine D Ergocalciférol
Les capsules d’ergocalciférol, USP sont indiquées pour le traitement de l’hypoparathyroïdie, du rachitisme réfractaire, également appelé rachitisme résistant à la vitamine D, et de l’hypophosphatémie familiale.
Contre-indications
Les capsules d’ergocalciférol, USP sont contre-indiquées chez les patients présentant une hypercalcémie, un syndrome de malabsorption, une sensibilité anormale aux effets toxiques de la vitamine D et une hypervitaminose D.
Avertissements
L’hypersensibilité à la vitamine D peut être un facteur étiologique chez les nourrissons présentant une hypercalcémie idiopathique. Dans ces cas, la vitamine D doit être strictement limitée.
Garder hors de portée des enfants.
Précautions
Généralités
L’administration de vitamine D à partir d’aliments enrichis, de compléments alimentaires, de sources auto-administrées et de médicaments sur ordonnance doit être évaluée. La posologie thérapeutique doit être réajustée dès qu’il y a une amélioration clinique. Les niveaux de dosage doivent être individualisés et une grande prudence doit être exercée pour éviter des effets toxiques graves. DANS LE CAS DU RACHITISME RÉSISTANT À LA VITAMINE D, LA FOURCHETTE ENTRE LES DOSES THÉRAPEUTIQUES ET TOXIQUES EST ÉTROITE. Lorsque des doses thérapeutiques élevées sont utilisées, les progrès doivent être suivis par des déterminations fréquentes du calcium sanguin.
Dans le traitement de l’hypoparathyroïdie, le calcium intraveineux, l’hormone parathyroïdienne et/ou le dihydrotachystérol peuvent être nécessaires.
Le maintien d’un taux normal de phosphore sérique par une restriction alimentaire en phosphate et/ou l’administration de gels d’aluminium comme liants intestinaux du phosphate chez les patients présentant une hyperphosphatémie comme cela est fréquemment observé dans l’ostéodystrophie rénale est essentiel pour prévenir la calcification métastatique.
Une quantité adéquate de calcium alimentaire est nécessaire pour une réponse clinique au traitement par la vitamine D.
Ce produit contient du FD&C jaune n°5 (tartrazine) qui peut provoquer des réactions de type allergique (y compris de l’asthme bronchique) chez certaines personnes sensibles. Bien que l’incidence globale de la sensibilité au FD&C jaune n° 5 (tartrazine) dans la population générale soit faible, elle est fréquemment observée chez les patients qui présentent également une hypersensibilité à l’aspirine.
Protéger de la lumière.
Interactions médicamenteuses
L’huile minérale interfère avec l’absorption des vitamines liposolubles, y compris les préparations de vitamine D.
L’administration de diurétiques thiazidiques à des patients hypoparathyroïdiens traités simultanément par des capsules d’ergocalciférol, USP peut provoquer une hypercalcémie.
Carcinogenèse, mutagenèse, altération de la fertilité
Aucune étude animale à long terme n’a été réalisée pour évaluer le potentiel du médicament dans ces domaines.
Grossesse Catégorie C
Des études de reproduction animale ont montré des anomalies fœtales chez plusieurs espèces associées à une hypervitaminose D. Celles-ci sont similaires au syndrome de sténose aortique supravalvulaire décrit chez les nourrissons par Black en Angleterre (1963). Ce syndrome était caractérisé par une sténose aortique supravalvulaire, un faciès d’elfe et un retard mental. Par conséquent, pour la protection du fœtus, l’utilisation de la vitamine D au-delà de l’apport alimentaire recommandé pendant une grossesse normale devrait être évitée à moins que, selon le jugement du médecin, les avantages potentiels dans un cas spécifique et unique l’emportent sur les risques importants encourus. L’innocuité au-delà de 400 unités USP de vitamine D par jour pendant la grossesse n’a pas été établie.
Mères allaitantes
La prudence est de mise lorsque les capsules d’ergocalciférol, USP sont administrées à une femme allaitante. Chez une mère ayant reçu de fortes doses de vitamine D, le 25-hydroxycholécalciférol est apparu dans le lait et a provoqué une hypercalcémie chez son enfant. Une surveillance de la concentration de calcium sérique du nourrisson est nécessaire dans ce cas (Goldberg, 1972).
Utilisation pédiatrique
Les doses pédiatriques doivent être individualisées (voir POSOLOGIE ET ADMINISTRATION).
Utilisation gériatrique
Les études cliniques des capsules d’ergocalciférol, USP n’ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer s’ils répondent différemment des sujets plus jeunes. D’autres expériences cliniques rapportées n’ont pas identifié de différences dans les réponses entre les personnes âgées et les patients plus jeunes. Quelques rapports publiés ont suggéré que l’absorption de la vitamine D administrée par voie orale peut être atténuée chez les personnes âgées par rapport aux personnes plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente, commençant habituellement à l’extrémité inférieure de la gamme de dosage, reflétant la plus grande fréquence d’une diminution de la fonction hépatique, rénale ou cardiaque, et de maladies concomitantes ou d’autres traitements médicamenteux.
Effets indésirables
L’hypervitaminose D est caractérisée par des effets sur le système organique suivant :
Rénal : Altération de la fonction rénale avec polyurie, nycturie, polydipsie, hypercalciurie, azotémie réversible, hypertension, néphrocalcinose, calcification vasculaire généralisée ou insuffisance rénale irréversible pouvant entraîner le décès.
CNS : Retard mental.
Tissus mous : Calcification généralisée des tissus mous, y compris le cœur, les vaisseaux sanguins, les tubules rénaux et les poumons.
Squelettique : Une déminéralisation osseuse (ostéoporose) chez les adultes se produit de façon concomitante.
Déclin du taux moyen de croissance linéaire et augmentation de la minéralisation des os chez les nourrissons et les enfants (nanisme) douleurs vagues, raideur et faiblesse.
Gastro-intestinal : Nausées, anorexie, constipation.
Métabolique : Acidose légère, anémie, perte de poids.
Appellez votre médecin pour obtenir un avis médical sur les effets secondaires. Vous pouvez signaler les effets secondaires à AvKARE au 1-855-361-3993 ou aller sur www.avkare.com.
Surdosage
Les effets de la vitamine D administrée peuvent persister pendant deux mois ou plus après l’arrêt du traitement.
L’hypervitaminose D se caractérise par :
- Une hypercalcémie avec anorexie, nausées, faiblesse, perte de poids, douleurs et raideurs vagues, constipation, retard mental, anémie et acidose légère.
- Détérioration de la fonction rénale avec polyurie, nycturie, polydipsie, hypercalciurie, azotémie réversible, hypertension, néphrocalcinose, calcification vasculaire généralisée ou insuffisance rénale irréversible pouvant entraîner la mort.
- Calcification généralisée des tissus mous, y compris le cur, les vaisseaux sanguins, les tubules rénaux et les poumons. Une déminéralisation osseuse (ostéoporose) chez les adultes se produit de façon concomitante.
- Déclin du taux moyen de croissance linéaire et augmentation de la minéralisation des os chez les nourrissons et les enfants (nanisme).
Le traitement de l’hypervitaminose D avec hypercalcémie consiste en un retrait immédiat de la vitamine, un régime pauvre en calcium, un apport généreux en liquides, ainsi qu’un traitement symptomatique et de soutien. La crise hypercalcémique avec déshydratation, stupeur, coma et azotémie nécessite un traitement plus vigoureux. La première étape doit être l’hydratation du patient. Une solution saline intraveineuse peut augmenter rapidement et de manière significative l’excrétion urinaire de calcium. Un diurétique de l’anse (furosémide ou acide éthacrynique) peut être administré avec la perfusion saline pour augmenter davantage l’excrétion rénale de calcium. Les autres mesures thérapeutiques signalées comprennent la dialyse ou l’administration de citrates, de sulfates, de phosphates, de corticostéroïdes, d’EDTA (acide éthylènediaminetétraacétique) et de mithramycine selon des schémas appropriés. Avec un traitement approprié, la guérison est le résultat habituel lorsqu’aucun dommage permanent n’est survenu. Des décès par insuffisance rénale ou cardiovasculaire ont été rapportés.
La DL 50 chez l’animal est inconnue. La dose orale toxique d’ergocalciférol chez le chien est de 4 mg/kg.
Vitamine D Ergocalciférol Posologie et administration
L’ÉCHELLE ENTRE LES DOSES THÉRAPEUTIQUES ET TOXIQUES EST ÉTROITE.
Rickets résistants à la vitamine D : 12 000 à 500 000 unités USP par jour.
Hypoparathyroïdie : 50 000 à 200 000 unités USP par jour en concomitance avec du lactate de calcium 4 g, six fois par jour.
La posologie doit être individualisée sous étroite surveillance médicale.
L’apport en calcium doit être suffisant. Des dosages sanguins du calcium et du phosphore doivent être effectués toutes les 2 semaines ou plus fréquemment si nécessaire.
Des radiographies des os doivent être réalisées tous les mois jusqu’à ce que l’état soit corrigé et stabilisé.
Comment la vitamine D Ergocalciférol est-elle fournie
Chaque capsule contient de la vitamine D (Ergocalciférol) 1,25 mg équivalent à 50 000 unités USP. Les gélules de gélatine molle transparentes de couleur verte et de forme ovale portent l’inscription « 194 » en blanc et contiennent un liquide huileux jaune clair.
NDC 50268-297-15 (10 gélules par carte, 5 cartes par carton).
Dispensé dans un matériau de perforation blister. Pour usage institutionnel seulement.
Réservez entre 20 et 25°C (68 à 77°F) .
Protégez de la lumière.
Fabriqué pour :
AvKARE
Pulaski, TN 38478
Rev. de fabrication 03/19
AV 03/20 (P)
AvPAK
Étiquette d’emballage.PANNEAU D’AFFICHAGE PRINCIPAL

| VITAMINE D ergocalciférol gélule |
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
Étiqueteur – AvPAK (832926666)
Plus d’informations sur l’ergocalciférol
- Effets secondaires
- Pendant la grossesse
- Dosage. Information
- Images des médicaments
- Interactions médicamenteuses
- Prix& Coupons
- En Español
- 26 Critiques
- Classe de médicaments : vitamines
- Alertes de la FDA (1)
Ressources pour les consommateurs
- Informations pour les patients
Ressources pour les professionnels
- Informations posologiques
- Ergocalciférol (Conseils aux professionnels et aux patients)
- Ergocalciférol (FDA)
Autres marques Drisdol
Guides thérapeutiques associés
- . Advice)
- Ergocalciférol (FDA)
Autres marques Drisdol
Guides de traitement associés
- Hypoparathyroïdie
- Hypocalcémie
- Hypophosphatémie familiale
- Hypophosphatémie
- … +5 autres
Avis médical